
【题目】
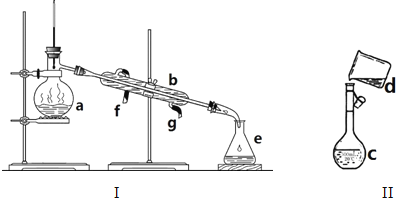
(1)写出下列仪器的名称:a. b.
(2)仪器a~e中,使用前必须检查是否漏水的有 。(填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。将仪器补充完整后进行实验,加热一会儿发现未加沸石或碎瓷片,应该选择哪种处理方式 。
A.冷却再加 B趁热加 C不采取任何方式
(4)现需配制0.1mol/·LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。(写一条)除了图中给出的仪器和托盘天平外,为完成实验还需要的玻璃仪器有: 、 ;
②根据计算得知,所需NaOH的质量为___ ___g。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作:
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.往容量瓶转移时,有少量液体溅出
D.未洗涤溶解NaOH的烧杯
E.定容时俯视刻度线
上述操作中所配溶液的物质的量浓度偏大的有(填写字母)__________
【答案】(1)蒸馏烧瓶;冷凝管(2)c(3)酒精灯,A
(4)①直接将液体水倾倒入容量瓶中或没有用玻璃棒引流;胶头滴管 玻璃棒;② 2 ;③BCAFED;④AE
【解析】试题分析:(1)a为蒸馏烧瓶,b为冷凝管,故答案为:蒸馏烧瓶;冷凝管;
(2)容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水,故答案为:c;
(3)分离四氯化碳和酒精的混合物用蒸馏的方法分离,必须用酒精灯加热;加热一会儿发现未加沸石或碎瓷片,应该冷却后再加,故选A,故答案为:酒精灯;A;
(4)①配制一定物质的量浓度的溶液是必须用玻璃棒引流,防止液体外溅,并且当滴加到离刻度线1~2cm时改用胶头滴管滴加液体,故答案为:未用玻璃棒引流;玻璃棒、胶头滴管;
②实验室没有450mL的容量瓶,应配制500mL,则需n(NaOH) =" 0.1" mol/L × 0.5L =" 0.05mol" ,m(NaOH) =" 0.05mol" × 40 g/mol = 2.0g,故答案为:2.0;
③配制溶液5000mL,配制步骤有量取、稀释、移液、洗涤移液、定容、摇匀等操作,用托盘天平称量2.0gNaOH,在烧杯中溶解,并用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤,并将洗涤液移入容量瓶,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀,所以操作顺序为BCAFED,故答案为:BCAFED;
④A.称量时用了生锈的砝码,称取的氢氧化钠质量偏大,n偏大,浓度偏大,故A正确;B.容量瓶未干燥即用来配制溶液,没有影响,故B错误;C.往容量瓶转移时,有少量液体溅出,溶质的物质的量n偏小,浓度偏小,故C错误;D.未洗涤溶解NaOH的烧杯,溶质有损耗,溶质的物质的量n偏小,浓度偏小,故D错误;E.定容时俯视刻度线,溶液的体积偏小,浓度偏大,故E正确;故答案为:AE。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.H2SO4(稀)![]() SO2
SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO3
(NH4)2SO3
B.NH3![]() NO
NO![]() NO2
NO2![]() HNO3
HNO3
C.Fe![]() FeCl2
FeCl2![]() Fe(OH)2
Fe(OH)2![]() Fe(OH)3
Fe(OH)3
D.Al![]() NaAlO2
NaAlO2![]() AlCl3溶液
AlCl3溶液![]() 无水AlCl3
无水AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始V A =V B =aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X (g) +Y (g) ![]() 2Z (g) +W (g) △H>0。达到平衡时,V A =1.2aL,则下列说法错误的是:
2Z (g) +W (g) △H>0。达到平衡时,V A =1.2aL,则下列说法错误的是:
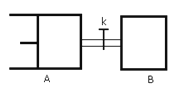
A.反应开始时,B容器中化学反应速率快
B.平衡时,A容器中X的转化率为40%,且比B容器中X的转化率大
C.打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D.打开K达新平衡后,升高温度,A容器体积一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是
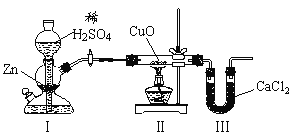
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D. CuO没有全部被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)![]() 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法错误的是
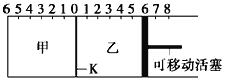
A.达到平衡时,甲容器中C的物质的量大于乙容器中C的物质的量
B.根据隔板K滑动与否可判断左右两边的反应是否达到平衡
C.达到平衡后,隔板K最终停留在左侧刻度0~1之间
D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6刻度的右侧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列有关说法不正确的是
A.常温下,48gO3和48gO2含有的原子数目为3NA
B.1molOH-l离子中含电子数目为10 NA
C.0.5L0.2mol·L-1的NaCl溶液中含有的Na+数是0.1 NA
D.33.6LCO中含有的原子总数是3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
(1)请将Au2O3之外反应物与生成物分别填入以下空格内。
![]()
(2)反应中,被还原的元素是____________,还原剂是____________。
(3)将氧化剂与还原剂填入空格中,并标出电子转移的方向和数目。
![]()
(4)纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白后布匹“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂物质的量之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一块铁的“氧化物”样品,用140mL5.0mol·L-1盐酸恰好将之完全溶解,所得溶液还能吸收0.025molCl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
A. Fe2O3 B. Fe3O4 C. Fe4O5 D. Fe5O7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com