
【题目】如图所示,向A中充入1molX和1molY,向B中充入2molX和2molY,起始V A =V B =aL,在相同温度和有催化剂的条件下,两容器中各自发生下列反应 X (g) +Y (g) ![]() 2Z (g) +W (g) △H>0。达到平衡时,V A =1.2aL,则下列说法错误的是:
2Z (g) +W (g) △H>0。达到平衡时,V A =1.2aL,则下列说法错误的是:
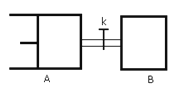
A.反应开始时,B容器中化学反应速率快
B.平衡时,A容器中X的转化率为40%,且比B容器中X的转化率大
C.打开K一段时间达平衡时,A的体积为1.6aL(连通管中气体体积不计)
D.打开K达新平衡后,升高温度,A容器体积一定增大
【答案】C
【解析】
试题分析:根据图象知,A保持恒压,B保持恒容。A.起始VA=VB=aL,B中的物质的量大于A中的物质的量,即B装置中的浓度大于A装置中的浓度,所以反应开始时,B反应速率大于A反应速率,正确;B.等压、等温条件下,气体的体积之比等于气体的物质的量之比,达到平衡时,VA=1.2a L,所以平衡后混合气体的物质的量是2.4mol。
设A物质反应了mmol,
X(g)+Y(g)![]() 2Z(g)+W(g) 物质的量增多
2Z(g)+W(g) 物质的量增多
1mol 1mol
mmol (2.4-2)mol
解得m=0.4mol,所以X物质的转化率=(0.4mol÷1mol)×100%=40%;
B装置是在等容条件下,反应向正反应方向移动时,混合气体的物质的量增大,导致容器内气体压强增大,增大压强,化学平衡向气体体积减小的逆反应方向移动,使X的转化率减小,故转化率A>B,正确;C.当打开K时,整个装置是在等温、等压条件下反应,使整个装置中气体的压强与A装置中的初始压强相同时,A和B的体积之和为3aL,其中B占aL,则A占2aL;当等温等压条件下反应达到平衡状态时,混合气体的体积是原来的1.2倍,即混合气体的体积是3.6aL,其中B是aL,所以A是2.6aL,错误;D.该反应的正反应是一个反应前后气体体积增大的吸热反应,升高温度,平衡向正反应方向移动,混合气体的物质的量增大,导致A容器的体积增大,正确。


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乙烯和苯都能使溴水褪色,因为苯和乙烯分子中都含有碳碳双键
B. 乙酸乙酯和乙烯一定条件下都能与水反应,两者属于同一类型的反应
C. 乙酸和葡萄糖都能与新制的氢氧化铜反应,两者所含的官能团相同
D. 乙烯能使溴的四氯化碳溶液和酸性高锰酸钾溶液褪色,两者褪色的本质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】萜品醇可作为消毒剂、抗氧化剂、医药和溶剂.合成α萜品醇G的路线之一如下:
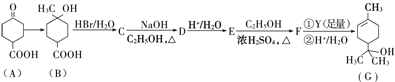
已知:RCOOC2H5![]()
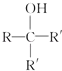 ,请回答下列问题:
,请回答下列问题:
(1)A催化氢化得Z(C7H12O3),写出Z在一定条件下聚合反应的化学方程式: .
(2)B的分子式为 ;写出一个同时满足下列条件的B的链状同分异构体的结构简式: .
①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
(3)B→C的反应类型为 .
(4)C→D的化学方程式为 .
(5)试剂Y的结构简式为 .
(6)G与H2O催化加成得不含手性碳原子(连有4个不同原子或原子团的碳原子叫手性碳原子)的化合物H,写出H的结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物X的结构简式如图所示,则下列有关说法中正确的是( )
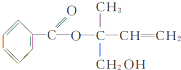
A.X的分子式为C12H16O3
B.X在一定条件下能发生加成、加聚、取代、消去等反应
C.在Ni作催化剂的条件下,1mol X最多只能与1mol H2加成
D.可用酸性高锰酸钾溶液区分苯和X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化合物B3N3H6(硼氮苯)与苯的分子结构相似,分别为

硼氮苯的二氯取代物(B3N3H4Cl2)的同分异构体的数目为( )
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼(B)、铝(Al)、镓(Ga)均属于硼族元素(第IIIA族),他们的化合物或单质都有重要用途。回答下列问题:
(1)写出基态镓原子占据的最高能层符号为________,基态铝原子有____个不同能级;基态镓原子的核外电子排布式为 。
(2)已知:无水氯化铝在178℃升华,它的蒸气是缔合的双分于(Al2Cl6),更高温度下Al2Cl6则离解生成A1Cl3单分子。
①固体氯化铝的晶体类型是 ;
②写出Al2Cl6分子的结构式 ;
③单分子A1Cl3的立体构型是 ,缔合双分子Al2Cl6中Al原子的轨道杂化类型是 。
(3)晶体硼的结构单元是正二十面体的原子晶体,其中含有20个等边三角形和一定数目的顶角,每个顶角各有一个原子,则这个基本结构单元由____个1硼原子组成,共含有____B-B键。
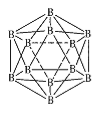
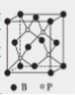
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,它是通过高温氢气氛围下(750℃)三溴化硼和三溴化磷反映值得的。BP晶胞如图所示。
①在BP晶胞中B的堆积方式为____。
②当晶胞晶格参数为acm(即途中立方体的每条边长为acm)时,磷化硼晶胞的密度为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
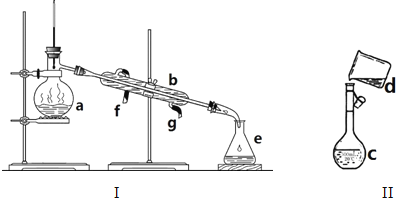
(1)写出下列仪器的名称:a. b.
(2)仪器a~e中,使用前必须检查是否漏水的有 。(填序号)
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。将仪器补充完整后进行实验,加热一会儿发现未加沸石或碎瓷片,应该选择哪种处理方式 。
A.冷却再加 B趁热加 C不采取任何方式
(4)现需配制0.1mol/·LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。(写一条)除了图中给出的仪器和托盘天平外,为完成实验还需要的玻璃仪器有: 、 ;
②根据计算得知,所需NaOH的质量为___ ___g。
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
④配制0.1 mol· L-1NaOH溶液的实验中,如果出现以下操作:
A.称量时用了生锈的砝码
B.容量瓶未干燥即用来配制溶液
C.往容量瓶转移时,有少量液体溅出
D.未洗涤溶解NaOH的烧杯
E.定容时俯视刻度线
上述操作中所配溶液的物质的量浓度偏大的有(填写字母)__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇(CH3OH)是一种重要的化工原料,广泛应用于化工生产,也可以直接用做燃料。
已知:CH3OH(1)+ O2(g) =CO(g) + 2H2O(g) ;△Ha = -443.64 kJ·mol-1
2CO (g) + O2(g) = 2CO2(g) ;△Hb =-566.0 kJ·mol-1
(1)试写出CH3OH(1)在氧气中完全燃烧生成CO2和H2O(g)的热化学方程式: 。
(2) CH3OH和H2的燃烧热分别为△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2和H2为原料合成CH3OH的热化学方程式____________________。
(3)科研人员新近开发出一种由甲醇和氧气以强碱做电解质溶液的新型手机电池,可使手机连续使用一个月才充一次电,据此回答下列问题: 甲醇在 极反应;电极反应式为 。
(4)利用电池可实现电能向化学能转化。某同学设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
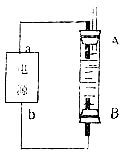
A.电源中的a一定为正极,b一定为负极 B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极 D.阴极发生的反应是:2H+ + 2e-→H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com