
| A、只含Cu2+、Fe2+、Zn2+ | B、只含Zn2+ | C、只含Fe2+、Zn2+ | D、只含Cu2+、Fe3+、Zn2+ |


科目:高中化学 来源: 题型:
 等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:
等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示:| 实验序号 | 甲 | 乙 | 丙 |
| 混合粉末质量/g | 6.2 | 18.6 | 24.8 |
| 生成气体体积(标准状况下)/mL | 2240 | 5600 | 5600 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 锌锰干电池中含NH4Cl淀粉糊(电糊)、Mn02、炭粉和锌筒(含锌、铁和铜 等)等物质(如图).
锌锰干电池中含NH4Cl淀粉糊(电糊)、Mn02、炭粉和锌筒(含锌、铁和铜 等)等物质(如图).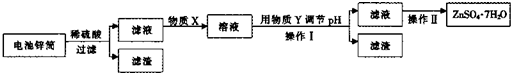
| 氢氧化物 | Fe(OH)3 | Mn(OH)2 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的pH | 2.7 | 8.1 | 7.6 | 6.5 | 4.7 |
| 完全沉淀的pH | 3.7 | 10.1 | 9.6 | 8.0 | 6.5 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河南省毕业班阶段性测试二化学试卷(解析版) 题型:选择题
将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是
A.只含Cu2+、Fe2+、Zn2+ B.只含Zn2+
C.只含Fe2+、Zn2+ D.只含Cu2+、Fe3+、Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com