
| A. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O 取代反应 | |
| B. | CH2=CH2+Br2→CH2Br-CH2Br 加成反应 | |
| C. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl 置换反应 | |
| D. | CH4$\frac{\underline{\;高温\;}}{\;}$C+2H2 氧化反应 |
分析 A、有机物分子中的某些原子或原子团被其他原子或原子团所代替的反应称为取代反应;
B、有机物分子中的不饱和键发生断裂,不饱和原子直接与其它原子或原子团相结合,生成新的化合物的反应称为加成反应;
C、置换反应指一种单质与一种化合物反应生成另外一种单与另外一种化合物的反应;
D、氧化还原反应指有化合价升降的反应.
解答 解:A、甲烷在氧气中燃烧,属于氧化反应,故A错误;
B、碳碳双键断裂,分别结合氢原子、溴原子,生成CH3-CH2Br,属于加成反应,故B正确;
C、甲烷中的氢原子被氯原子代替,生成CH3Cl,属于取代反应,故C错误;
D、甲烷分解为C单质和氢气,属于分解反应,故D错误.
故选B.
点评 本题考查了反应类型,根据概念判断,难度不大,注意概念的理解把握.


科目:高中化学 来源: 题型:解答题
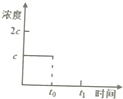 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题:| 酸 | 电离方程式 | 电离平衡常数K |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.96×10-5 |
| HClO | HClO?ClO-+H+ | 3.0×10-8 |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.4×10-7 K2=5.6×10-11 |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(B)=0.8mol/(L•s) | B. | v(A)=0.6mol/(L•s) | C. | v(C)=0.9mol/(L•s) | D. | v(B)=1.0mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
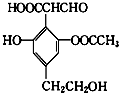
| A. | 该物质可以使酸性KMnO4溶液褪色,也可发生消去反应 | |
| B. | 可以与NaHCO3溶液反应放出CO2气体 | |
| C. | 可以与FeCl3溶液反应显色,也可与Ag(NH3)2OH反应 | |
| D. | 该物质可与H2反应,1mol该物质最多消耗5mol H2反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它与金刚石互为同素异形体 | |
| B. | 它与C60互称同分异构体 | |
| C. | 它与C60的物理性质与化学性质完全相同 | |
| D. | 它与13C互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在多电子的原子里,能量高的电子通常顺离核近的区域内运动 | |
| B. | 核外电子总是先排在能量低的电子层上,例如只有排满了K层后才排L层 | |
| C. | 两种微粒,若核外电子排布完全相同,则其化学性质一定相同 | |
| D. | 微粒的最外层只能是8个电子才稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 四 | ⑩ | ⑪ | ⑫ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | H2、I2和HI分子中的化学键都是非极性共价键 | |
| B. | 断开2mol HI分子中的化学键所需能量约为(c+b+a)kJ | |
| C. | 相同条件下,1mol H2(g)和1mol I2(g)总能量小于2molHI(g)的总能量 | |
| D. | 向密闭容器中加入2mol H2(g)和2mol I2(g),充分反应后放出的热量小于2a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
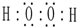 ;肼的结构式
;肼的结构式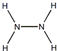 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com