
【题目】化学是认识和创造物质的科学,下列说法不正确的是( )
A.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础
B.在人类研究物质微观结构的过程中,光学显微镜、电子显微镜、扫描隧道显微镜三种不同层次的观测仪器先后得到了使用
C.根据酸碱质子理论,CO32-属于酸
D.燃煤烟气脱硫、汽车尾气的消除、二氧化碳的回收均体现了化学对环境保护的贡献
【答案】C
【解析】
A.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础,故A不符合题意;
B.光学显微镜距离直接观察原子和分子实在太遥远了,而电子显微镜虽然比光学显微镜前进了一大步,但是离开直接观察原子和分子还有一段距离,20世纪80年代初发展起来的扫描隧道显微镜是使人们能够直接观察和研究物质微观结构的新型显微镜,故B不符合题意;
C.根据酸碱质子理论,![]() 能结合质子(即H+)属于碱,故C符合题意;
能结合质子(即H+)属于碱,故C符合题意;
D.燃煤烟气的脱硫,减轻二氧化硫对空气的危害,汽车尾气的消除,减轻氮的氧化物对空气的危害,二氧化碳的回收减少温室效应,则均体现了化学对环境保护的贡献,故D不符合题意;
故答案为:C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I: CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g) ![]() H1
H1
反应II:CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g)
CH3OH(g)+ H2O(g) ![]() H2
H2
①上述反应符合“原子经济”原则的是____________(填“Ⅰ”或“Ⅱ”)。
②下表所列数据是反应I在不同温度下的化学平衡常数(K)。
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
由表中数据判断反应I为______________热反应(填“吸”或“放”)。
③某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分发生反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为_______,此时的温度为_______(从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ![]() H1kJ/mol
H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) ![]() H2kJ/mol
H2kJ/mol
③H2O(g)=H2O(l) ![]() H3 kJ/mol
H3 kJ/mol
则反应 CH3OH(l)+ O2(g)= CO(g)+ 2H2O(l) ![]() H=________kJ/mol
H=________kJ/mol
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有Cr2O72)时,实验室利用如图装置模拟该法:
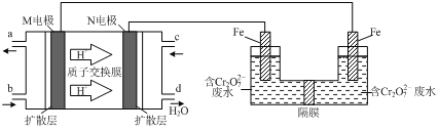
①N电极的电极反应式为____________。
②请完成电解池中Cr2O72-转化为Cr3+的离子反应方程式:
Cr2O72-+_______Fe2+ +________ [___]═ ________Cr3++_______Fe3++_________[___]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①![]() 、
、![]() 、
、![]() 属于碱性氧化物,
属于碱性氧化物,![]() 、
、![]() 、
、![]() 都能和碱溶液发生反应属于酸性氧化物
都能和碱溶液发生反应属于酸性氧化物
②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物
③混合物:漂白粉、水玻璃、![]() 胶体、冰水混合物
胶体、冰水混合物
④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物
⑤硅导电,铝在浓硫酸中钝化均属于物理变化
⑥盐酸属于混合物,而液氯、冰醋酸均属于纯净物
A.①③⑤B.④⑤⑥C.②④⑥D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】均三甲苯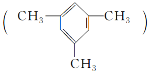 是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
是一种易燃、不溶于水、比水密度小的有毒液体,是重要的有机化工原料,用于制备合成树脂、抗氧化剂等。
(1)均三甲苯属于苯的同系物,选用一种试剂区别苯和均三甲苯:________________。
(2)均三甲苯分子中的一个H原子被Cl原子取代,所得产物有________种。
(3)下列属于苯的同系物的是________(填字母)。
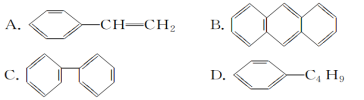
(4)下列物质中,能发生加成反应,也能发生取代反应,同时能使溴水因加成反应而褪色,还能使酸性高锰酸钾溶液褪色的是________(填字母)。
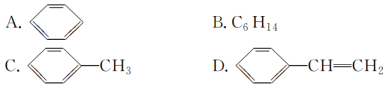
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科研工作者结合实验与计算机模拟来研究钌催化剂表面不同位点上合成氨反应历程,如图所示,其中实线表示位点A上合成氨的反应历程,虚线表示位点B上合成氨的反应历程,吸附在催化剂表面的物种用*标注。下列说法错误的是
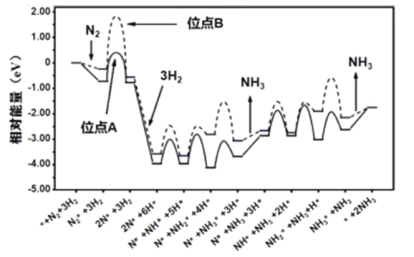
A.由图可以判断合成氨反应属于放热反应
B.氮气在位点A上转变成2N*速率比在位点B上的快
C.整个反应历程中活化能最大的步骤是2N*+3H2→2N*+6H*
D.从图中知选择合适的催化剂位点可加快合成氨的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化性:Br2 > Fe3+> I2,向含 a mol FeI2 和 a mol BaCl2 的混合溶液中缓慢通入 b mol Br2,并不断搅拌,溶液中离子的物质的量随 Br2加入的变化如图所示(不考虑盐类水解、水的电离及溶液体积变化)。则下列说法不正确的是( )
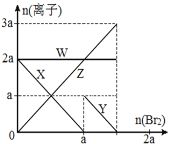
A.离子的还原性 I-> Fe2+> Br-
B.四条线与溶液中离子的对应关系是: X-Fe2+、Y-I-、Z-Br-、W-Cl-
C.当4a =3b时,反应后的离子浓度比:c(Fe2+):c(Fe3+):c(Br-) = 1:2:8
D.当3a≤2b时,发生的离子方程式:2Fe2++ 4I-+ 3Br2=2Fe3++ 2I2+6Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠NaBO2为主要原料制备NaBH4,其流程如下:
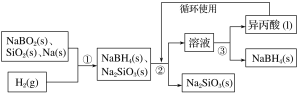
已知:NaBH4常温下能与水反应,可溶于异丙酸(沸点:33 ℃)。
(1)在第①步反应加料之前,需要将反应器加热至100 ℃以上并通入氩气,该操作的目的是______________,原料中的金属钠通常保存在________中,实验室取用少量金属钠需要用到的实验用品有________、________、玻璃片和小刀等。
(2)第②步分离采用的方法是________;第③步分离(NaBH4)并回收溶剂,采用的方法是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定质量的某有机物与足量金属钠反应生成气体VAL;相同质量的该有机物与适量的Na2CO3溶液反应生成气体VBL。已知在同温同压下VA和VB不相等,则该有机物可能是( )
①CH3CH(OH)COOH ②HOOCCOOH ③CH3CH2COOH ④![]()
A.①②B.②③C.③④D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.1 mol Cl2参加反应转移电子数一定为2NA
B.在反应KIO3 + 6HI = KI + 3I2 +3H2O中,每生成3 mol I2转移的电子数为6NA
C.根据反应中HNO3(稀)![]() NO,而HNO3(浓)
NO,而HNO3(浓)![]() NO2可知,氧化性:HNO3(稀) > HNO3(浓)
NO2可知,氧化性:HNO3(稀) > HNO3(浓)
D.含有大量NO3-的溶液中,不能同时大量存在H+、Fe2+、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com