
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:

| A、虚线框中接灵敏电流计,该装置可将化学能转化为电能 | ||||
B、虚线框中接直流电源,可能发生:Cu+H2SO4
| ||||
C、虚线框中接直流电源,可能发生:Zn+H2SO4
| ||||
| D、生成2.24L H2时,一定转移0.2 mol e- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.
(1)按官能团的不同可以对有机物进行分类,请指出下列有机物的种类,填在横线上.

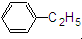

查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H2SO3) | ||
c(HS
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、H+、Cl-、OH- |
| B、Ba2+、Na+、SO42-、NO3- |
| C、Na+、Ca2+、NO3-、CO32- |
| D、Na+、Cu2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②⑤⑥ | B、②③④⑥ |
| C、②③④⑤ | D、①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向甲容器中充入一定量的氦气 |
| B、向甲容器中充入一定量的SO3气体 |
| C、升高乙容器的温度 |
| D、增大甲容器的压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,烧杯中试管内有一枚铁钉,放置数天后观察:
如图所示,烧杯中试管内有一枚铁钉,放置数天后观察:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com