
科目:高中化学 来源: 题型:
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | H | F |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、O-18原子的符号:
| ||
B、S2-的结构示意图: | ||
C、氯化氢分子的电子式:H+[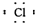 ]- ]- | ||
| D、CO2分子的结构式:O=C=O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在周期表中,族序数都等于该族元素的最外层电子数 |
| B、非金属性最强的元素,其最高价氧化物对应的水化物的酸性最强 |
| C、同周期的主族元素从左到右原子半径逐渐减小,它们形成简单离子的半径逐渐增大 |
| D、碱金属随原子序数的增大,其熔沸点逐渐降低;卤素单质随原子序数的增大,其熔沸点逐渐升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH大于7的溶液:Na+、Ba2+、SO32-、ClO- |
| B、含有0.1 mol?L-1 Fe(NO3)2的溶液:H+、Mg2+、SCN-、Cl- |
| C、使酚酞试液变红色的溶液:Na+、Ba2+、I-、Cl- |
| D、由水电离产生的c(H+)=10-13mol?L-1的溶液:NH4+、SO42-、NO3-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com