
����Ŀ��M��X��N��Z��Yԭ��������������Ķ����ڵ���������Ԫ�أ�����X��Zͬ���壬Y��Zͬ���ڣ�M��X��Y�Ȳ�ͬ�壬Ҳ��ͬ���ڡ�Xԭ�������������Ǻ�����Ӳ�����������Y������ϼ�������ͻ��ϼ۵Ĵ����͵���6��N�Ƕ���������Ԫ����ԭ�Ӱ뾶���ķǽ���Ԫ�ء�
(1)��д������Ԫ�ص�Ԫ�����ƣ�X________��M________��
(2) Y�����ڱ��е�λ��______________��д��Z���⻯��ĵ���ʽ_____________
(3) N��������������������Һ��Ӧ�Ļ�ѧ����ʽ_________________��
(4)Y��Z������������Ӧˮ���������ǿ��˳��________��________(�û�ѧʽ��ʾ)��
���𰸡��� �� �������ڢ�A�� ![]() SiO2+2NaOH=Na2SiO3+H2O HClO4 H2SO4
SiO2+2NaOH=Na2SiO3+H2O HClO4 H2SO4
��������
M��X��N��Z��Yԭ��������������Ķ����ڵ���������Ԫ�أ�Xԭ�������������Ǻ�����Ӳ�������������Xλ�ڵڶ����ڣ�����㺬��6�����ӣ�ΪOԪ�أ�X��Zͬ���壬��ZΪSԪ�أ�Y��ԭ����������S����YΪClԪ�أ�N�Ƕ���������Ԫ����ԭ�Ӱ뾶���ķǽ���Ԫ�أ���NΪSiԪ�أ�Y������ϼ�������ͻ��ϼ۵Ĵ����͵���6��Yλ�ڢ�A�壬��ԭ������С��Si����YΪFԪ�أ�M��X��Y�Ȳ�ͬ�壬Ҳ��ͬ���ڣ���MΪHԪ�أ��ݴ˷������
��������������֪��MΪHԪ�أ�XΪOԪ�أ�NΪSiԪ�أ�ZΪSԪ�أ�YΪClԪ�ء�
(1)XΪOԪ�أ�����Ϊ����MΪH������Ϊ�⣬�ʴ�Ϊ�������⣻
(2)Cl��ԭ������Ϊ17��λ�����ڱ��е������ڢ�A�壻Z���⻯��Ϊ���⣬����Ϊ���ۻ���������ʽΪ![]() ���ʴ�Ϊ���������ڢ�A�壻
���ʴ�Ϊ���������ڢ�A�壻![]() ��
��
(3)N��������ΪSiO2��SiO2��NaOH��Һ��Ӧ���ɹ����ƺ�ˮ���÷�Ӧ�Ļ�ѧ����ʽΪSiO2+2NaOH=Na2SiO3+H2O���ʴ�Ϊ��SiO2+2NaOH=Na2SiO3+H2O��
(4)�ǽ�����Խǿ������������Ӧˮ���������Խǿ���ǽ�����Cl��S��������������Ӧˮ��������ԣ�HClO4��H2SO4���ʴ�Ϊ��HClO4��H2SO4��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������(NH4)2Fe(SO4)26H2O�ֳ�Ī���Σ���dz��ɫ���塣��������(��Ҫ��FeS2��SiO2��)�Ʊ�Ī���ε��������£�

��֪��FeS2��H2SO4����Ӧ����Ӧ���ʵ��ܽ����������ͼ��
(1)FeS2��SԪ�صĻ��ϼ�Ϊ______��
(2)�������յ�����Ӧ�ǣ�4FeS2+11O2![]() 2Fe2O3+8SO2���ӿ������������ʵĴ�ʩ��______(д���㼴��)��
2Fe2O3+8SO2���ӿ������������ʵĴ�ʩ��______(д���㼴��)��
(3)��H2SO4�����������Ӧ�����ӷ���ʽΪ______��
(4)����ԭ��ʱ��Fe3+��ͨ����Ӧ������FeS2��ԭ����Ӧ��Ϊ��FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42��+16H+��Ӧ������ӷ���ʽΪ��______��
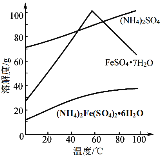
(5)�õ�Ī���ξ���IJ����ǣ�����Ũ�����ᾧ�����ˡ�ϴ�ӡ��ᾧ������ʱѡ��������¶�Ϊ60�棬����ѡ����¶ȵ�ԭ��______��
(6)Ϊ֤������Ī���ξ����к���Fe2+��NH4+��ʵ�鷽����ȡ��������Һ��һ֧�Թ�����______��֤������Fe2+��NH4+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1 mol/LNaOH��Һ�ֱ�μӵ�0.1 mol/LHA��Һ��HB��Һ�У��������Һ������Ũ����pH�ı仯��ϵ��ͼ��ʾ���ش��������⣺

��1��������Ka(HA) =_____��Ka(HB)_____ Ka(HA) (�����' �����ڡ���С�ڡ�)��
��2����Ũ�ȵ�HA��HB��Һ����Ҫ������֮һ��ˮ�ö���pHֵ��ȣ�Ӧ����_____�м�ˮ��
��3�����ֱ����Ũ�ȵ������HA��HB��Һ�м���NaOH�����ö���Һ�������ԣ��� ______��Ҫ��NaOH�ࡣ
��4��a����Һ�У�ˮ�������c(H+)=_______��b����Һ�У�c(B-)____ c(Na+)(����ڡ��������ڡ���С�ڡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������X������Y��2 mol����ij10 L�����ܱ������У�������ӦX(g)+Y(g) ![]() 2Z(g) ��H<0������ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H<0������ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t/min | 2 | 4 | 10 | 12 |
n(Y)/mol | 1.40 | 1.10 | 0.40 | 0.40 |
����˵����ȷ����
A. ��Ӧǰ2 min ��ƽ������v(Z)=3.0xl0-2 mol L-1min-1
B. ���¶��´˷�Ӧ��ƽ�ⳣ��K=64
C. ƽ��������������䣬�ٳ���2 mol Z����ƽ��ʱX�������������
D. ��Ӧ���е�10 minʱ���������������䣬�����¶ȣ���Ӧ�ﵽ��ƽ��ǰv(��)>v(����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����lOmL 1 mol L-1��HCOOH��Һ�в��ϵμ�1 mol L-1��NaOH��Һ����һֱ���ֳ��£����Ӽ�������-lgc(H+)�Ĺ�ϵ��ͼ��ʾ��c(H+)Ϊ��Һ��ˮ�������c(H+)������˵����ȷ���ǣ���

A. HCOOHΪǿ�����
B. a��b����pH��Ϊ7
C. �����Һ��pH������
D. ��a�㵽b�㣬��Һ�ĵ���������ǿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����������ʵ�鷽������̽��ij��Ӧ�Ƿ��ȷ�Ӧ�������ȷ�Ӧ��

����һ����ͼ1����С�ձ����һЩ��ȥ����������Ĥ����Ƭ��Ȼ�����ձ������10 mL 2 mol/Lϡ���ᣬ�ٲ���һ֧�¶ȼƣ��¶ȼƵ��¶���20 ��������75 �棬����¶����½�������ͣ����20 �档
����������ͼ2�����ձ��ײ������ڵ�����ճһ��СľƬ�����ձ������10 mL 2 mol/L������Һ���������м�������������Һ��Ƭ�̺������ձ�������СľƬ����������
����������ͼ3�����Թ��з���ij��ѧ��Ӧ��ʵ��ǰU�ιܺ�īˮҺ����ƽ���ڻ�ѧ��Ӧ�����У�ͨ��U�ι������īˮҺ��ߵ��ж�ij��Ӧ�����ȷ�Ӧ���Ƿ��ȷ�Ӧ��
��� | ���Թ������Ӧ������ | U�ι����īˮҺ�� |
�� | ��������ˮ | ����Ҹ� |
�� | ���������������Ȼ�茶���(��ֽ���) | �� |
�� | ��Ƭ���ռ���Һ | ����Ҹ� |
�� | ͭ��Ũ���� | ����Ҹ� |
��������ʵ��ش�������⣺
(1)����Ƭ��ϡ����ķ�Ӧ��________(��������������������)��Ӧ��
(2)�������У�СľƬ�����ԭ����_________���ɴ˵ó��Ľ�����________��
(3)�ɷ�����������ó����ۣ��٢ۢ������ʷ����ķ�Ӧ����________(��������������������)��Ӧ��
(4)������ʵ��ڵ�U�ι��е�����Ϊ___________��˵����Ӧ���������С�����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���ӦN2��g��+3H2(g)![]() 2NH3(g)������Ϊ�ﵽƽ��״̬�����ݵ���
2NH3(g)������Ϊ�ﵽƽ��״̬�����ݵ���
A. N2��H2��NH3�������������ٸı�
B. c(N2)��c(H2)��c(NH3)��1��3��2
C. �Ͽ�1 mol H-H��ͬʱ�γ�1 mol H-H
D. ��λʱ����ÿ����1 mol N2��ͬʱ����3 molH2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ�о�С��̽����������Ի�ѧ��ӦmA(g)+nB(g)![]() pC(g)�����ʺ�ƽ���Ӱ����ͼ�����£������ж���ȷ������ ��
pC(g)�����ʺ�ƽ���Ӱ����ͼ�����£������ж���ȷ������ ��

A. ��ͼa��֪��T1>T2���÷�Ӧ���淴ӦΪ���ȷ�Ӧ
B. ��ͼb��֪���÷�Ӧm+n<p
C. ͼc�Ǿ������������ʺ�ʱ���ͼ���ɴ�˵���÷�Ӧ����
D. ͼd�У���m+n=p��������aһ��������ѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����±���������ϵ��ͼ��ʾ����˵����ȷ����

A. ��֪HF��������ˮ���ȣ���HF����H1<0
B. ��ͬ�����£�HCl����H2��HBr��С
C. ��ͬ�����£�HCl����H3+��H4��HI�Ĵ�
D. һ�������£���̬ԭ������1molH-X���ų�akJ�����������������H2=+akJ/mol
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com