
【题目】按要求填空:
(1) 除去KNO3中混有的SO42-应选择的除杂试剂为__________;
(2) 向沸腾的蒸馏水中滴加饱和FeCl3溶液可制取Fe(OH)3胶体,用化学方程式表示该方法的原理:_______;
(3) 在水溶液中,KHSO4的电离方程式为:______________________________;
(4) 盐酸与氢氧化钠溶液反应的离子方程式为:__________________________;
(5) CO2与足量澄清石灰水反应的离子方程式:__________________________;
(6) 硫酸铜溶液与氢氧化钡溶液反应的离子方程式为:____________________ ;
(7)小苏打常作为食品制作过程中的膨松剂,其溶液与稀HNO3反应的离子方程式为:___;
【答案】Ba(NO3)2 FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl KHSO4=K++H++SO42- OH-+H+=H2O CO2+Ca2++2OH-=CaCO3↓+H2O Cu2++2OH-+SO42-+Ba2+=Cu(OH)2↓+BaSO4↓ HCO3-+H+=CO2
Fe(OH)3(胶体)+3HCl KHSO4=K++H++SO42- OH-+H+=H2O CO2+Ca2++2OH-=CaCO3↓+H2O Cu2++2OH-+SO42-+Ba2+=Cu(OH)2↓+BaSO4↓ HCO3-+H+=CO2![]() +H2O
+H2O
【解析】
(1)欲除去KNO3溶液中的SO42-,先加过量Ba(NO3)2,除去SO42-,除杂试剂为Ba(NO3)2;
(2)Fe(OH)3胶体制备,是向沸腾的蒸馏水中加入几滴饱和FeCl3溶液并继续加热至液体变成红褐色,制备Fe(OH)3胶体的化学方程式为:FeCl3+3H2O![]() Fe(OH)3(胶体)+3HCl;
Fe(OH)3(胶体)+3HCl;
(3)硫酸氢钾在水中完全电离出钾离子、氢离子、硫酸根离子,电离方程式为:KHSO4=K++H++SO42-;
(4)稀盐酸与氢氧化钠溶液反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O,氯化氢、氢氧化钠、氯化钠都是易溶物、强电解质,离子方程式中需要拆开,该反应的离子方程式为:OH-+H+=H2O;
(5)CO2与足量澄清石灰水反应,产生了CaCO3,离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O;
(6)硫酸铜溶液与氢氧化钡溶液反应生成硫酸钡和氢氧化铜沉淀正确的离子方程式为:Cu2++2OH-+SO42-+Ba2+=Cu(OH)2↓+BaSO4↓;
(7)小苏打(NaHCO3)与稀HNO3反应生成二氧化碳和水,离子方程式为:HCO3-+H+=CO2![]() +H2O。
+H2O。


科目:高中化学 来源: 题型:
【题目】向1 L水中通入560 L NH3 (已折算为标准状况的体积),从而形成密度为 0.858g·cm-3的氨水(溶质为NH3),求:
(1)560 L氨气的物质的最为________mol。
(2)氨水的质量分数为_____(保留三位有效数字)。
(3)氨水的物质的量浓度_______。(列出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在20 L的密闭容器中按物质的量之比为1∶2充入CO和H2,发生反应:CO(g)+2H2(g)![]() CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度及不同压强下的变化如图所示,p2和195 ℃时n(H2)随时间的变化结果如表所示。下列说法正确的是( )
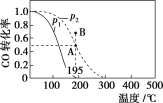
p2及195 ℃ 时n(H2)随时间变化
t/min | 0 | 1 | 3 | 5 |
n(H2)/mol | 8 | 5 | 4 | 4 |
A. p1>p2,ΔH<0
B. 在p2及195 ℃ 时,反应前3 min的平均速率v(CH3OH)=0.8 mol·L-1·min-1
C. 在p2及195 ℃ 时,该反应的平衡常数为25
D. 在B 点时,v正>v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用63%的浓硝酸(其密度为1.4g/mL)配制240mL0.50mol/L稀硝酸,若实验仪器有:A 10mL量筒 B 50mL量筒 C 托盘天平 D 玻璃棒 E 100mL容量瓶 F 250mL容量瓶 G 500mL容量瓶 H 胶头滴管 I 200mL烧杯。
(1)此浓硝酸的物质的量浓度为____________mol/L
(2)应量取63%的浓硝酸_____________mL,应选用___________。(填仪器的字母编号)
(3)实验时还需选用的仪器有______________(填仪器的字母编号)
(4)配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是______(填序号)。 |
A.可以按此建议改进,便于使用容量瓶 |
B.不能按此建议改进,因为会降低容量瓶的精确度 |
C.不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕获二氧化碳生成甲酸的过程如图所示。下列说法正确的是(NA为阿伏加德罗常数的值)
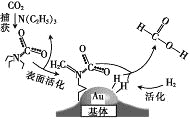
A. 标准状况下,22.4L CO2中所含的电子数目为16NA
B. 10.1g N(C2H5)3中所含的非极性共价键数目为0.3NA
C. 2mol Au与2mol H2中所含的分子数目均为2NA
D. 100g 46%的甲酸水溶液中所含的氧原子数目为5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用容量瓶配制一定物质的量浓度的NaCl溶液的实验中,会使所配溶液浓度偏高的是
A. 称量NaCl固体时砝码上有杂质
B. 没有洗涤溶解NaCl固体的烧杯和玻璃棒
C. 定容时加水加多了,用滴管吸出溶液至刻度线
D. 定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以菱锰矿(主要成分MnCO3,还含有FeCO3、CaCO3、SiO2、Al2O3、Fe2O3、MgCO3等杂质)为原料制备二氧化锰的工艺流程如下:
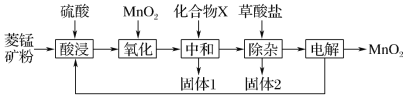
已知草酸钙、草酸镁不溶于水。
(1)写出“氧化”时发生反应的离子方程式:__________________________________________。
(2)“中和”的目的是将铁、铝元素转化为沉淀除去,化合物X可用______________________(写一种物质的化学式)。
(3)该工艺流程中固体1和固体2均需用水洗涤,目的是______________________。
(4)“除杂”时,除去的金属离子有______________________________________。
(5) 该流程中可以循环使用的物质有________。
(6)电解过程中MnO2 在______(填“阴”或“阳”)极生成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2+K2SO4+2CO2+2H2O,
(1)双线桥表示氧化还原,线桥上标明得失电子、发生的反应。_______
(2)若1mo KClO3参加反应时有_______mol电子转移。
(3)若生成标准状况下的CO2的体积是44.8L,则参加反应的还原剂的物质的量是多少mol?(要求有规范的过程)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应: 3A(g) ![]() B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是( )
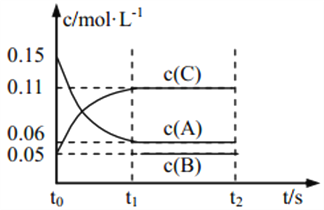
A. 若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.004 mol·L-1·s-1
B. t1时该反应达到平衡, A 的转化率为 60%
C. 该容器的容积为2 L,B的起始的物质的量为 0.02 mol
D. t0~t1 阶段, 此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为 3A(g)![]() B(g)+2C(g) ΔH=-50a kJ·mol-1
B(g)+2C(g) ΔH=-50a kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com