
【题目】以下性质的比较中,错误的是
A.热稳定性:H2S>PH3B.密度: 1-氯己烷>1-氯戊烷
C.酸性H2CO3>H2SiO3D.原子半径:Na>Cl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.某工厂的工业废水中含有大量的FeSO4和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:

(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿(主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有________(填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CH3OH(g)CH3OCH3(g)+H2O(g)△H=﹣25kJ/mol,某温度下的平衡常数为400.此温度下,在1L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
c/(molL﹣1) | 0.8 | 1.24 | 1.24 |
下列说法正确的是( )
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6mol/L
③平衡吋,反应混合物的总能量减少20kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08mol/L.
A.①②④⑤
B.②⑥
C.②③④⑥
D.②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香草醛是食品添加剂的增香原料,可由丁香酚经以下反应合成香草醛. 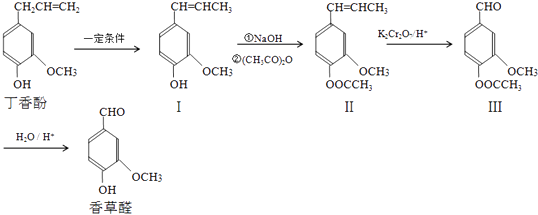
(1)写出香草醛分子中含氧官能团的名称 (任意写两种).
(2)下列有关丁香酚和香草醛的说法正确的是 .
A.丁香酚既能发生加成反应又能发生取代反应
B.香草醛中的﹣OH能被酸性K2Cr2O7氧化
C.丁香酚和化合物Ⅰ互为同分异构体
D.1mol香草醛最多能与3mol氢气发生加成反应
(3)写出化合物Ⅲ﹣→香草醛的化学方程式 .
(4)乙基香草醛(其结构见图a)也是食品添加剂的增香原料,它的一种同分异构体A属于酯类.A在酸性条件下水解,其中一种产物的结构见图b.A的结构简式是 .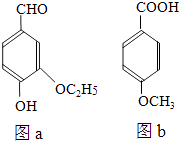
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知溶液中可发生反应:2FeBr2+Br2=2FeBr3,现向100mL的FeBr2溶液中通入3.36LCl2(标准状况),充分反应后测得溶液中Cl-和Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
A. 2molL-1 B. 1molL-1 C. 0.4molL-1 D. 0.2molL-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡元素有强还原性,+4价铅元素的化合物有强氧化性,例如:Sn2+还原性比Fe2+还原性强,PbO2的氧化性比Cl2的氧化性强,根据以上的叙述,回答有关的问题:
(1)写出下列反应的化学方程式:
①氯气与锡共热______________; ②氯气与铅共热______________;
③PbO2与浓盐酸共热_________________。
(2)能说明Sn2+还原性比Fe2+还原性强的离子方程式为________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 由一种元素组成的物质一定是单质
B. 由两种元素组成的物质一定是化合物
C. 化合物和碱性化合物属于包含关系
D. 氧化物和酸、碱、盐属于包含关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HAH++A﹣ , 回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向(填“正”、“逆”)反应方向移动,理由是 .
(2)若向溶液中加入适量NaCl溶液,以上平衡将向(填“正”、“逆”)反应方向移动,溶液中c(A﹣)将(填“增大”、“减小”或“不变”),溶液中c(OH﹣)将(填“增大”、“减小”或“不变”).
(3)已知室温时,0.1molL﹣1的某一元酸HA在水中有 0.1% 发生电离,回答下列各问题:
①该溶液的pH= .
②HA的电离平衡常数K= .
③升高温度时,K将(填“增大”、“减小”或“不变”),pH将(填“增大”、“减小”或“不变”).
④由HA电离出的c(H+)约为水电离出的c(H+)的倍.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com