
【题目】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力如图所示。回答下列问题:

(1)“O”点时液体不能导电,说明醋酸中________(填“含有”或“不含”)离子键。
(2)a、b、c三点醋酸电离程度由大到小的顺序为____________,a、b、c三点对应的溶液中c(H+)最大的是____。
(3)将等体积的a、b、c三点所对应的溶液用1 mol·L-1的NaOH溶液中和,消耗NaOH溶液体积由大到小的顺序____________。
(4)要使c点溶液中c(CH3COO-)增大而c(H+)减小,可采取的两种措施是加入____________。
(5)若实验测得c点处溶液中c(CH3COOH)=0.1 mol·L-1,c(CH3COO-)=0.001 mol·L-1,则该条件下CH3COOH的电离常数Ka=___________。
【答案】不含 c>b>a b a>b>c Zn(s)、NaOH(s)或醋酸钠 1.0×10-5
【解析】
冰醋酸是无水醋酸,加水稀释形成醋酸溶液,存在电离平衡CH3COOH![]() H++CH3COO-
H++CH3COO-
(1)“O”点时液体不能导电,说明“O”点时不存在自由移动的阴阳离子,冰醋酸中不含离子键,即CH3COOH是共价化合物,不含离子键;
(2)弱电解质溶液的浓度越小,弱电解质的电离度越大,a、b、c三点加水体积逐渐增大,所以醋酸电离程度逐渐增大即c>b>a ,由图知b点导电能力最大,则对应的溶液中c(H+)最大的是b点;
(3)等体积的酸,酸的浓度排序是a>b>c,等体积时酸的浓度越大,消耗NaOH溶液的体积越大,故消耗NaOH溶液体积由大到小的顺序a>b>c;
(4)由电离平衡CH3COOH![]() H++CH3COO-可知,要使c点溶液中c(CH3COO-)增大而c(H+)减小,可采取的措施是加入Zn(s)、Mg等金属、NaOH(s)、醋酸钠(s)、碳酸钠(s)等。
H++CH3COO-可知,要使c点溶液中c(CH3COO-)增大而c(H+)减小,可采取的措施是加入Zn(s)、Mg等金属、NaOH(s)、醋酸钠(s)、碳酸钠(s)等。
(5)c(CH3COO-)=c(H+)=0.001 mol·L-1 ,则Ka=![]() ,代入数据可得Ka=
,代入数据可得Ka=![]() 。
。


科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式____________________________。
(2)碳的燃烧热为393.50 kJ·mol-1,写出表示C燃烧热的热化学方程式:______________。
(3)已知CO转化成CO2的能量关系如下图所示。写出该反应的热化学方程式:_______。

(4)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为Q kJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式________。
(5)已知下列热化学方程式:
①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol
③H2(g)+![]() O2(g)===H2O(l)ΔH3=-285.8 kJ/mol
O2(g)===H2O(l)ΔH3=-285.8 kJ/mol
写出由C(s)、H2(g)和O2(g)化合生成CH3COOH(l)的热化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂, 可由NO与Cl2在通常条件下反应得到。某学习小组在实验室用如图所示装置制备NOCl。
已知:亚硝酰氯(NOCl)的熔点为-64.5℃、沸点为-5.5℃, 气态呈黄色,液态时呈红褐色,易与水反应。
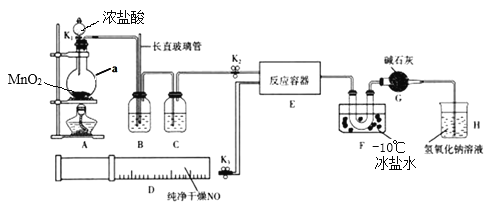
请回答下列问题:
(1)装置A中仪器a的名称是____________。
(2)实验开始时,应先打开K2,再打开____________(填K1”或K3”),通入一段时间气体,其目的是____________。
(3)实验时利用装置B除去某些杂质气体并通过观察B中的气泡来判断反应速率,装置B中的长直玻璃管还具有的作用是____________。
(4)装置C中应选用的试剂为____________(填试剂名称)。
(5)装置F的作用是____________。
(6)工业上可用间接电化学法除去NO,其原理如图所示,吸收塔中发生的反应为:NO+S2O42-+H 2O——N2+HSO3-(未配平)
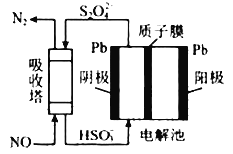
①吸收塔内发生反应的氧化剂与还原剂物质的量之比为________。
②阴极的电极反应式为_______。
(7)NOCl与H2O反应生成HNO2和HCl。请设计实验证明HNO2是弱酸:_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)陶瓷是一种新型无机非金属材料, 最高可稳定到2473K, 导热性好、热膨胀系数小,是良好的耐热冲击材料。制取原理为:Al2O3+3C+N2![]() 2A1N+3CO,回答下列问题:
2A1N+3CO,回答下列问题:
(1)氮化铝的晶体类型为________。在上述化学方程式中第二周期元素的第一电离能由小到大的顺序是______。
(2)基态氧原子电子占据最高能级的原子轨道的形状是________,未成对电子数为________。
(3)等电子体具有相似的结构。CO与N2互为等电子体,CO分子中σ键与π键数目之比为_______。
(4)Cu2+处于:[Cu(NH3)4]2+的中心,若将配离子[Cu(NH3)4]2+中的2个NH3换为CN-,则有2种结构,则Cu2+是否为sp3杂化________(填“是”或“否”)理由为_________。
(5)AlN晶体结构如图所示,1个Al原子周围距离最近的Al原子数为______个;若晶胞结构的高为a nm, 底边长为b nm,NA表示阿伏伽德罗常数的值,则其密度为_______g.cm-3(列出计算式)。
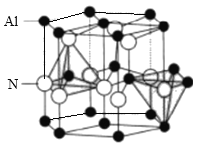
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数。X与Y位于不同周期,X与W的最高化合价之和为8,元素Z的单质是目前使用量最大的主族金属元素单质。下列说法中正确的是
A. 化合物YX4W溶于水后,得到的溶液呈碱性
B. 化合物YW3为共价化合物,电子式为![]()
C. Y、Z形成的一种化合物强度高,热膨胀系数小,是良好的耐热冲击材料
D. 原子半径大小:W>Z>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼对植物的生长和人体骨骼的健康有着十分重要的作用。请回答下列问題:
(1)区分晶体硼和无定硼形科学的方法为_________________________________。
(2)下列B原子基态的价层电子排布图中正确的是___________
A.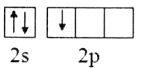 B.
B.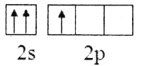
C.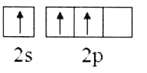 D.
D.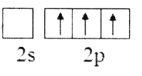
(3)NaBH4是重要的储氢载体,阴离子的立体构型为___________。
(4)三硫化四磷分子(结构如下图1所示)是___________分子(填极性”或非极性)。
(5)图2表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为___________。
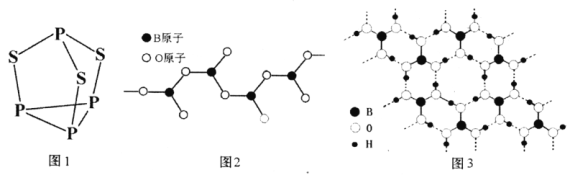
(6)硼酸晶体是片层结构,其中一层的结构如图3所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是_________________________________。
(7)立方氮化硼(BN)是新型高强度耐磨材料,可作为金属表面的保护层,其晶胞结构(如右图)与金刚石类似。已知该晶体密度为ag/cm3,则晶体中两个N原子间的最小距离为___________pm。(用含a的代数式表示,NA表示阿伏加德罗常数)
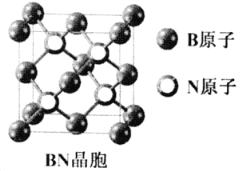
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。
已知:C10H18(l)![]() C10H12(l)+3H2(g) ΔH1
C10H12(l)+3H2(g) ΔH1
C10H12(l)![]() C10H8(l)+2H2(g) ΔH2
C10H8(l)+2H2(g) ΔH2
ΔH1>ΔH2>0;C10H18→C10H12的活化能为Ea1,C10H12→C10H8的活化能为Ea2,十氢萘的常压沸点为192℃;在192℃,液态十氢萘的脱氢反应的平衡转化率约为9%。
请回答:
(1)有利于提高上述反应平衡转化率的条件是___。
A.高温高压 B.低温低压
C.高温低压 D.低温高压
(2)研究表明,将适量的十氢萘置于恒容密闭反应器中,升高温度带来高压,该条件下也可显著释氢,理由是___。
(3)温度335℃,在恒容密闭反应器中进行高压液态十氢萘(1.00mol)催化脱氢实验(两步反应都使用了催化剂),测得C10H12和C10H8的产率x1和x2(以物质的量分数计)随时间的变化关系,如图1所示。
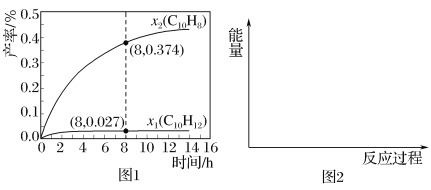
①在8h时,反应体系内氢气的量为___mol(忽略其他副反应)。
②x1显著低于x2的原因是___。
③在图2中绘制“C10H18→C10H12→C10H8”的“能量—反应过程”示意图___。
Ⅱ.(1)科学家发现,以H2O和N2为原料,熔融NaOH—KOH为电解质,纳米Fe2O3作催化剂,在250℃和常压下可实现电化学合成氨。阴极区发生的变化可视为按两步进行,请补充完整。
电极反应式:___和2Fe+3H2O+N2=Fe2O3+2NH3。
(2)常温下饱和亚硫酸溶液的物质的量浓度为1.25mol·L-1,电离常数Ka1=1.54×10-2,Ka2=1.02×10-7。向10mL饱和H2SO3溶液中滴加相同物质的量浓度的NaOH溶液VmL。当V=amL时,溶液中离子浓度有如下关系:c(Na+)=2c(SO32-)+c(HSO3-);当V=bmL时,溶液中离子浓度有如下关系:c(Na+)=c(SO32-)+c(HSO32-)+c(H2SO3);则a___(填“大于”“小于”或“等于”)b。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com