
【题目】将4molSO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2+O22SO3 测得平衡时SO3的浓度为0.5mol/L,求:
(1)平衡时各物质的浓度;
(2)平衡时SO2的转化率;
(3)该条件下的平衡常数K.
【答案】
(1)解:测得平衡混合物总的物质的量为5mol,则平衡时各组成物质的量变化为:
2SO2 | + | O2 |
| 2SO3 | 物质的量减少△n |
1 | 1 | 2 | 1 | ||
2mol | 1mol | 2mol | (4mol+2mol)﹣5mol=1mol |
平衡时氧气的物质的量为2mol﹣1mol=1mol,平衡时氧气的浓度= ![]() =0.25mol/L,
=0.25mol/L,
平衡时二氧化硫的浓度为: ![]() =0.50mol/L,
=0.50mol/L,
平衡时三氧化硫的浓度为: ![]() =0.50mol/L,
=0.50mol/L,
答:平衡时氧气的浓度为0.25mol/L,二氧化硫的浓度为0.50mol/L,三氧化硫的浓度为0.50mol/L
(2)解:平衡时SO2的转化率= ![]() ×100%=50%,
×100%=50%,
答:平衡时二氧化硫的转化率为50%
(3)解:该温度下平衡常数为: ![]() =4L/mol,
=4L/mol,
答:该反应的平衡常数为4L/mol
【解析】根据差量法计算参加反应的SO2、O2的物质的量,计算生成三氧化硫的物质的量;(1)计算平衡时氧气的物质的量,根据c= ![]() 计算平衡时各物质的浓度;(2)二氧化硫的转化率=
计算平衡时各物质的浓度;(2)二氧化硫的转化率= ![]() ×100%;(3)根据平衡常数表达式及各组分的浓度计算出该反应的平衡常数.
×100%;(3)根据平衡常数表达式及各组分的浓度计算出该反应的平衡常数.
【考点精析】解答此题的关键在于理解化学平衡的计算的相关知识,掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


科目:高中化学 来源: 题型:
【题目】某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示.由图中所给数据进行分析: 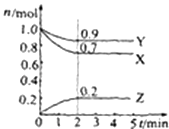
(1)该反应的化学方程式为;
(2)反应从开始至2分钟末,用Z表示该反应的平均反应速率;
(3)反应达平衡时X的转化率: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作不能增大化学反应速率的是
A.把食物储存在冰箱里
B.双氧水分解时加入二氧化锰
C.实验室制备氢气用粗锌代替纯锌
D.用2mol/L 50mL的硫酸代替2mol/L 50mL的盐酸与大小、形状、纯度相同的锌粒反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中发生如下反应:A(s)+2B(g)![]() 2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是
2C(g) ΔH<0,反应过程中B、C的物质的量随时间变化的关系如图1;反应达平衡后在t1、t2、t3、t4时分别都只改变了一种条件,逆反应速率随时间变化的关系如图2.下列有关说法正确的是

A. 反应开始2 min内,v(B)=0.1 mol/(L·min)
B. t1时改变的条件可能是升高温度
C. t3时改变的条件可能是加压,此时c(B)不变
D. t4时可能是使用了催化剂,此时c(B)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.强电解质溶液的导电能力一定比弱电解质溶液强
B.中和等体积、等物质的量浓度的盐酸和醋酸溶液,盐酸所需氢氧化钠等于醋酸
C.将氢氧化钠和氨水溶液各稀释一倍,两者的OH﹣浓度均减少到原来的 ![]()
D.如果盐酸的浓度是醋酸浓度的二倍,则盐酸的H+浓度也是醋酸的二倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学技术名词审定委员会已确定第116号元素Lv的名称为鉝.关于 ![]() Lv的叙述错误的是( )
Lv的叙述错误的是( )
A.原子序数116
B.中子数177
C.核外电子数116
D.相对原子质量293
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关氨气的实验较多,下面对这些实验的实验原理的分析中,不正确的是
A. 氨气极易溶解于水的性质可以解释氨气的喷泉实验
B. 氨气的还原性可以解释氨气与氯化氢的反应实验
C. NH3·H2O少部分电离产生OH-,可以解释氨水使酚酞试剂变为红色
D. NH3·H2O的热不稳定性可以解释实验室中用加热氨水的方法制取氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com