
【题目】“反向燃烧”可将二氧化碳变为燃料。回答下列问题:

(已知甲烷的标准燃烧热ΔH=-890 kJ·mol-1) 。
(1)科学家用氮化镓材料与铜组装如图所示的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。
①写出铜电极表面的电极反应式:_________________________;
②该总反应的热化学方程式为:___________________________,
(2)利用CO2与H2反应可制备CH4。
已知氢气的标准燃烧热ΔH=-286 kJ·mol-1 ;H2O(g) = H2O (l),ΔH=-44kJ·mol-1;
则二氧化碳与氢气反应生成甲烷和水蒸气的热化学方程式为_____________________;
该反应能自发的条件是__________(填高温或低温)。
【答案】CO2+8e-+8H+=CH4+2H2O CO2(g)+2H2O(l)=CH4(g)+2 O 2(g)△H=+890kJ·mol-1 CO2(g)+ 4H2(g)=CH4(g)+ 2H2O(g)△H=﹣166kJ·mol-1 低温
【解析】
(1)由电池装置图可知,在太阳光作用下形成原电池,电池工作时是将太阳能转化为电能的过程,铜的表面发生还原反应,CO2得电子与氢离子反应生成甲烷;原电池的总反应为甲烷燃烧的逆过程,能量变化为吸热,以此分析。
(2)写出方程式CO2(g)+ 4H2(g)=CH4(g)+ 2H2O(g),根据盖斯定律结合已知的热化学方程式求出反应热;根据△H-T△S<0,分析反应条件。
(1)①由电池装置图可知,Cu上二氧化碳得电子生成甲烷,则Cu电极上的电极反应为:CO2+8e-+8H+=CH4+2H2O;
因此,本题正确答案是:CO2+8e-+8H+=CH4+2H2O;
②该原电池负极反应为4H2O-4e-=8H++2O 2↑,则总反应为:CO2+2H2O=CH4+2O 2,该反应为甲烷燃烧的逆过程,能量变化为吸热,根据甲烷的标准燃烧热ΔH=-890 kJ·mol-1,可得该总反应的热化学方程式为:CO2(g)+2H2O(l)=CH4(g)+2 O 2(g)△H=+890kJ·mol-1,
因此,本题正确答案是:CO2(g)+2H2O(l)=CH4(g)+2 O 2(g)△H=+890kJ·mol-1。
(2)根据已知①CO2(g)+2H2O(l)=CH4(g)+2 O 2(g)△H=+890kJ·mol-1,
②H2(g)+![]() O2(g)=H2O(l) △H=-286kJ·mol-1,
O2(g)=H2O(l) △H=-286kJ·mol-1,
③ H2O(g) = H2O (l),ΔH=-44kJ·mol-1;
根据盖斯定律,①+②![]() 4-③
4-③![]() 2,得到CO2(g)+ 4H2(g)=CH4(g)+ 2H2O(g)
2,得到CO2(g)+ 4H2(g)=CH4(g)+ 2H2O(g)
△H=+890 kJ·mol-1+(-286 kJ·mol-1)![]() 4﹣(-44 kJ·mol-1)
4﹣(-44 kJ·mol-1)![]() 2=﹣166kJ·mol-1 ,
2=﹣166kJ·mol-1 ,
根据△H-T△S<0时,反应能够自发进行,该反应为放热反应,ΔH<0,气体分子数减小,ΔS<0,所以,低温有利于反应自发进行,
因此,本题正确答案是:CO2(g)+ 4H2(g)=CH4(g)+ 2H2O(g)△H=﹣166kJ·mol-1;低温。


科目:高中化学 来源: 题型:
【题目】在一定温度下,10 mL 0.40 mol·L-1H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
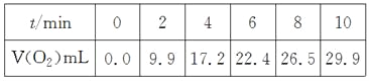
下列叙述不正确的是(溶液体积变化忽略不计)( )
A. 0~6 min的平衡反应速率:v(H2O2)≈3.3×10-2mol·L-1·min-1
B. 6~10 min的平衡反应速率:v(H2O2)<3.3×10-2mol·L-1·min-1
C. 反应到6 min时,c(H2O2)=0.30 mol·L-1
D. 反应到6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是

A. 以铅蓄电池为电源,则a极为Pb电极
B. 石墨Ⅱ电极附近的pH逐渐减小
C. 阳极反应为CH3CHO+H2O-2e-=CH3COOH+2H+
D. 每处理含8.8g乙醛的废水,转移电子的数目为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国是最早发现并使用青铜器的国家。司母戊鼎是迄今为止出土的世界上最大、最重的青铜礼器,享有“镇国之宝”的美誉(如图1)。

(1)Cu原子的外围电子排布式为_______。
(2)图2所示为第四周期某主族元素的第一至五电离能数据,该元素是_______,I3远大于I2的原因是_______。
(3)图3是某含铜配合物的晶体结构示意图。
①晶体中H2O和SO42-的中心原子的杂化类型为_______,试判断H2O和SO42-的键角大小关系并说明原因_______。
②图3中的氢键有(H2O)O—H···O(H2O)和_______。
③写出该配合物的化学式_______。
(4)一种铜的氯化物晶胞结构如下图所示。

该化合物的化学式为_______,已知P、Q、R的原子坐标分别(0,0,0)、(1,1,1)、 (![]() ,
,![]() ,
,![]() ),若Cu原子与最近的Cl原子的核间距为a pm,则该晶体的密度计算表达式为_______。
),若Cu原子与最近的Cl原子的核间距为a pm,则该晶体的密度计算表达式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氢气对废气进行脱碳处理可实现绿色环保、废物利用,对于减少雾霾也具有重要意义。
(1)汽车尾气的主要污染物为NO,用H2催化还原NO可以达到消除污染的目的。
已知:2NO(g) ![]() N2(g)+O2(g) ΔH=-180.5 kJ·mol-1
N2(g)+O2(g) ΔH=-180.5 kJ·mol-1
2H2O(l)===2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是______________。
(2)某研究小组模拟研究如下:向2 L恒容密闭容器中充入2 mol NO发生反应2NO(g) ![]() N2(g)+O2(g),在不同的温度下,反应过程中物质的量与时间的关系如图所示:
N2(g)+O2(g),在不同的温度下,反应过程中物质的量与时间的关系如图所示:

①T2下,在0~5 min内,v(O2)=______________mol·L-1·min-1;该温度下反应N2(g)+O2(g) ![]() 2NO(g)的平衡常数K=______________。
2NO(g)的平衡常数K=______________。
②该反应进行到M点放出的热量______________进行到W点放出的热量(填“>”、“<”或“=”)。
M点时再加入一定量NO,平衡后NO的转化率______________(填“变大”、“变小”或“不变”)。
③反应开始至达到平衡的过程中,容器中下列各项发生变化的是______________(填序号)。
a.混合气体的密度 b.逆反应速率
c.单位时间内,N2和NO的消耗量之比 d.气体的平均相对分子质量
(3)氢气作为一种理想燃料,但不利于贮存和运输。利用氢能需要选择合适的储氢材料,镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) ![]() LaNi5H6(s) ΔH<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是______________(填字母编号)。
LaNi5H6(s) ΔH<0,欲使LaNi5H6(s)释放出气态氢,根据平衡移动原理,可改变的条件是______________(填字母编号)。
A.增加LaNi5H6(s)的量 B.升高温度
C.使用催化剂 D.减小压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. ![]() 属于同分异构体
属于同分异构体
B. CH3COOCH2CH3与CHI3CH2COOCH3中均含有甲基、乙基和酯基,为同一种物质
C. C60与14C互为同素异形体
D. 乙酸与硬脂酸互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A. 苯能与溴发生取代反应,因此不能用苯萃取溴水中的溴
B. 甲烷和苯都属于烃,都不存在同分异构体
C. 乙烯、乙炔、苯燃烧时都伴有黑烟或浓烟
D. 丙烯和苯分子中的所有原子都在同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的数值。请回答下列问题:
(1)0.5mol SO2共含有约_______个原子,它与_______g SO3所含硫原子数相等。
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)___________。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是_____;
(4)标准状况下某种O2和N2的混合气体m g,含有b个分子,则n g该混合气体在相同状况下所占的体积应是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质M是一种酰胺类局麻药,某研究小组以A、E两种烃为有机原料,按以下路线合成M

已知:①![]() ;②
;②![]() ;
;
③![]() 。
。
请回答:
(1)化合物G的结构简式为______。
(2)下列说法不正确的是_________。
A.A→B为氧化反应
B.化合物G能与浓盐酸反应形成盐
C.化合物H与NaOH溶液反应最多消耗2molNaOH
D.局麻药M的分子式为C14H20N2O
(3)写出D+G→H的化学方程式:____________。
(4)写出满足下列条件的化合物F的所有同分异构体的结构简式________。
ⅰ.能与FeCl3溶液发生显色反应
ⅱ.能发生银镜反应
ⅲ.苯环上只有两个取代基且苯环上只有2种不同环境的氢原子
(5)该小组成员还提出另一种合成M的方案:化合物C与二乙胺[HN(CH2CH3)2]反应制取化合物X,X与G经一步反应即可制得药物M。请设计以烃A为原料制备化合物X的合成路线___________________________(用流程图表示,无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com