
����Ŀ���������Ƚ������ʼ��仯���������������������Ź㷺��Ӧ�á�
��1������ұ���봦�����漰������ԭ��Ӧ������������ұ����Ӧ��������ʱ���õ�ⷨ����_________��
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
��2��ij�о���ѧϰС���������ͼ��ʾװ��̽�������ĸ�ʴ�������

Ϊ��ֹ����Fe����ʴ�����Բ�������_______����װ����ţ�װ��ԭ�����з�����װ�������ܷ�Ӧ�����ӷ���ʽΪ______________________________________________��
��3�����ü״���CH3OH�����������ȼ�ϵ�أ��������ҺΪ���ԣ���ع���ʱ������ӦʽΪ_____________��
��4������Ҳ����Ϊȼ�ϵ�ص�ȼ��Դ�Ƴɸ�Ч������Ⱦ��ȼ�ϵ��ϵͳ���ܷ�ӦʽΪ��![]() ��δ��ƽ����д���˼���ȼ�ϵ�صĸ�����Ӧʽ��_______��
��δ��ƽ����д���˼���ȼ�ϵ�صĸ�����Ӧʽ��_______��
��5��������أ�K2FeO4����һ��ǿ������������Ϊˮ��������������ز��ϡ���MnO2-Zn������ƣ�K2FeO4-ZnҲ������ɼ��Ե�أ�K2FeO4�ڵ������Ϊ�������ϣ���缫��ӦʽΪ_________________________��
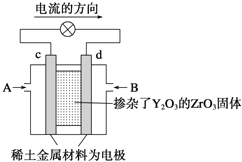
��6����ѧ�������һ��ʹ�ù������ʵ�ȼ�ϵ�أ���Ч�ʸ�����Ⱦ�������ں��캽�ա���ͼ��ʾװ���У���ϡ���������������Ե缫���������Ϸֱ�ͨ��CH4�Ϳ��������й��������Dz�����Y2O3��ZrO3���壬���ڸ������ܴ����������ɵ�O2-��O2+4e-��2O2-����d�缫�ϵĵ缫��ӦʽΪ_____________________��
���𰸡� bd �ڢ� 2Cl����2H2O![]() 2OH����H2����Cl2�� CH3OH��6e����8OH����CO32����6H2O 2NH3��6e����6OH����N2��6H2O FeO42����3e����4H2O��Fe(OH)3����5OH�� CH4��8e����4O2����CO2��2H2O
2OH����H2����Cl2�� CH3OH��6e����8OH����CO32����6H2O 2NH3��6e����6OH����N2��6H2O FeO42����3e����4H2O��Fe(OH)3����5OH�� CH4��8e����4O2����CO2��2H2O
����������������1�����ݻ����Խ���һ����õ�ⷨұ��������
��2��Ҫ��ֹ����������ʴ������Ҫ������ԭ��ص���������ص����������Ե缫��ⱥ��ʳ��ˮ�����������������������ƣ��ݴ���д�ܷ�Ӧʽ��
��3���״��ڸ�������ʧȥ���ӵ�������Ӧ����ϵ������Һ���������д�缫��Ӧʽ��
��4�������ڸ�������ʧȥ���ӵ�������Ӧ����ϵ������Һ���������д�缫��Ӧʽ��
��5��������صõ����ӱ���ԭΪ������������ϵ������Һ�����ʽ��
��6�����ݵ����ķ����ж�����������Ϸŵ�����д�缫��Ӧʽ��
��⣺��1��a.���ǽϻ��õĽ�������ҵ�����û�ԭ����ԭFe2O3ұ����������a����b.���ǻ��õĽ�������ҵ��ͨ��������ڵ�NaClұ�������ƣ�b��ȷ��c.ͭ�Dz����õĽ�������ҵ��ͨ��Cu2S�������ڸ����·�Ӧ�Ʊ���������ͭ��c����d.���ǻ��õĽ�������ҵ��ͨ��������ڵ�Al2O3ұ����������d��ȷ����ѡbd��
��2����װ����ԭ��أ�������Fe��Cu�����Ǹ���������ʧȥ���ӵ�������Ӧ��������ʴ����װ����ԭ��أ�������Fe��Zn����������������������װ���ǵ��أ������Դ�ĸ����������������������������Ϊ��ֹ����Fe����ʴ�����Բ��������ڢ�װ��ԭ�����з�����װ�â��е�ⱥ��ʳ��ˮ�����������ӷŵ磬���������ӷŵ磬���ܷ�Ӧ�����ӷ���ʽΪ2Cl����2H2O![]() 2OH����H2����Cl2����
2OH����H2����Cl2����
��3��ԭ����и�������ʧȥ���ӵ�������Ӧ����״��ڸ���ͨ�룬���ڵ������Һ�Լ��ԣ����ع���ʱ������ӦʽΪCH3OH��6e����8OH����CO32����6H2O��
��4�������ܷ�Ӧʽ���жϰ�������ʧȥ���ӵ�������Ӧ�����������ǵ��������ڵ������Һ�Լ��ԣ���˼���ȼ�ϵ�صĸ�����ӦʽΪ2NH3��6e����6OH����N2��6H2O��
��5��K2FeO4�ڵ������Ϊ�������ϣ��õ����������������������ڵ������Һ�Լ��ԣ�����缫��ӦʽΪFeO42����3e����4H2O��Fe(OH)3����5OH����
��6�����ݵ��������֪c�缫��������b�缫�Ǹ����������ڸ�������ʧȥ���ӵ�������Ӧ���������й��������Dz�����Y2O3��ZrO3���壬���ڸ������ܴ����������ɵ�O2-��O2+4e-��2O2-�������d�缫�ϵĵ缫��ӦʽΪCH4��8e����4O2����CO2��2H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
A. ��Ԫ�ؾ��ǿ��п���Ԫ��
B. ��Ԫ����Ҫ��ָCu��Fe��B��Mn��
C. ȱ����Ԫ�������Ҫ�ܵ�Ӱ��
D. ��Ԫ��Ҳ�������ͷ�����繲�е�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǹ㷺�����ڻ����еĽ���Ԫ�أ���ˮ������Ҫ�����ۺ����۸��Ļ�����Ϊ�����������۸������к���ͨ�������۸������Թ�ҵ��ˮ�Ĵ�������Ϊ��
![]()
��ش��������⣺
I����1���ڢٲ�����ƽ�⣺2CrO42��(��ɫ)+2H+![]() Cr2O72��(��ɫ)+H2O����д���÷�Ӧ��ƽ�ⳣ������ʽK= ______________���ڢٲ���Ӧ������״̬һ���ﵽƽ�����________��
Cr2O72��(��ɫ)+H2O����д���÷�Ӧ��ƽ�ⳣ������ʽK= ______________���ڢٲ���Ӧ������״̬һ���ﵽƽ�����________��
a��Cr2O72-��CrO42-��Ũ����ͬ b��2v (Cr2O72-) = v (CrO42-) c����Һ����ɫ���ֲ���
��2�������£���100mL��0.1mol/L��K2CrO4��Һ����1mol/L����10mL������ƽ�⣺
2CrO42��(��ɫ)+2H+![]() Cr2O72��(��ɫ)+H2O K=5��1014
Cr2O72��(��ɫ)+H2O K=5��1014
����������Һ�м���ŨKOH��Һ����Һ����ɫ�ɳ�ɫ����Ϊ��ɫ����Ӧ��ת��Cr2O72��(��ɫ) +2OH��![]() 2CrO42��(��ɫ) +H2O
2CrO42��(��ɫ) +H2O
��÷�Ӧ��ƽ�ⳣ��ΪK1����K1=_______________��
II��Ϊ��һ���о���ʼpH�Ͳ���Ũ�ȶԵڢڲ���Ӧ���ʵ�Ӱ�죬ijѧϰС����ƶԱ�ʵ�����±���
ʵ���� | ��ʼpH | ��ˮ��Ʒ���/mL | ������Һ���/mL | ����ˮ���/mL |
�� | 4 | 60 | 10 | 30 |
�� | 5 | x | 10 | 30 |
�� | 5 | y | 5 | z |
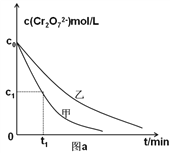
��3��ʵ����Ʊ���z=_______mL��
��4��ʵ�����0��t1ʱ��η�Ӧ����v(Cr3+)=________mol/(L��min) (�ú���ĸ�Ĵ���ʽ��ʾ)��
��5�������£��ڢ۲����ɵ�Cr(OH)3����Һ�д�������ƽ�⣺Cr(OH)3(s)![]() Cr3+(aq)+3OH��(aq)���ܶȻ�Ksp[Cr(OH)3]��1��10��32��Ҫʹc(Cr3+)������10��5mol/L����Һ��pHӦ����___________��
Cr3+(aq)+3OH��(aq)���ܶȻ�Ksp[Cr(OH)3]��1��10��32��Ҫʹc(Cr3+)������10��5mol/L����Һ��pHӦ����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ϩ����H2�ӳɺ�IJ����� ![]() �����ϩ���Ľṹʽ�����У�������
�����ϩ���Ľṹʽ�����У�������
A.1
B.2
C.3
D.4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������һ�����ォ��ˮ�е��л���(�����)�ͷ���NO�Ļ�ѧ��ֱ��ת��Ϊ���ܣ�����˵����һ����ȷ����
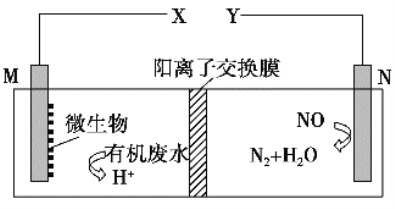
A. �����������ӽ���Ĥ���������ƶ�
B. ��X���������õ��������������Ľ�����
C. M�缫��Ӧʽ��(C6H10O5)n��7nH2O��24ne��===6nCO2����24nH��
D. ��M�缫���ォ��ˮ��16.2 g����ת����ʱ��N�缫����134.4 L N2������£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��һ������ȼ�ϵ�ع���ʱ��ʾ��ͼ���ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱ��M��N�����缫�������������٣���ش��������⣺
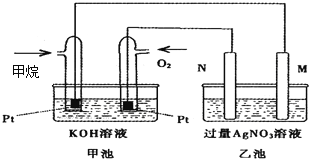
��1��M�缫�IJ�����__________����缫������_____________��
��2��N�ĵ缫��ӦʽΪ____________________________��ͨ�����ĵ缫��ӦʽΪ______________________________________________��
��3���ҳ��ܷ�Ӧ�Ļ�ѧ����ʽ��_______________________________________________��
��4���ڴ˹����У��ҳ���ijһ�缫����������4.32g���׳�����������������Ϊ_____mL����״���£�������ʱ�ҳ���Һ�����Ϊ400mL�����ҳ�����Һ��H+��Ũ��Ϊ__________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������̼����ȼ�ϵ����Li2CO3��K2CO3Ϊ����ʡ���CH4Ϊȼ��ʱ���õ�ع���ԭ����ͼ������˵����ȷ����
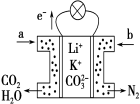
A��aΪO2��bΪCH4
B��CO 32-�������ƶ�
C���˵���ڳ���ʱҲ�ܹ���
D�������缫��ӦʽΪ2CO2+O2+4e����2CO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��H2��g����![]() O2��g����H2O��g�� ��H1
O2��g����H2O��g�� ��H1
![]() N2��g����O2��g����NO2��g�� ��H2
N2��g����O2��g����NO2��g�� ��H2
![]() N2��g����
N2��g����![]() H2��g����NH3��g�� ��H3
H2��g����NH3��g�� ��H3
��Ӧ2NH3��g����![]() O2��g����2NO2��g����3H2O��g������HΪ
O2��g����2NO2��g����3H2O��g������HΪ
A. 2��H1��2��H2��2��H3 B. ��H1����H2����H3
C. 3��H1��2��H2��2��H3 D. 3��H1��2��H2��2��H3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2 (g) +3H2 (g)![]() 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
����������ȷ����
A. ����������������ʱ��˵���÷�Ӧһ���ﵽƽ��״̬
B. ���������������ԭ���Ķ�������(��)��С����(��)����ƽ�������ƶ�
C. �����������N2��ת���ʣ��������̴ﵽƽ������ʱ�䣬�������Ч��
D. ���ܱ������з���1 mol N2��3 mol H2���з�Ӧ����÷�Ӧ�ų�������С��92.4 kJ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com