
����Ŀ��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2 (g) +3H2 (g)![]() 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
����������ȷ����
A. ����������������ʱ��˵���÷�Ӧһ���ﵽƽ��״̬
B. ���������������ԭ���Ķ�������(��)��С����(��)����ƽ�������ƶ�
C. �����������N2��ת���ʣ��������̴ﵽƽ������ʱ�䣬�������Ч��
D. ���ܱ������з���1 mol N2��3 mol H2���з�Ӧ����÷�Ӧ�ų�������С��92.4 kJ
���𰸡�D
��������A�������Ƿ�Ӧ�ﻹ��������������壬����˵�������Ƿ�ﵽƽ�⣬�����������������䡣
B�����������������ԭ���Ķ�������Ӧ�������Ũ�Ⱦ���С�������(��)����(��)����С��ƽ�������ƶ�
C�������Ȳ������N2��ת����,�������̴ﵽƽ������ʱ�䣬�������Ч��
D�����ڴ˷�Ӧʱ���淴Ӧ�����ܱ������з���1 mol N2��3 mol H2���з�Ӧ����÷�Ӧ�ų�������С��92.4 kJ



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ƚ������ʼ��仯���������������������Ź㷺��Ӧ�á�
��1������ұ���봦�����漰������ԭ��Ӧ������������ұ����Ӧ��������ʱ���õ�ⷨ����_________��
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
��2��ij�о���ѧϰС���������ͼ��ʾװ��̽�������ĸ�ʴ�������

Ϊ��ֹ����Fe����ʴ�����Բ�������_______����װ����ţ�װ��ԭ�����з�����װ�������ܷ�Ӧ�����ӷ���ʽΪ______________________________________________��
��3�����ü״���CH3OH�����������ȼ�ϵ�أ��������ҺΪ���ԣ���ع���ʱ������ӦʽΪ_____________��
��4������Ҳ����Ϊȼ�ϵ�ص�ȼ��Դ�Ƴɸ�Ч������Ⱦ��ȼ�ϵ��ϵͳ���ܷ�ӦʽΪ��![]() ��δ��ƽ����д���˼���ȼ�ϵ�صĸ�����Ӧʽ��_______��
��δ��ƽ����д���˼���ȼ�ϵ�صĸ�����Ӧʽ��_______��
��5��������أ�K2FeO4����һ��ǿ������������Ϊˮ��������������ز��ϡ���MnO2-Zn������ƣ�K2FeO4-ZnҲ������ɼ��Ե�أ�K2FeO4�ڵ������Ϊ�������ϣ���缫��ӦʽΪ_________________________��
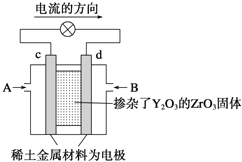
��6����ѧ�������һ��ʹ�ù������ʵ�ȼ�ϵ�أ���Ч�ʸ�����Ⱦ�������ں��캽�ա���ͼ��ʾװ���У���ϡ���������������Ե缫���������Ϸֱ�ͨ��CH4�Ϳ��������й��������Dz�����Y2O3��ZrO3���壬���ڸ������ܴ����������ɵ�O2-��O2+4e-��2O2-����d�缫�ϵĵ缫��ӦʽΪ_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���͵�صĹ���ԭ����ͼ��ʾ���ŵ�ʱ�ܷ�ӦΪ��Al+3NiO(OH)+NaOH+H2O=NaAlO2+3Ni(OH)2������˵���������

A. �ŵ�ʱ�������ĵ缫��ӦʽΪNiO(OH)+e-+H2O=Ni(OH)2+OH-
B. ���ʱ�������ĵ缫��ӦʽΪAlO2--3e-+2H2O=A1+4OH-
C. �ŵ�ʱ��Na+�������ƶ�
D. ���ʱ������·��ͨ��3NA����ʱ��������������3g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�ˮ�ĵ���ﵽƽ�⣺H2O![]() H+ + OH-������������ȷ����
H+ + OH-������������ȷ����
A. ��ˮ���ȣ�ƽ��������Ӧ�����ƶ���Kw����
B. ��ˮ�м����������ᣬƽ�����淴Ӧ�����ƶ���c��H+������
C. ��ˮ�м�������NaOH���壬ƽ�����淴Ӧ�����ƶ���c��OH-������
D. ��ˮ�м�������CH3COONa���壬ƽ��������Ӧ�����ƶ���c��OH-��= c��H+��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л�������A�����ϣ��������к�̼Ϊ70.59%������Ϊ 5.88%�����ຬ�������������з����ⶨ���л����������Է��������ͷ��ӽṹ�� ����һ��������������֪A������ͼ��ͼ1��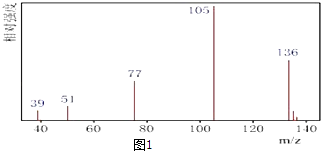
���������˴Ź����Dz��A�ĺ˴Ź���������4���壬�����֮��Ϊ1��2��2��3����ͼ2��
�����������ú�������Dz��A���ӵĺ�����ף���ͼ3��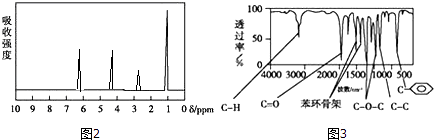
��1�������й����ֻ�ѧ������ͬ����ԭ�ӣ�
��2��A�ķ���ʽΪ ��
��3��������������һ���л��� ��
��4��A�ķ�����ֻ��һ������������������ţ��� a��A����Է������� b��A�ķ���ʽ c��A�ĺ˴Ź�������ͼ d��A���ӵĺ������ͼ
��5��A�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��4������������ͨ������·�ߺϳɣ�ijЩ��Ӧ�ķ�Ӧ��ͷ�Ӧ����δ�г����� 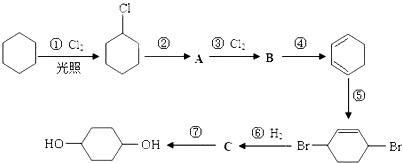
��1��д����Ӧ�ܡ��ߵĻ�ѧ����ʽ������ �� ��
��2���ڵķ�Ӧ������ �� �����߸���Ӧ�����ڼӳɷ�Ӧ�������Ӧ��ţ���
��3����Ӧ���п��ܲ���һ�����ĸ��������ܵĽṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��MnSO4�ڹ�ҵ������ҪӦ�á������̿���Ҫ�ɷ�ΪMnO2��ˮ������Fe2O3��FeO��Al2O3������PbO�����ʣ������Ʊ�MnSO4����������£�
I�������̿���ͨ��SO2���̡���������ǦԪ����������ʽ��������ý���Һ��pH��2��
II�������Һ�м�MnO2����ַ�Ӧ����ʯ���飬����ҺpH = 4.7��
III���ټ��������������������ú���ˡ�
IV����Һ����Ũ������ȴ�ᾧ�����MnSO4���塣
�����ϡ������������γ��������������pH
���� | Fe2+ | Fe3+ | Al3+ | Mn2+ | Pb2+ |
��ʼ����ʱ��pH | 7.6 | 2.7 | 3.8 | 8.3 | 8.0 |
��ȫ����ʱ��pH | 9.7 | 3.7 | 4.7 | 9.8 | 8.8 |
��1��I�������̿���ͨ��SO2����MnSO4���÷�Ӧ�Ļ�ѧ����ʽ��________��
��2��II�м���MnO2����ҪĿ����________������Һ pH=4.7�����ɵij�����Ҫ����________������CaSO4��
��3��III�м�������������������Ҫ��ȥ��������________��
��4���ö��Ե缫���MnSO4��Һ�������Ƶø���MnO2��
�����MnSO4��Һ�����ӷ���ʽ��________��
������MnO2�����ڴ������ȩ���й����ı仯����ͼ��ʾ������X��________���ܷ�Ӧ�Ļ�ѧ����ʽ��________��
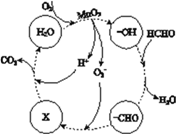
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Cu2SO3��CuSO3��2H2O��һ�����ɫ����(������M��ʾ)��ijѧϰС����ⶨ������Ʒ�Ĵ��ȣ�������Ϊԭ���Ʊ�M��
��֪����M������ˮ���Ҵ���100��ʱ�����ֽⷴӦ��
��M���ɵ�����SO2Ϊԭ���Ʊ�����Ӧԭ��Ϊ3Cu2++6H2O+3SO2![]() Cu2SO3��CuSO3��2H2O��+8H++SO42-��
Cu2SO3��CuSO3��2H2O��+8H++SO42-��
I���ⶨ������Ʒ�Ĵ��ȡ�
��1��ȡw g������Ʒ��������ˮ���Ƴ�250mL��Һ������ȡ25.00mL����ƿ�У�����ָʾ������c mol��L-1EDTA(��д��Na4Y)����Һ�ζ����յ�(�ζ�ԭ����Cu2++Y4-====CuY2-)�����������V mL EDTA����Һ����õ�����Ʒ�Ĵ���Ϊ____________��(�ú�c��V��w�Ĵ���ʽ��ʾ)������ζ���װҺǰû����EDTA����Һ��ϴ����õĽ����_________ (�ƫ�ߡ���ƫ�͡�����Ӱ�족)��
���Ʊ�M��ʵ��װ������ͼ��ʾ��
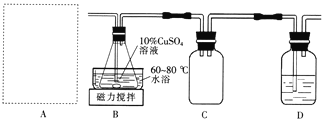
��2��ʵ������70���������������Ʒ�ĩ�ڳ������Ʊ�SO2����ͼA�������巢��װ�ÿɴ���ͼװ����ѡ������ʵ���________(����ĸ)��
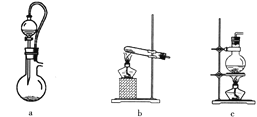
��3��װ��D�е��Լ���____________��װ��B��ˮԡ���ȵ��ŵ���____________________��
��4��ʵ�������ȴ�����º���ƿ�з����Ʒ�IJ���������__________��ˮϴ���Ҵ�ϴ�����¸���ò�ƷCu2SO3��CuSO3��2H2O�������Ʒ��ˮϴ��ȫ�IJ�����_______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼװ�ÿ��Բⶨͭпԭ��ع���ʱת�Ƶ��ӵ����ʵ�����������Ͳ�������㹻��пƬ�� ͭƬ�������ʣ����������ת��Ϊ��״��������˵����ȷ���� ( )

A. a �缫�ĵ缫������ͭ
B. �����ϡ���ỻΪ CuSO4 ��Һ�����ܴﵽʵ��Ŀ��
C. п��ϡ���ᷴӦʱ�ų���������ʵ��ⶨ������Ӱ��
D. ����Ͳ���ռ��� a L H2����������Һ��ͨ����![]() mol ����
mol ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com