
����Ŀ��ij�л�������A�����ϣ��������к�̼Ϊ70.59%������Ϊ 5.88%�����ຬ�������������з����ⶨ���л����������Է��������ͷ��ӽṹ�� ����һ��������������֪A������ͼ��ͼ1��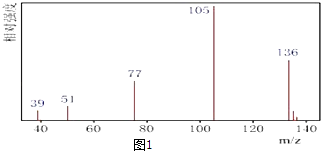
���������˴Ź����Dz��A�ĺ˴Ź���������4���壬�����֮��Ϊ1��2��2��3����ͼ2��
�����������ú�������Dz��A���ӵĺ�����ף���ͼ3��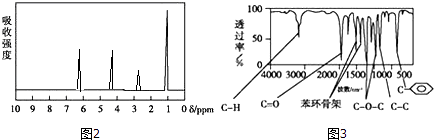
��1�������й����ֻ�ѧ������ͬ����ԭ�ӣ�
��2��A�ķ���ʽΪ ��
��3��������������һ���л��� ��
��4��A�ķ�����ֻ��һ������������������ţ��� a��A����Է������� b��A�ķ���ʽ c��A�ĺ˴Ź�������ͼ d��A���ӵĺ������ͼ
��5��A�Ľṹ��ʽΪ ��
���𰸡�
��1��4
��2��C8H8O2
��3������
��4��bc
��5��![]()
���������⣺��1����A�ĺ˴Ź�������ͼ֪��A��4���壬��A����4����ԭ�ӣ�
���Դ��ǣ�4����2����A������ͼ����֪A ����Է�������Ϊ136���������N��C��= ![]() =8��N��H��=
=8��N��H��= ![]() =8����N��O��=
=8����N��O��= ![]() =2�������ʽΪC8H8O2��
=2�������ʽΪC8H8O2��
���Դ��ǣ�C8H8O2����3���ɺ������ͼ֪��A���б�����ռ6��Cԭ�ӣ�������C=O��C��O��C��C��C��C��H������C=O��C��O��C�����Ϊ ![]() ��֪��4����ԭ�ӣ��������Ϊ1��2��2��3�������ک�CH3����ԭ����Ϊ3������ֻ����һ����CH3����A�Ľṹ��ʽΪ��
��֪��4����ԭ�ӣ��������Ϊ1��2��2��3�������ک�CH3����ԭ����Ϊ3������ֻ����һ����CH3����A�Ľṹ��ʽΪ�� ![]() ���������࣬
���������࣬
���Դ��ǣ����ࣻ��4�����������3���Ľ������ٽ��ͼA֪��4����ԭ�ӣ��������Ϊ1��2��2��3�������ک�CH3����ԭ����Ϊ3������ֻ����һ����CH3��
���Դ��ǣ�bc����5������������A�Ľṹ��ʽΪ ![]() ��
��
���Դ��ǣ� ![]() ��
��


 Сѧͬ�����������ܾ�ϵ�д�
Сѧͬ�����������ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ������һ�����ォ��ˮ�е��л���(�����)�ͷ���NO�Ļ�ѧ��ֱ��ת��Ϊ���ܣ�����˵����һ����ȷ����
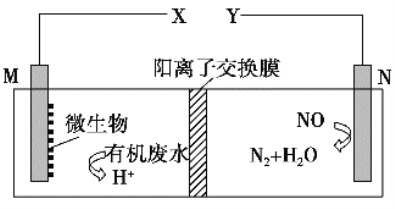
A. �����������ӽ���Ĥ���������ƶ�
B. ��X���������õ��������������Ľ�����
C. M�缫��Ӧʽ��(C6H10O5)n��7nH2O��24ne��===6nCO2����24nH��
D. ��M�缫���ォ��ˮ��16.2 g����ת����ʱ��N�缫����134.4 L N2������£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��M��R��Q�Ƕ���������Ԫ�أ�������Ϣ���±���ʾ��
X | Y | Z | M | R | Q | |
ԭ�Ӱ뾶 | 0.186 | 0.074 | 0.099 | 0.143 | ||
��Ҫ���ϼ� | ��4����4 | ��2 | ��1����7 | ��3 | ||
���� | ������������� | ���ǽ������ϵ����� | ��ɫ��Ӧ�ʻ�ɫ |
��1��X��M��ԭ�ӿɹ���18���ӵķ��ӣ��÷��ӵķ���ʽΪ______________��
��2��Z��Q��ȣ������Խ�ǿ����______________����Ԫ�ط��ű�ʾ����������ʵ��֤��һ���۵���______________������ĸ���ţ���
A.Q���۵��Z���۵�ߣ�Q��Ӳ�ȱ�Z��Ӳ�ȴ�
B.Z����ˮ��ӦѸ�٣���Q����ˮ��������Ӧ
C.Z������������Ӧˮ������ǿ���Q������������Ӧˮ�����������
��3����YԪ��ͬ����Ķ�����Ԫ��E����Ȼ���д��ڶ��ֺ��أ�����֮��Ĺ�ϵ��Ϊ_______________��
��4��д��Z2M2�ĵ���ʽ��___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 1molCl2����ˮ����Һ��Cl2��HClO��ClO-��Cl-������������Ϊ2NA
B. 6.4gCu������Ũ���ᷴӦ����NO2������ĿΪNA
C. 1mol����(C6H10O5)nˮ�������������Ƿ�����ĿΪNA
D. ��״���£�2molNa2O2��44.8LSO2��ȫ��Ӧ��ת�Ƶĵ�����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
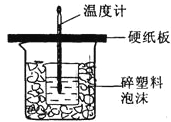
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ��_____________��
��2���ձ���������ֽ����������___________________��
��3�������60mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������__________�����ȡ�����ȡ����������к���__________�����ȡ�����ȡ�������������__________________________________________________��
��4������ͬŨ�Ⱥ�����İ�ˮ��NH3��H2O������NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��______________���ƫ����ƫС��������Ӱ�족����
��5�����ü�����ˮ��Ӧ�Ʊ���������ԭ�����۲����ʸߣ�����ʵ���ƹ��ֵ��
��֪����CH4(g)��H2O(g)��CO(g)��3H2(g) ��H����206.2kJ��mol��1
��CO(g)��H2O(g)��CO2(g)��H2(g) ��H����42.3kJ��mol��1
�����ˮ�������ɶ�����̼���������Ȼ�ѧ����ʽ_______________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ���ϳɰ���Ӧ���Ȼ�ѧ����ʽΪ��N2 (g) +3H2 (g)![]() 2NH3(g) ��H����92.4 kJ/mol
2NH3(g) ��H����92.4 kJ/mol
����������ȷ����
A. ����������������ʱ��˵���÷�Ӧһ���ﵽƽ��״̬
B. ���������������ԭ���Ķ�������(��)��С����(��)����ƽ�������ƶ�
C. �����������N2��ת���ʣ��������̴ﵽƽ������ʱ�䣬�������Ч��
D. ���ܱ������з���1 mol N2��3 mol H2���з�Ӧ����÷�Ӧ�ų�������С��92.4 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪: 25�桢101 kPa�£��� 2 Na(s) + 1/2 O2(g) = Na2O(s) ��H1 = - 414 kJ / mol
�� 2 Na(s) + O2(g) = Na2O2(s) ��H2 = - 511 kJ / mol
����˵����ȷ����
A. ������������������Ӹ����Ȳ����
B. ���������ɵ����ʵ����IJ��ת�Ƶ�������ͬ
C. ������Na������O2��Ӧ����Na2O�����¶���������Na2O�������ӿ�
D. 25�桢101 kPa�£�Na2O2(s) + 2 Na(s) = 2 Na2O(s) ��H = -317 kJ / mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4A��s��+3B��g���T2C��g��+D��g������2min��B��Ũ�ȼ���0.6mol/L���Դ˷�Ӧ���ʵı�ʾ��ȷ���ǣ�������
A.��A��ʾ�ķ�Ӧ������0.4 mol��Lmin����1
B.�ֱ���B,C,D��ʾ�ķ�Ӧ�������ֵ��3��2��1
C.��2minĩ�ķ�Ӧ���ʣ���B��ʾ��0.3 mol��Lmin����1
D.����2min����B��C��ʾ�ķ�Ӧ���ʵ�ֵ������С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�CO2�����öԴٽ���̼���Ĺ���������Ҫ�����塣
��1�� ��һ�������½�CO2 ��H2ת��Ϊ�״�������ˮ��������ط�Ӧ����
CO2(g) +H2(g)![]() CO(g)+H2O(g) ��H1=+41KJ/mol
CO(g)+H2O(g) ��H1=+41KJ/mol
CO(g) +2H2(g)![]() CH3OH(g) ��H2=-90KJ/mol
CH3OH(g) ��H2=-90KJ/mol
����CO2��H2ת��Ϊ�״�������ˮ�������Ȼ�ѧ����ʽΪ_____________________________________��
��2����һ���¶��£���2L�̶��ݻ����ܱ�������ͨ��2molCO2��3molH2��������ӦCO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) ��H3<0�����CO2(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
CH3OH(g) +H2O(g) ��H3<0�����CO2(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
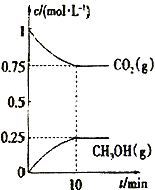
����˵���÷�Ӧ�Ѵ�ƽ��״̬����________________________��
A.��λʱ������3n molH-H�����ѣ�ͬʱ����2n mol O-H������
B.���������ܶȲ���ʱ��仯
C.��ϵ��n(CO2)/n(H2)=1��1���ұ��ֲ���
D. CO2����������ڻ�������б��ֲ���
�����д�ʩ��ʹn(CH3OH)/n(CO2)�������_______________��
A.�����¶� B.���º����£��ٳ���2molCO2��3molH2
C.ʹ�ø�Ч���� D.���º��ݳ���Heʹ��ϵѹǿ����
�ۼ�����¶��´˷�Ӧ��ƽ�ⳣ��K=_________������3λ��Ч���֣�����ʹK��ֵ��Ϊ1����Ӧ��ȡ�Ĵ�ʩ��___________________________��
A.����ѹǿ B.��ѹ����һ����H2 C. �����¶� D. �����¶�
��3����CO2��������Na2CO3��Һ����100mL 0.1mol/LNa2CO3��Һ��ȫ��0.44gCO2���壨��Һ����仯��������������Һ��c(HCO3-)+c(CO32-)+c(H2CO3)=________ mol/L
��4������Ϊ�ı�δ�������ʮ��Ƽ�֮һ��ȼ�ϵ����һ�����͵�����Ⱦ������������Ч�ʵ����������ͷ����豸�������Ʋ��ɵ�֮�Ƽ���������ҵ�͵�����ҵ��д���״�ȼ�ϵ�ؼ��Ե��������Ϊ���������ҺΪKOH ��Һ���ĸ����缫��Ӧ��___________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com