
【题目】用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
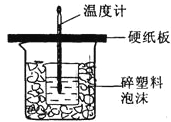
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________。
(2)烧杯间填满碎纸条的作用是___________________。
(3)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量__________(填“相等、不相等”)。所求中和热__________(填“相等、不相等”)。简述理由__________________________________________________。
(4)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会______________(填“偏大”、“偏小”、“无影响”)。
(5)利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值。
已知:①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-42.3kJ·mol-1
甲烷和水蒸气生成二氧化碳和氢气的热化学方程式_______________________________。
【答案】 环形玻璃搅拌棒 减少实验过程中的热量损失 不相等 相等 因为中和热是指酸跟碱发生中和反应生成1mol·H2O所放出的热量,与酸碱的用量无关 偏小 CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+163.9kJ·mol-1
【解析】分析:(1)根据量热计的构造来判断该装置的缺少仪器;
(2)根据中和热测定实验成败的关键是保温工作,据此解答;
(3)反应放出的热量和所用酸以及碱的量的多少有关,根据中和热的概念和实质来回答;
(4)根据一水合氨存在电离平衡分析;
(5)根据盖斯定律计算。
详解:(1)由量热计的构造可知该装置缺少的仪器是环形玻璃搅拌棒;
(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎泡沫塑料的作用是减少实验过程中的热量损失;
(3)反应放出的热量和所用酸以及碱的量的多少有关,如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关,因此所得的中和热相等;
(4)氨水中存在一水合氨的电离平衡,电离吸热,因此用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会偏小;
(5)已知:
①CH4(g)+H2O(g)=CO(g)+3H2(g) △H=+206.2kJ·mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-42.3kJ·mol-1
根据盖斯定律可知①+②即得到甲烷和水蒸气生成二氧化碳和氢气的热化学方程式为CH4(g)+2H2O(g)=CO2(g)+4H2(g) △H=+163.9kJ·mol-1。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铅镍蓄电池又称爱迪生电池,放电时的总反应为:![]() 下列有关该电池的说法不正确的是( )
下列有关该电池的说法不正确的是( )
A. 电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B. 电池放电时,负极反应为Fe+2OH--2e-═Fe(OH)2
C. 电池充电过程中,阴极附近溶液的pH降低
D. 电池充电时,阳极反应为2Ni(OH)2+2OH--2e-═Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
实验序号号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
① | 100 | 17.2 | 2.24 |
② | 200 | 8.00 | 4.48 |
③ | 400 | 0 | V |
下列说法正确的是( )
A.表中 V=7.84 L
B.原混合物粉末的质量为25.6 g
C.原混合物粉未中铁和铜的物质的量之比为2:3
D.实验3所得溶液中硝酸的物质的量浓度为0.875 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物体内构成血红蛋白、叶绿素、甲状腺激素、动物骨骼的重要元素依次是( )
A. I、Mg、Ca、Fe B. Fe、Mg、I、Ca
C. Fe、Ca、I、Mg D. Mg、Fe、I、Ca
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温泉有远古“圣水”之誉,富含各种对人体有益的微量元素及矿物质,水温高达56℃,水质淡黄清澈,享有“一盆玉汤”的美誉,对治疗皮肤病、色斑、关节炎及神经衰弱等有特殊的疗效.下列元素在生物体内含量较少,但对维持生物体正常生命活动必不可少的元素是( )
A. Fe Mn Zn Mg B. Zn Cu Mg Ca C. Zn Cu B Mn D. Mg Mn Cu Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A经李比希法测得其中含碳为70.59%、含氢为 5.88%,其余含有氧.现用下列方法测定该有机化合物的相对分子质量和分子结构. 方法一:用质谱法分析得知A的质谱图如图1: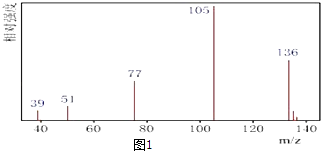
方法二:核磁共振仪测出A的核磁共振氢谱有4个峰,其面积之比为1:2:2:3.如图2.
方法三:利用红外光谱仪测得A分子的红外光谱,如图3.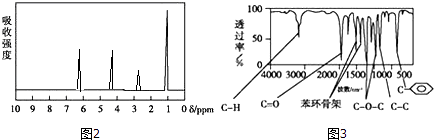
(1)分子中共有种化学环境不同的氢原子.
(2)A的分子式为 .
(3)该物质属于哪一类有机物 .
(4)A的分子中只含一个甲基的依据是(填序号). a.A的相对分子质量 b.A的分子式 c.A的核磁共振氢谱图 d.A分子的红外光谱图
(5)A的结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关酶和ATP的叙述,错误的是( )
A. ATP中的A代表腺嘌呤,T代表 3,P代表磷酸基团
B. ATP 脱去2个磷酸基团后是RNA的基本组成单位之一
C. 酶促反应速率往往受温度、pH和底物浓度等因素的影响
D. 人体内的酶不能通过食物获得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,通电5 min后,第③极增重2.16 g,同时在A池中收集到标准状况下的气体224 mL,设A池中原混合液的体积为200 mL,回答下列问题:

(1)电源F是__________极;
(2)A池的第②极上的电极反应式_________
(3)通电前A池中原混合溶液Cu2+的浓度________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有,OH﹣、CO32﹣ , AlO2﹣ , SiO32﹣ , SO42﹣ , K+ , Na+ , Fe3+ , Mg2+ , Al3+等离子,当向溶液中逐滴加入一定物质的量的盐酸时,生成沉淀物质的量与加入盐酸体积的关系如图.下列判断正确的是( ) 
A.原溶液中一定含有Na2SO4
B.原溶液中一定含有的阴离子是OH﹣ , CO32﹣ , SiO32﹣ , AlO2﹣
C.反应后形成的溶液溶质为NaCl
D.原溶液中含有CO32﹣与AlO2﹣的物质的量比为1:2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com