
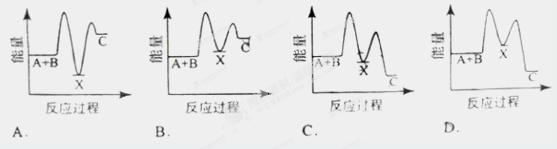
反应 A+B →C(△H <0)分两步进行 ① A+B→X (△H >0) ② X→C(△H <0)下列示意图中,能正确表示总反应过程中能量变化的是
科目:高中化学 来源: 题型:
某温度下在密闭容器中发生如下反应3 M(g)+ N(g) 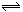 2G(g)
2G(g)
若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入3 molM和1molN的混合气体,达平衡时M的转化率为 ( )
A.20% B.40% C.60% D. 80%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O;5:1
②Fe2O3+2Al Al2O3+2Fe;1:2
Al2O3+2Fe;1:2
③4HC1(浓)+MnO2 MnC12+C12↑+2H2O;1:2
MnC12+C12↑+2H2O;1:2
④3NO2+H2O═2HNO3+NO;2:1.
|
| A. | ①②③ | B. | ②③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,不正确的是
A.反应热指的是反应过程中吸收或放出的热量 B.原电池的负极发生氧化反应
C.伴随能量变化的不一定是化学变化 D.电解池的阳极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
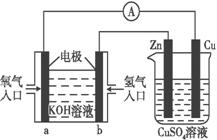
已知外电路中,电子由铜流向a极。有关如上图所示的
装置分析合理的一项是
A.该装置中Cu极为正极 B. 一段时间后锌片质量减少
C.b极的电极反应式:H2-2e- 2H+
2H+
D. 当铜片的质量变化为12.8 g时,a极上消耗的O2在标准状况下的体积为2.24 L
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图所示,某同学设计一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
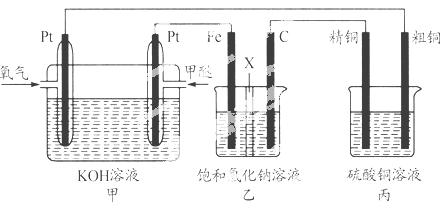
根据要求回答相关问题:
(1)通入氧气的电极为________(填“正极”或“负极”),写出负极的电极反应式_______________________________。
(2)铁电极为________(填“阳极”或“阴极”),石墨电极(C)的电极反应式为________________________________________。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________(填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为______ ___ __,反应一段时间,硫酸铜溶液浓度将________(填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的标况下的体积为____ ____;丙装置中阴极析出铜的质量为____ ___ _。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学实验事实及其解释不正确的是( )
A.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3
B.钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气
C.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应
D.钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列装置或操作能达到目的的是( )
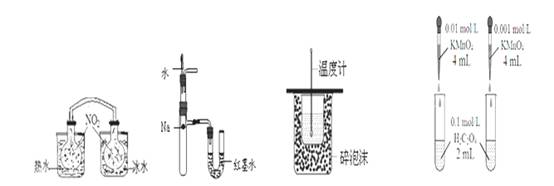 ① ② ③ ④
① ② ③ ④
A.装置①依据两容器内气体颜色变化,不能判断反应2NO2(g) N2O4(g)平衡移动的方向
N2O4(g)平衡移动的方向
B.装置②依据U管两边液面的高低判断Na和水反应的热效应
C.装置③测定中和热
D.装置④依据褪色快慢比较浓度对反应速率的影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com