
【题目】下列离子方程式错误的是( )
A. 实验室制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. 在NaCl溶液中滴入AgNO3溶液:Ag++Cl-===AgCl↓
C. Cl2溶于水:Cl2+H2O===2H++Cl-+ClO-
D. 用NaOH溶液吸收Cl2:Cl2+2OH-===Cl-+ClO-+H2O
科目:高中化学 来源: 题型:
【题目】液流电池是一种新型可充电的高性能蓄电池,其工作原理如下图。两边电解液存储罐盛放的电解液分别是含有V3+、V2+的混合液和VO2+、VO2+酸性混合液,且两极电解液分开,各自循环。下列说法不正确的是( )

A.充电时阴极的电极反应是V3++e-=V2+
B.放电时,VO2+作氧化剂,在正极被还原,V2+做还原剂,在负极被氧化
C.若离子交换膜为质子交换膜,充电时当有1mol e-发生转移时,左槽电解液的H+的物质的量增加了1mol
D.若离子交换膜为阴离子交换膜,放电时阴离子由左罐移向右罐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜晶体(CuSO4·xH2O)是一种用途广泛的试剂。某小组拟探究硫酸铜性质并测定其晶体中结晶水含量。
实验(一):探究硫酸铜的氧化性。
取适量硫酸铜溶液于试管,加入(NH4)2SO3溶液,产生沉淀M。过滤、洗涤、得M固体。为了探究M的组成,进行如下实验:
①取一定量M固体分成两份;
②在一份固体中加入稀硫酸,产生刺激性气味的气体X,将气体X通入溴水中,溴水褪色;溶液变成蓝色并有红色固体生成。
③在另一份固体中加入浓烧碱溶液,共热,产生的气体Y通入甲基橙溶液中,溶液变黄色。
(1)X的化学式是______________。
(2)经测定,M中阳离子、阴离子个数之比为2∶1。写出M与稀硫酸反应的化学方程式:____________。
实验(二):探究硫酸铜晶体的热稳定性。
他们取少量硫酸铜晶体进行实验,装置如图所示。
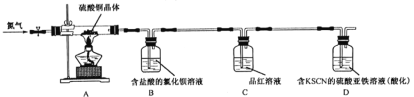
观察到的实验现象:A中蓝色晶体逐渐变成白色粉末,最后变成黑色粉末;B中产生白色沉淀;D中无色溶液变红色溶液。
(3)B中用盐酸酸化的目的是______________;C中现象是__________________________________。
(4)D中有单质参加反应的离子方程式:________________________________________________。
实验(三):测定硫酸铜晶体中结晶水含量。
取wg硫酸铜晶体(CuSO4·xH2O)配制成250mL溶液,取20.00mL所配制溶液用cmol·L-1EDTA(简化为Na4Y)溶液滴定至终点,消耗EDTA滴定液休积为VmL。(滴定反应:Cu2++Y4-=CuY2-)
(5)x=_____________________(用代数式表示)。
(6)下列情况会使测得x值偏大的是______________(填字母)。
a.样品失去部分结晶水 b.滴定管未用EDTA溶液润洗
c.开始读数时滴定管尖嘴有气泡(终点时尖嘴无气泡) d.滴定终点时俯视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语书写正确的是( )
A. 次氯酸的电离方程式:HClO===H++ClO-
B. 铝溶于烧碱溶液的离子方程式:Al+2OH-==AlO2-+H2↑
C. 电解精炼铜的阴极反应式:Cu-2e-==Cu2+
D. 已知中和热为57.3 kJ·mol-1,稀硫酸与氢氧化钠稀溶液反应的热化学方程式:H2SO4 (aq)+2NaOH(aq)==Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1,2-二氯乙烷在常温下为无色液体,沸点为83.5 ℃,密度为1.23 g·mL-1,难溶于水,易溶于醇、醚、丙酮等有机溶剂;乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如图所示的实验装置。请回答下列问题:

(1)为了检查整套装置的气密性,某同学将导气管末端插入盛有水的烧杯中,用双手捂着装置A中大试管,但该方法并不能准确说明装置的气密性是否良好。则正确检查整套装置气密性的方法是_______________。
(2)向装置A中大试管里先加入1,2-二氯乙烷和NaOH的乙醇溶液,再加入______,目的是______,并向装置C中试管里加入适量稀溴水。
(3)为了使反应在75 ℃左右进行,常用的方法是_______________________________。
(4)与装置A中大试管相连接的长玻璃管的作用是______,装置B的作用是______。
(5)能证明1,2-二氯乙烷已发生消去反应的实验现象是______,装置A、C中发生反应的化学方程式分别为_________________________;________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 已知:H2(g)+![]() O2(g)═H2O(l);△H=﹣285.8 kJmol﹣1 , 则H2的燃烧热为﹣285.8 kJmol﹣1
O2(g)═H2O(l);△H=﹣285.8 kJmol﹣1 , 则H2的燃烧热为﹣285.8 kJmol﹣1
B. 已知:S(g)+O2(g)═SO2(g)△H1=﹣Q1;S(s)+O2(g)═SO2(g)△H2=﹣Q2 , 则Q1<Q2
C. 已知:![]() H2SO4(浓)+NaOH(aq)═
H2SO4(浓)+NaOH(aq)═![]() Na2SO4(aq)+H2O(l)△H1;CH3COOH(aq)+NH3H2O(aq)═CH3COONH4(aq)+H2O(l)△H2 , 则有|△H1|<|△H2|
Na2SO4(aq)+H2O(l)△H1;CH3COOH(aq)+NH3H2O(aq)═CH3COONH4(aq)+H2O(l)△H2 , 则有|△H1|<|△H2|
D. 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=+489.0 kJmol﹣1
CO(g)+![]() O2(g)═CO2(g)△H=﹣283.0 kJmol﹣1
O2(g)═CO2(g)△H=﹣283.0 kJmol﹣1
C(石墨)+O2(g)═CO2(g)△H=﹣393.5 kJmol﹣1
则4Fe(s)+3O2(g)═2Fe2O3(s)△H=﹣1641.0 kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见如图,电池总反应可表示为2H2+O2===2H2O,下列有关说法正确的是( )

A. 电子通过外电路从b极流向a极
B. b极上的电极反应式为O2+2H2O+4e-===4OH-
C. 每转移0.1 mol电子,便消耗1.12 L的O2
D. H+由a极通过固体酸电解质传递到b极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
A. 25% B. 50% C. 75% D. 80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com