
【题目】下列说法正确的是( )
A. 已知:H2(g)+![]() O2(g)═H2O(l);△H=﹣285.8 kJmol﹣1 , 则H2的燃烧热为﹣285.8 kJmol﹣1
O2(g)═H2O(l);△H=﹣285.8 kJmol﹣1 , 则H2的燃烧热为﹣285.8 kJmol﹣1
B. 已知:S(g)+O2(g)═SO2(g)△H1=﹣Q1;S(s)+O2(g)═SO2(g)△H2=﹣Q2 , 则Q1<Q2
C. 已知:![]() H2SO4(浓)+NaOH(aq)═
H2SO4(浓)+NaOH(aq)═![]() Na2SO4(aq)+H2O(l)△H1;CH3COOH(aq)+NH3H2O(aq)═CH3COONH4(aq)+H2O(l)△H2 , 则有|△H1|<|△H2|
Na2SO4(aq)+H2O(l)△H1;CH3COOH(aq)+NH3H2O(aq)═CH3COONH4(aq)+H2O(l)△H2 , 则有|△H1|<|△H2|
D. 已知:Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g)△H=+489.0 kJmol﹣1
CO(g)+![]() O2(g)═CO2(g)△H=﹣283.0 kJmol﹣1
O2(g)═CO2(g)△H=﹣283.0 kJmol﹣1
C(石墨)+O2(g)═CO2(g)△H=﹣393.5 kJmol﹣1
则4Fe(s)+3O2(g)═2Fe2O3(s)△H=﹣1641.0 kJmol﹣1
【答案】D
【解析】A、燃烧热是1mol可燃物完全燃烧生成稳定的氧化物时放出的热量,其中H2O为液态,因此氢气的燃烧热是285.8kJ·mol-1,故A错误;B、S(g)=S(s)放出热量,S的燃烧是放热反应,即△H<0,因此有Q1>Q2,故B错误;C、浓硫酸与水放出热量,CH3COOH属于弱电解质,电离是吸热过程,即|△H1|>|△H2|,故C错误;D、①Fe2O3(s)+3C(石墨)═2Fe(s)+3CO(g),②CO(g)+ 1/2O2(g)═CO2(g),③C(石墨)+O2(g)═CO2(g),根据目标反应方程式,(③×3-②×3-①)×2,得出:4Fe(s)+3O2(g)═2Fe2O3(s)△H=﹣1641.0 kJ·mol-1,故D正确。


科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
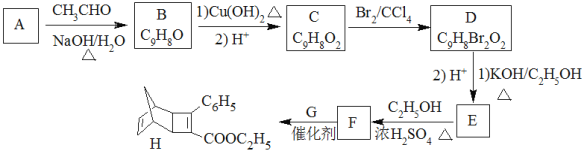
已知:
![]()
![]()
回答下列问题:
(1)A的化学名称为_____________________。
(2)由C生成D和E生成F的反应类型分别为__________、_________。
(3)E的结构简式为________________________。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为________________________。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶1∶1,写出1种符合要求的X的结构简式_____________________________。
(6)写出用环戊烷和2-丁炔为原料制备化合物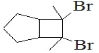 的合成路线_______(其他试剂任选)。
的合成路线_______(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究和验证氯气的性质,某研究性学习小组以MnO2和浓盐酸为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了研究。
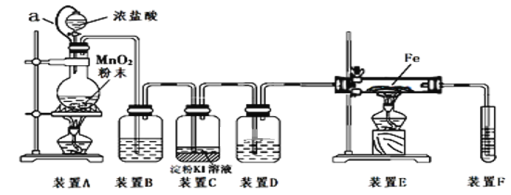
(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________。
(2)装置B中的试剂为_________,装置D作用是________。
(3)装置C中发生反应的离子方程式为_____________________________。
(4)反应开始后,装置E发生反应的化学方程式为____________________________。
(5)装置F中发生反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式错误的是( )
A. 实验室制Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
B. 在NaCl溶液中滴入AgNO3溶液:Ag++Cl-===AgCl↓
C. Cl2溶于水:Cl2+H2O===2H++Cl-+ClO-
D. 用NaOH溶液吸收Cl2:Cl2+2OH-===Cl-+ClO-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)分子式为C8H18,一氯代物只有一种的烷烃的名称为________________。
(2)金刚烷的结构如图所示,其分子式为___________;其一氯代物有_____种,二氯代物有_____种。
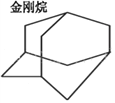
(3)异戊二烯(CH2=C(CH3)CH=CH2),顺式聚异戊二烯的结构简式为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下是碳和碳的化合物的转化关系:
![]()
其各步转化的基本反应类型从左到右依次是( )
A. 化合、分解、置换、复分解 B. 置换、化合、复分解、分解
C. 复分解、化合、分解、置换 D. 分解、置换、化合、复分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ. 无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝的试剂瓶久置于潮湿空气中,会自动爆炸并产生大量白雾.氯化铝常作为有机合成和石油工业的催化剂,并用于处理润滑油等.工业上由金属铝和氯气作用或由无水氯化氢气体与熔融金属铝作用制得.
某课外兴趣小组在实验室中,通过下图装置制取少量纯净的无水氯化铝.
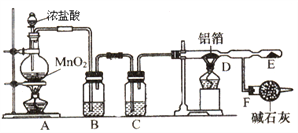
(1)A装置中发生反应的离子方程式为_____________________________;
(2)B、C装置中应盛放的试剂分别为______、______;
(3)从A装置导出的气体若不经过B、C装置而直接进入D管,对实验产生的不良后果是___.
(4)F装置所起的作用______.
Ⅱ. 有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32﹣、SO42﹣等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图1所示:

(1)在原溶液中一定存在的离子有______;
(2)第③实验中,若取原溶液100mL,滴加NaOH溶液的物质的量浓度为0.5molL﹣1 ,且生成沉淀的量与加入NaOH 的量如图2所示,则该溶液中所含阳离子的浓度为_____molL﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取Na2CO3和NaHCO3的混合粉末样品22.1g,将其加热到质量不再改变,冷却后称固体质量为15.9g。则原混合物中Na2CO3的质量为
A. 4.2g B. 5.3g C. 8.4 g D. 10.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是食品与硫酸和催化剂一同加热,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
①样品处理:准确称取一定量的固体样品奶粉,移入干燥的烧杯中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
②NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离态,游离氨经硼酸吸收。
③氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,由消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
请回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水_________。
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大_______。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯 B.定容时,俯视刻度线
C.定容时,仰视刻度线 D.移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100mL的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol·L-1盐酸滴定,其用去盐酸的体积为23.0mL,则该样品中N的含量为________。
(滴定过程中涉及到的反应方程式:(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3)
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com