
”¾ĢāÄæ”æČĖĄą»ī¶Æ²śÉśµÄCO2³¤ĘŚ»żĄŪ£¬ĶžŠ²µ½ÉśĢ¬»·¾³£¬Ęä¼õÅÅĪŹĢāŹÜµ½Č«ŹĄ½ē¹Ų×¢”£
(1)¹¤ŅµÉĻ³£ÓĆøßÅØ¶ČµÄK2CO3 ČÜŅŗĪüŹÕCO2£¬µĆČÜŅŗX£¬ŌŁĄūÓƵē½ā·ØŹ¹K2CO3 ČÜŅŗŌŁÉś£¬Ęä×°ÖĆŹ¾ŅāĶ¼ČēĻĀ£ŗ

¢ŁŌŚŃō¼«Ēų·¢ÉśµÄ·“Ó¦°üĄØ ŗĶH++HCO3-![]() H2O+CO2”ü”£
H2O+CO2ӟӣ
¢Ś¼ņŹöCO32-ŌŚŅõ¼«ĒųŌŁÉśµÄŌĄķ ”£
(2)ŌŁÉś×°ÖĆÖŠ²śÉśµÄCO2ŗĶH2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ӧɜ³É¼×“¼µČ²śĪļ£¬¹¤ŅµÉĻĄūÓĆøĆ·“Ó¦ŗĻ³É¼×“¼”£ŅŃÖŖ£ŗ25 ”ę£¬101 KPaĻĀ£ŗ
H2(g)+![]() O2(g)
O2(g)![]() H2O(g)¦¤H1=-242kJ”¤mol£1
H2O(g)¦¤H1=-242kJ”¤mol£1
CH3OH(g)+![]() O2(g)
O2(g)![]() CO2(g)+2H2O(g)¦¤H2=-676kJ”¤mol£1
CO2(g)+2H2O(g)¦¤H2=-676kJ”¤mol£1
¢ŁŠ“³öCO2ŗĶH2Éś³ÉĘųĢ¬¼×“¼µČ²śĪļµÄČČ»Æѧ·½³ĢŹ½ ”£
¢ŚĻĀĆę±ķŹ¾ŗĻ³É¼×“¼µÄ·“Ó¦µÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£¬ĘäÖŠÕżČ·µÄŹĒ (Ģī×ÖÄøŠņŗÅ)”£

A B C D
(3)Ī¢ÉśĪļČ¼ĮĻµē³ŲŹĒŅ»ÖÖĄūÓĆĪ¢ÉśĪļ½«»ÆѧÄÜÖ±½Ó×Ŗ»Æ³ÉµēÄܵÄ×°ÖĆ”£ŅŃÖŖijÖּד¼Ī¢ÉśĪļČ¼ĮĻµē³ŲÖŠ£¬µē½āÖŹČÜŅŗĪŖĖįŠŌ£¬Ź¾ŅāĶ¼ČēĻĀ£ŗ
 Ӣ
Ӣ
¢ŁøƵē³ŲĶāµēĀ·µē×ÓµÄĮ÷¶Æ·½ĻņĪŖ (ĢīŠ“”°“ÓAµ½B”±»ņ”°“ÓBµ½A”±)”£
¢ŚAµē¼«ø½½ü¼×“¼·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖ ”£
”¾“š°ø”æ
(1)¢Ł4OHØC£4e-=2H2O+O2”ü£»¢ŚHCO3ØC“ęŌŚµēĄėĘ½ŗā£ŗHCO3ØC![]() H++CO32-£¬Ņõ¼«H+·ÅµēÅØ¶Č¼õŠ”Ę½ŗāÓŅŅĘ”£(»ņŅõ¼«H+·ÅµēOH-ÅضČŌö“ó£¬OH-ÓėHCO3ØC·“Ӧɜ³ÉCO32-)
H++CO32-£¬Ņõ¼«H+·ÅµēÅØ¶Č¼õŠ”Ę½ŗāÓŅŅĘ”£(»ņŅõ¼«H+·ÅµēOH-ÅضČŌö“ó£¬OH-ÓėHCO3ØC·“Ӧɜ³ÉCO32-)
(2)¢ŁCO2(g)+3H2(g)=CH3OH(g)+H2O(g)”÷H=£50kJ”¤mol£1£»¢ŚA
(3)¢Ł“ÓAµ½B£»¢ŚCH3OH+H2O-6e-=6H++CO2”ü
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ(1)¢ŁŃō¼«ÉĻĒāŃõøłĄė×ӷŵēÉś³ÉŃõĘųŗĶĖ®£¬µē¼«·“Ó¦Ź½ĪŖ4OH--4e-ØT2H2O+O2”ü£¬¹Ź“š°øĪŖ£ŗ4OH--4e-ØT2H2O+O2”ü£»¢ŚHCO3-“ęŌŚµēĄėĘ½ŗā£ŗHCO3-H++CO32-£¬Ņõ¼«H+·ÅµēÅØ¶Č¼õŠ”Ę½ŗāÓŅŅĘ£¬CO32-ŌŁÉś£»Ņõ¼«H+·ÅµēOH-ÅضČŌö“ó£¬OH-ÓėHCO3-·“Ӧɜ³ÉCO32-£¬CO32-ŌŁÉś£¬¹Ź“š°øĪŖ£ŗHCO3-“ęŌŚµēĄėĘ½ŗā£ŗHCO3-![]() H++CO32-£¬Ņõ¼«H+·ÅµēÅØ¶Č¼õŠ”£¬Ę½ŗāÓŅŅĘ£¬CO32-ŌŁÉś£»Ņõ¼«H+·ÅµēOH-ÅضČŌö“ó£¬OH-ÓėHCO3-·“Ӧɜ³ÉCO32-£¬CO32-ŌŁÉś£»
H++CO32-£¬Ņõ¼«H+·ÅµēÅØ¶Č¼õŠ”£¬Ę½ŗāÓŅŅĘ£¬CO32-ŌŁÉś£»Ņõ¼«H+·ÅµēOH-ÅضČŌö“ó£¬OH-ÓėHCO3-·“Ӧɜ³ÉCO32-£¬CO32-ŌŁÉś£»
(2)¢ŁH2(g)+![]() O2(g)ØTH2O(g)”÷H1=-242kJ/mol¢Ł£¬CH3OH(g)+
O2(g)ØTH2O(g)”÷H1=-242kJ/mol¢Ł£¬CH3OH(g)+![]() O2(g)ØTCO2(g)+2H2O(g) ”÷H2=-676kJ/mol ¢Ś£¬½«·½³ĢŹ½3¢Ł-¢ŚµĆCO2(g)+3H2(g)ØTCH3OH(g)+H2O(g)”÷H =3”Į(-242kJ/mol)-(-676kJ/mol) =-50 kJ/mol£¬¹Ź“š°øĪŖ£ŗCO2(g)+3H2(g)ØTCH3OH(g)+H2O(g)”÷H=-50 kJ/mol£»¢ŚøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬·“Ó¦Īļ×ÜÄÜĮæ“óÓŚÉś³ÉĪļ×ÜÄÜĮ棬ĪļÖŹŌ½ĪČ¶Ø£¬ĘäÄÜĮæŌ½Š”£¬ĖłŅŌŅŗĢ¬ĪļÖŹµÄÄÜĮæŠ”ÓŚĘųĢ¬ĪļÖŹ£¬Ōņ·ūŗĻĢõ¼žµÄĶ¼ĻóŹĒA£¬¹ŹŃ”A£»
O2(g)ØTCO2(g)+2H2O(g) ”÷H2=-676kJ/mol ¢Ś£¬½«·½³ĢŹ½3¢Ł-¢ŚµĆCO2(g)+3H2(g)ØTCH3OH(g)+H2O(g)”÷H =3”Į(-242kJ/mol)-(-676kJ/mol) =-50 kJ/mol£¬¹Ź“š°øĪŖ£ŗCO2(g)+3H2(g)ØTCH3OH(g)+H2O(g)”÷H=-50 kJ/mol£»¢ŚøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬·“Ó¦Īļ×ÜÄÜĮæ“óÓŚÉś³ÉĪļ×ÜÄÜĮ棬ĪļÖŹŌ½ĪČ¶Ø£¬ĘäÄÜĮæŌ½Š”£¬ĖłŅŌŅŗĢ¬ĪļÖŹµÄÄÜĮæŠ”ÓŚĘųĢ¬ĪļÖŹ£¬Ōņ·ūŗĻĢõ¼žµÄĶ¼ĻóŹĒA£¬¹ŹŃ”A£»
(3)¢ŁøĆČ¼ĮĻµē³ŲÖŠ£¬¼×“¼Ź§µē×Ó·¢ÉśŃõ»Æ·“Ó¦£¬ĖłŅŌAŹĒøŗ¼«£¬BŹĒÕż¼«£¬µē×Ó“Óøŗ¼«AĮ÷ĻņÕż¼«B£¬¹Ź“š°øĪŖ£ŗ“ÓAµ½B£»¢ŚAµē¼«ÉĻ¼×“¼Ź§µē×ÓŗĶĖ®·“Ӧɜ³ÉĒāĄė×ÓŗĶ¶žŃõ»ÆĢ¼£¬µē¼«·“Ó¦Ź½ĪŖ£ŗCH3OH+H2O-6e-ØT6H++CO2”ü£¬¹Ź“š°øĪŖ£ŗCH3OH+H2O-6e-ØT6H++CO2”ü”£


 ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
ĆæČÕ10·ÖÖÓæŚĖćŠÄĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀĢ·ÆæÉÓĆ×÷³ż²Ż¼Į”¢¾»Ė®¼Į»ņæ¹Ę¶ŃŖŅ©µČ£®Ä³ŃŠ¾æŠ”×éĶ¬Ń§²ÉÓĆĮņĢśæó±ŗÉÕŗóµÄÉÕŌü£ØÖ÷ŅŖ³É·ŻĪŖFe2O3”¢Al2O3ŗĶSiO2£¬²»æ¼ĀĒĘäĖūŌÓÖŹ£©ÖʱøĀĢ·Æ£¬Éč¼ĘĮĖČēĻĀĮ÷³Ģ£®

Ēė»Ų“š£ŗ
£Ø1£©¢Ł”«¢ŪĖłÉę¼°µÄŹµŃé²Ł×÷·½·ØÖŠ£¬ÓƵ½¹żĀĖµÄŹĒ £ØĢīŠņŗÅ£©£®
£Ø2£©¢ŪÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ £®
£Ø3£©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ØĢī×ÖÄø£© £®
a£®¢ŁÖŠæÉŃ”ÓĆŃĪĖį£¬¢ŪÖŠÖ»ÄÜÓĆĮņĖį
b£®ČÜŅŗBÖŠŗ¬ÓŠOH©”¢SiO32©”¢AlO2©µČŅõĄė×Ó
c£®¢ÜÖŠ·¢ÉśĮĖŃõ»Æ»¹Ō·“Ó¦£¬¹ĢĢåC×ö»¹Ō¼Į
£Ø4£©ŌÉÕŌüÖŠFe2O3µÄÖŹĮæ·ÖŹżĪŖ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ2SO2(g)+O2(g)![]() 2SO3(g) ”÷H=£196 kJ/mol”£Ä³ĪĀ¶ČĻĀ£¬ĻņŅ»Ģå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.2molSO2ŗĶ0.1molO2£¬5minŗó“ļµ½Ę½ŗā£¬¹²·Å³öČČĮæ11.76kJ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
2SO3(g) ”÷H=£196 kJ/mol”£Ä³ĪĀ¶ČĻĀ£¬ĻņŅ»Ģå»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ³äČė0.2molSO2ŗĶ0.1molO2£¬5minŗó“ļµ½Ę½ŗā£¬¹²·Å³öČČĮæ11.76kJ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®5minÄŚÓĆO2±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ0.12mol/(L”¤min)
B£®¼ÓČė“߻ƼĮ£¬æÉŹ¹øĆ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬”÷H±äŠ”
C£®SO2µÄĘ½ŗāÅضČĪŖ0.12mol/L
D£®“ļµ½Ę½ŗāŹ±£¬ČōŌö“óČŻĘ÷µÄĢå»ż£¬ŌņøĆ·“Ó¦µÄ»Æѧ·“Ó¦ĖŁĀŹ¼õĀż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖĢåÄŚÓŠ20¶ąÖÖĪ¢ĮæŌŖĖŲ£¬ĖüĆĒµÄÖŹĮæ×ÜŗĶ²»µ½ĢåÖŲµÄĒ§Ķņ·ÖÖ®Ņ»£¬µ«ŹĒ¶ŌČĖµÄ½”æµČ“Ęš×ÅÖŲŅŖµÄ×÷ÓĆ£¬ĻĀĮŠø÷×éŌŖĖŲČ«²æŹĒĪ¢ĮæŌŖĖŲµÄŹĒ£Ø £©
A. Na K Cl S O B. B Mn Fe Zn Cu
C. N Mg Mo P Zn D. Mo Ca Cu Mg C
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ŲÓŚN2”¢N2O”¢N2O5µÄŠšŹö£¬ÕżČ·µÄŹĒ( )
A. Ćæøö·Ö×ÓÖŠ¶¼ŗ¬ÓŠµŖ·Ö×Ó B. Ćæøö·Ö×ÓÖŠµÄµŖŌ×ÓøöŹżĻąµČ
C. ĆæÖÖĪļÖŹÖŠµŖŌŖĖŲµÄÖŹĮæ·ÖŹżĻąĶ¬ D. ¶¼ŹōÓŚŃõ»ÆĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃéµÄ·“Ó¦ŌĄķÓĆĄė×Ó·½³ĢŹ½±ķŹ¾ÕżČ·µÄŹĒ( )
A£®ŹŅĪĀĻĀ£¬²āµÄĀČ»Æļ§ČÜŅŗpH<7£¬Ö¤Ć÷Ņ»Ė®ŗĻ°±µÄŹĒČõ¼ī£ŗNH4£«£«2H2O=NH3”¤H2O£«H3O£«
B£®ÓĆĒāŃõ»ÆÄĘČÜŅŗ³żČ„Ć¾·ŪÖŠµÄŌÓÖŹĀĮ£ŗ2Al£«2OH££«2H2O=2AlO2££«3H2”ü
C£®ÓĆĢ¼ĖįĒāÄĘČÜŅŗ¼ģŃéĖ®ŃīĖįÖŠµÄōČ»ł£ŗ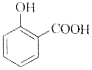 +2HCO3-”ś
+2HCO3-”ś +2H2O+2CO2”ü
+2H2O+2CO2ӟ
D£®ÓĆøßĆĢĖį¼Ų±ź×¼ČÜŅŗµĪ¶Ø²ŻĖį£ŗ2MnO4££«16H£«£«5C2O42£=2Mn2£«£«10CO2”ü£«8H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆĻĀĮŠŹµŃé×°ÖĆ½ųŠŠĻąÓ¦ŹµŃ飬ÄÜ“ļµ½ŹµŃéÄæµÄŹĒ£Ø £©

A£®ÓĆĶ¼£Øa£©ĖłŹ¾×°ÖĆ³żČ„Cl2ÖŠŗ¬ÓŠµÄÉŁĮæHCl
B£®ÓĆĶ¼£Øb£©ĖłŹ¾×°ÖĆÕōøÉNH4Cl±„ŗĶČÜŅŗÖʱøNH4Cl¾§Ģå
C£®ÓĆĶ¼£Øc£©ĖłŹ¾×°ÖĆÖĘȔɣĮæ“æ¾»µÄCO2ĘųĢå
D£®ÓĆĶ¼£Ød£©ĖłŹ¾×°ÖĆ·ÖĄėCCl4ŻĶČ”µāĖ®ŗóŅŃ·Ö²ćµÄÓŠ»ś²ćŗĶĖ®²ć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®NAøöCO2·Ö×ÓÕ¼ÓŠµÄĢå»żŅ»¶ØĪŖ22.4L
B£®±ź×¼×“æöĻĀ£¬22.4LĖÄĀČ»ÆĢ¼ŗ¬ÓŠµÄ·Ö×ÓŹżĪŖNA
C£®³£ĪĀ³£Ń¹ĻĀ,1.06g Na2CO3ŗ¬ÓŠµÄNa+ŹżĪŖ0.02 NA
D£®ĪļÖŹµÄĮæÅضČĪŖ0.5mol/LµÄMgCl2ČÜŅŗÖŠ£¬ŗ¬Cl-øöŹżĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£®ĻĀĮŠŠšŹöÕżČ·µÄŹĒ£Ø £©
A£®9g¼×»ł£Ø©CH3£©Ėłŗ¬ÓŠµÄµē×ÓŹżŹĒ10 NAøö
B£®22£®4LŅŅĶéÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżĪŖ7NAøö
C£®³£ĪĀĻĀ£¬14gŅŅĻ©ŗĶ±ūĻ©µÄ»ģŗĻĪļÖŠ×ÜŌ×ÓŹżĪŖ3NA
D£®4£®2g C3H6ÖŠŗ¬ÓŠµÄĢ¼Ģ¼Ė«¼üŹżŅ»¶ØĪŖ0£®1NA
²éæ““š°øŗĶ½āĪö>>
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com