
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A.室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B.用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C.用碳酸氢钠溶液检验水杨酸中的羧基: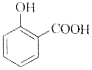 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D.用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验原理、方法和结论都正确的是
A.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体
B.取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+
C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚
D.已知I3-![]() I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,说明KI3在CCl4中的溶解度比在水中的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取镁的主要步骤如下:
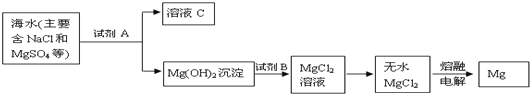
①上述从海水中提取镁的步骤中,试剂A可以选用 ,试剂B选用 .
②分离出Mg(OH)2后的溶液C中除NaCl外,还含有CaCl2、Na2SO4等杂质,为了获得NaCl溶液,在分离后的溶液中依次加入过量的BaCl2溶液、Na2CO3溶液,过滤,再向滤液中加入适量盐酸.写出加入过量BaCl2溶液发生反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)为了做到合理营养,我国营养学家将食物分为A、B、C、D、E五类,请回答下列问题:①营养学家将这五类形象地设计成图示的“ ”,并提倡居民每天均衡地吃这五类食物.为保证身体健康,建议在每日摄入的总能量中,早、中、晚餐的能量比例是 .
②正在生长发育的青少年,应多吃图中C、D类食物,原因是该类食物中含有丰富的 和钙质.
③你每天吃的主食是 类食物,膳食中如果不搭配该类食物会造成身体内缺乏 .
④B类食物所含的主要营养成分是 和无机盐.
(2)随着我国经济的发展,摩托车、小汽车进入家庭成为日常主要交通工具.大量的机动车所排放的尾气也逐步成为我国空气的主要污染源之一.
①请写出一种污染空气的气体的名称: .
②为实现环境整体效率最优化,请提出减小或治理大气污染的一点建议: .

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
(1)工业上常用高浓度的K2CO3 溶液吸收CO2,得溶液X,再利用电解法使K2CO3 溶液再生,其装置示意图如下:

①在阳极区发生的反应包括 和H++HCO3-![]() H2O+CO2↑。
H2O+CO2↑。
②简述CO32-在阴极区再生的原理 。
(2)再生装置中产生的CO2和H2在一定条件下反应生成甲醇等产物,工业上利用该反应合成甲醇。已知:25 ℃,101 KPa下:
H2(g)+![]() O2(g)
O2(g)![]() H2O(g)ΔH1=-242kJ·mol-1
H2O(g)ΔH1=-242kJ·mol-1
CH3OH(g)+![]() O2(g)
O2(g)![]() CO2(g)+2H2O(g)ΔH2=-676kJ·mol-1
CO2(g)+2H2O(g)ΔH2=-676kJ·mol-1
①写出CO2和H2生成气态甲醇等产物的热化学方程式 。
②下面表示合成甲醇的反应的能量变化示意图,其中正确的是 (填字母序号)。

A B C D
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
 、
、
①该电池外电路电子的流动方向为 (填写“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.12g铁粉加入25mL 2molL﹣1的氯化铁溶液中,充分反应后,其结果是( )
A.铁有剩余,溶液呈浅绿色,Cl﹣浓度基本不变
B.往溶液中滴入无色KSCN溶液,显黄色
C.Fe2+和Fe3+的物质的量之比为6:1
D.氧化产物与还原产物的物质的量之比为2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的液态化合物XY2,在一定量O2中恰好完全反应:XY2(l)+3O2(g)==XO2(g)+2YO2(g),其中l、g分别表示物质为液体、气体。冷却后,在标准状况下,测得生成物的体积为672mL,密度为2.56 g·L-1.
(1)反应前O2的体积为______________。
(2)化合物XY2的摩尔质量是_____________。
(3)在XY2分子中,X、Y两元素的质量之比为3∶16,则X、Y两元素分别为___________和___________(写元素名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列氧化还原反应中,水既不作氧化剂又不作还原剂的是( )
①2Na+2H2O=2NaOH+H2↑
②2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
③2F2+2H2O=O2+4HF
④3NO2+H2O=2HNO3+NO
⑤NaH+H2O=NaOH+H2↑
⑥2Na2O2+2H2O=4NaOH+O2↑
A. ③④⑥ B. ②③⑤ C. ①②③⑤ D. ④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com