
����Ŀ��2014��ŵ��������ѧ�������Ĺ����Ƿ�����һ�ָ�Ч�������Ĺ�Դ������ɫ��������ܣ�LED����ijͬѧ�Դ˷dz�����Ȥ���������ijͬѧ��������ռ��Ĺ�����
��1��LED�о���ʼ�ڶ�̼���辧����о���1907�꣬Ӣ����ѧ��Henry Joseph Round������ʩ�ӵ���ʱ�ܹ���̼���辧���з��ַ������� ��i��̼���辧���������壮
��ii��̼����ľ����ṹ����ʯ�����ƣ���̼���辧���У�̼ԭ����������С�Ļ�����̼ԭ�Ӻ�����ԭ����ɣ�ÿ��̼ԭ�������������Ļ���
��iii��̼�����У�̼ԭ�Ӳ�ȡ�ӻ���ʽ������Χ�Ĺ�ԭ���γɵļ���Ϊ ��
��iv������ԭ�ӽṹ��֪ʶ���ͷ����ԭ�� ��
��2���ִ�LED��1962�꣬GE��˾ʹ�����黯�أ�GaAsxP1��x�������Ƴ��˺�ɫ��������ܣ����ǵ�һ�ſɼ���LED������Ϊ�ִ�LED֮�森����ֳ�������ɫLED���أ�GaP���ͻ�ɫLED̼���裬ʹ������չ���ȹ⡢�ƹ���̹⣮ ��i������Ԫ�����ڱ���λ���� �� ���̬ԭ�ӵļ۵����Ų�ʽΪ ��
��ii�����Ƿ��������黯�ػ������в��ӵ������õ����������λ�ã�����������䷢��Ч�ʣ���ԭ����Ϊ����ѡ����
A�����İ뾶������İ뾶С���õ����沿�������λ�ò���Ӱ�쾧��Ĺ��ͣ�
B��N�ĵ�һ�����ܴ������飬����ʧȥ���ӣ���������ԾǨ��
C��N�ĵ縺�Դ��Ӻ�õ���λ���д��������
D��N�����顢������ͬ�۵��ӽṹ�����ʣ����Ե�����������������ǿ����ɵȵ������壮
��3��1993�꣬�д������˿���������������ĵ�����LED��ƾ��˳ɾͣ��������2014��ŵ��������ѧ���� Ϊ���Ե�������ɫLED��ǿ������Ĺ�ϵ���õ���ͼ����ͼ�����ܵõ�������дһ�����ɣ�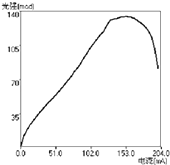
���𰸡�
��1��ԭ�ӣ�3��3��12��sp3��![]() �����Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����
�����Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����
��2���������ڢ�A�壻4s24p1��BC
��3������������ͬʱ��������С��153.0 mAʱ����������ɫLED��ǿ���ŵ��������Ӷ���ǿ������������153.0 mAʱ����ǿ���ŵ�������ǿ������
���������⣺��1����i��̼���辧������ԭ�Ӿ��壬���Դ��ǣ�ԭ�ӣ���ii�����ʯ�����У�̼ԭ����������С�Ļ�����6��̼ԭ�ӣ�̼���辧������С�Ļ�����6��ԭ�ӣ���C��Siԭ����Ŀ֮��Ϊ1��1������̼���辧���У�̼ԭ����������С�Ļ���3��̼ԭ�Ӻ�3����ԭ����ɣ�ÿ��Cԭ���γ�4��C��Si��������2��C��Si����2����Ԫ����4��C��Si����6����ϣ�����ÿ��̼ԭ������2��6=12 �������Ļ������Դ��ǣ�3��3��12����iii��̼�����У�̼ԭ���γ�4��C��Si�����ӻ������ĿΪ4��Cԭ�Ӳ�ȡsp3�ӻ���Cԭ������Χ��4��Siԭ���γ���������ṹ������Ϊ��109��28����
���Դ��ǣ�sp3��109��28������iv�����Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�������
���Դ��ǣ����Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ���������2����i������Ԫ�����ڱ���λ���ǣ��������ڢ�A�壬���̬ԭ�ӵļ۵����Ų�ʽΪ4s24p1 ��
���Դ��ǣ��������ڢ�A�壻4s24p1����ii��A�����İ뾶������İ뾶С���õ����沿�������λ�ò���Ӱ�쾧��Ĺ��ͣ�������ȷ��
B��N�ĵ�һ�����ܴ������飬������ʧȥ���ӣ��ʲ�������ȷ��
C�����黯�ػ�������û��Hԭ�ӣ�����Nԭ�Ӳ����γ��������������ȷ��
N�ĵ縺�Դ��Ӻ�õ���λ���д��������
D��N�����顢������ͬ�۵��ӽṹ�����ʣ�N�����縺�Խϴ��Ե�����������������ǿ����ɵȵ������壬������ȷ��
��ѡ��BC����3����ͼ��֪������������ͬʱ��������С��153.0 mAʱ����������ɫLED��ǿ���ŵ��������Ӷ���ǿ������������153.0 mAʱ����ǿ���ŵ�������ǿ��������
���Դ��ǣ�����������ͬʱ��������С��153.0 mAʱ����������ɫLED��ǿ���ŵ��������Ӷ���ǿ������������153.0 mAʱ����ǿ���ŵ�������ǿ��������
�����㾫����������Ĺؼ���������ԭ�Ӿ�������֪ʶ����������ԭ�Ӽ��Թ��ۼ����϶��γɿռ���״�ṹ�ľ����ԭ�Ӿ��壮


 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ������18.4mol/L��Ũ��������0.4mol/L��ϡ����250mL���Իش��������⣺
��1��ͨ���������Ũ�����������������Ͳ��ȡ����ȡ����ֵΪV=______mL��������������С�����һλ��
��2������������Һ�IJ����У���ȷ��˳����________��������ţ�
�ٽ�Ũ����ת����������������ˮ���ձ��У����ò���������
����ȴ��ϡ�ͺõ���Һת��250mL����ƿ��
������Ͳ��ȡV mLŨ����
�ܸǺ�ƿ�����������µߵ���ҡ��
��С�ĵ���250mL����ƿ�м�����ˮ������̶���1-2cm��
���ý�ͷ�ιܵμ�����ˮ��Һ����̶�������
������������ˮϴ���ձ�2-3�Σ���ϴ��Һת����250mL����ƿ�У�����ҡ������ƿ��ʹ��Һ��Ͼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л�������������ȷ���ǣ� ��
A.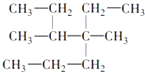 4������4��5�����һ�����
4������4��5�����һ�����
B.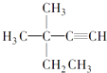 3��3��������1����Ȳ
3��3��������1����Ȳ
C.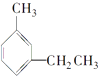 3�����һ���
3�����һ���
D.![]() 3������1��3������ϩ
3������1��3������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͬϵ���У��еIJ����ܱ�KMnO4������Һ���������ɷ����ᣬ��Ӧ���£�

(1)���б���ͬϵ��ס��ң�����ʽ����C10H14���ײ��ܱ�KMnO4������Һ����Ϊ�����ᣬ���Ľṹ��ʽ��______________�����ܱ�KMnO4������Һ����Ϊ����ʽΪC8H6O4�ķ����ᣬ���ҿ��ܵĽṹ��________�֡�
(2)�л����Ҳ�DZ���ͬϵ�����ʽҲ��C10H14�����ı����ϵ�һ�����ֻ��һ�֣���д�������п��ܵĽṹ��ʽ��__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ������С��36��A��B��C��D��E����Ԫ�أ�ԭ��������������A��D���γ�����Һ̬��������ң�ԭ�Ӹ����ȷֱ�Ϊ2��1��1��1��B���γɻ�������������Ԫ�أ�Cԭ�ӻ�̬ʱ2pԭ�ӹ������3��δ�ɶԵĵ��ӣ�E��̬ԭ�ӵĵ�һ�ܲ�������ܲ����ĵ�������ͬ���ڶ��ܲ�������ܲ����ĵ�������ͬ��
��1��B2A2���л��ϳɹ�ҵ��һ��ԭ�ϣ� ��i����B2A2ͨ��[Cu��NH3��2]Cl��Һ����Cu2C2����ɫ������[Cu��NH3��2]Cl�д��ڵĻ�ѧ���������� �� Cu+��̬��������Ų�ʽΪ ��
��ii��B2A2��ABC��Ӧ�ɵñ�ϩ�棨H2C=CH��C��N����ABC���ӵĹ����� �� ��ϩ�������̼ԭ�ӹ���ӻ�������
��2����ҵ����EB2��A2D��Ӧ����B2A2 �� ��i��EB2�е�B22����D22+��Ϊ�ȵ����壬D22+�ĵ���ʽ�ɱ�ʾΪ��1mol D22+�к��еĦм���ĿΪ ��
��ii����ҵ��B2A2��ԭ�ϣ�EB2��A2D���Լ����B2A2���ķе�Ӹߵ���������˳��Ϊ���û�ѧʽ��ʾ����������Ϊ ��
��iii��EB2����ľ����ṹ��NaCl��������ƣ���ͼ��ʾ������EB2�����к��е���������B22���Ĵ��ڣ�ʹ������һ�����������������ı߳��ֱ�Ϊ0.387nm��0.387nm��0.637nm��EB2�����У������ӵ���λ��Ϊ �� �������������������֮��ľ���Ϊnm������3λ��Ч���֣���EB2���ܶ�g/cm3����ʽ���ɣ���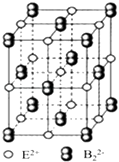
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A.�����յķ���������ë�ߺ�����
B.����ʯ��ʱ���¶ȼƵ�ˮ����������Һ����
C.��������Ӧʵ����Թܱ��ϵ�����������ϴ��
D.մ�����Թ��ڱ��ϵ���֬�����ȼ�Һϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ҫ����1 mol��L��1������100mL����ȡ��98%��Ũ���ᣨ�ܶ�Ϊ1.84g��mL��1��______________mL(����һλС��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������������ij��ƷAֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ��ͼ��������֮������ߴ�����ѧ�����絥����˫���ȣ��� 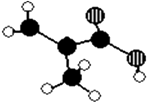
��1���ò�Ʒ�Ľṹ��ʽΪ �� ���еĹ��������� ��
��2���û�����ĺ˴Ź����������������շ壮
��3��������ţ����������У���A��Ϊͬ���칹����� �� ��A��Ϊͬϵ����� ��CH3CH=CHCOOH ��CH2=CHCOOCH3
��CH3CH2CH=CHCOOH ��CH3CH��CH3��COOH
��4��д����������״���Ӧ�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com