
【题目】下列有机化合物命名正确的是( )
A.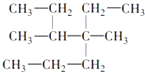 4﹣甲基﹣4,5﹣二乙基乙烷
4﹣甲基﹣4,5﹣二乙基乙烷
B.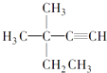 3,3﹣二甲基﹣1﹣戊炔
3,3﹣二甲基﹣1﹣戊炔
C.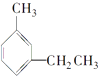 3﹣甲基乙基苯
3﹣甲基乙基苯
D.![]() 3﹣甲基﹣1,3﹣丁二烯
3﹣甲基﹣1,3﹣丁二烯
【答案】B
【解析】解:A、烷烃命名时,要选最长的碳链为主链,故主链上有7个碳原子,故为庚烷,从离支链近的一端给主链上碳原子编号,故在3号和4号碳原子上各有一个甲基,在4号碳原子上有一个乙基,故名称为3,4﹣二甲基﹣4﹣乙基庚烷,故A错误;B、炔烃命名时,要选含官能团的最长的碳链为主链,故主链上有5个碳原子,为戊炔,从离官能团最近的一端给主链上的碳原子编号,并表示出官能团的位置,故在3号碳原子上有2个甲基,故名称为3,3﹣二甲基﹣1﹣戊炔,故B正确;C、苯的同系物在命名时,从简单的侧链开始按顺时针或逆时针给主链上的碳原子进行编号,使侧链的位次和最小,故甲基在1号碳原子上,在3号碳原子上有乙基,故名称为:1﹣甲基﹣3﹣乙基苯,故C错误;
D、二烯烃命名时,要选含官能团的最长的碳链为主链,故为丁二烯,从离官能团最近的一端给主链上的碳原子编号,当两端离官能团一样近时,要从离支链近的一端给主链上碳原子编号,并表示出官能团的位置,则在1号和2号碳原子间、3号和4号碳原子间各有一条双键,在2号碳原子上有一个甲基,故名称为:2﹣甲基﹣1,3﹣丁二烯,故D错误;
故选B.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作中,错误的是( )
A. 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
B. 过滤可以除掉粗盐中可溶于水的杂质
C. 碘易溶于有机溶剂,可用CCl4萃取碘水中的碘
D. 用托盘天平称量固体药品时,砝码放在右盘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法不正确的是( )
A.向Na2CO3溶液中通入NH3 , ![]() 减小
减小
B.将0.1mol?L﹣1的K2C2O4溶液从25℃升温至35℃, ![]() 增大
增大
C.向0.1mol?L﹣1的HF溶液中滴加NaOH溶液至中性, ![]() =1
=1
D.向0.1mol?L﹣1的CH3COONa溶液中加入少量水, ![]() 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中,既能因发生化学反应而使溴水褪色,又能使高锰酸钾酸性溶液褪色的是( )
①CH3CH2CH2CH3 ②CH3CH2CH===CH2

A.①②③④ B.②③④
C.②④ D.只有②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫的多种化合物在工业中有重要的应用.
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性.
①Na2S2O4中S元素的化合价为 .
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为(填化学式).
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2 . 该反应的化学方程式为 .
(2)铬会造成环境污染.某酸性废水中含有Cr2O72﹣ , 处理时可用焦亚硫酸钠(Na2S2O3)将Cr2O转化为毒性较低的Cr3+ , 再调节pH至8,使铬元索沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg/L,达到排放标准.
①Na2S2O3参加反应的离子方程式为 .
②处理后的废水中Cr3+的物质的量浓度为 mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年诺贝尔物理学奖得主的贡献是发明了一种高效而环保的光源﹣﹣蓝色发光二极管(LED).某同学对此非常感兴趣,请你帮助某同学完成资料收集的工作.
(1)LED研究起始于对碳化硅晶体的研究.1907年,英国科学家Henry Joseph Round发现在施加电流时能够在碳化硅晶体中发现发光现象. (i)碳化硅晶体属于晶体.
(ii)碳化硅的晶胞结构与金刚石的相似,在碳化硅晶体中,碳原子所连接最小的环由个碳原子和个硅原子组成,每个碳原子连接个这样的环.
(iii)碳化硅中,碳原子采取杂化方式,与周围的硅原子形成的键角为 .
(iv)请结合原子结构的知识解释发光的原因: .
(2)准现代LED.1962年,GE公司使用磷砷化镓(GaAsxP1﹣x)材料制成了红色发光二极管.这是第一颗可见光LED,被视为现代LED之祖.随后又出现了绿色LED磷化镓(GaP)和黄色LED碳化硅,使光谱拓展到橙光、黄光和绿光. (i)镓在元素周期表的位置是 , 其基态原子的价电子排布式为 .
(ii)人们发现在磷砷化镓或磷化镓中掺杂氮(利用氮代替磷或砷的位置),可以提高其发光效率.其原因不可能为(多选).
A、氮的半径比磷和砷的半径小,用氮代替部分磷或砷的位置不会影响晶体的构型.
B、N的第一电离能大于磷和砷,容易失去电子,发生电子跃迁.
C、N的电负性大,掺杂后得到的位置中存在氢键.
D、N是与砷、磷具有相同价电子结构的杂质,但对电子束缚能力较磷和砷强,造成等电子陷阱.
(3)1993年,中村修二等人开发出首个明亮蓝光的氮化镓LED.凭借此成就,他获得了2014年诺贝尔物理学奖. 为测试氮化镓绿色LED光强与电流的关系,得到如图,从图中你能得到规律(写一条即可)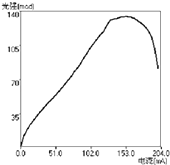
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积均为2L的甲乙丙三个恒容密闭容器中均加入0.10mol/L的N2、0.26mol/L的H2 , 进行合成氨反应:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJ/mol.图1表示不同反应条件下N2的浓度随时间的变化,图2表示其它条件相同,温度分别为T1、T2、T3且恒定不变,达到平衡时NH3的质量分数.下列判断不正确的是( ) 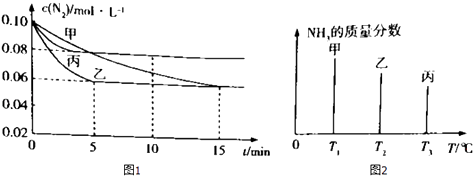
A.图2 中反应速率最快的是容器丙
B.图1 中容器乙的反应可能使用了催化剂
C.图1 中容器乙0~5 min时间内v ![]() =0.012mol/(L?min)
=0.012mol/(L?min)
D.图1 中容器丙内反应的平衡常数为2.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com