
【题目】“司乐平”是治疗高血压的一种临床药物,其有效成分M的结构简式如图所示。
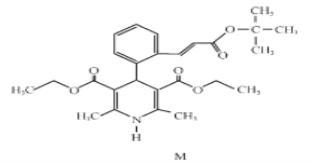
(1)下列关于M的说法正确的是______(填序号)。
a.属于芳香族化合物
b.遇FeCl3溶液显紫色
c.能使酸性高锰酸钾溶液褪色
d.1molM完全水解生成2mol醇
(2)肉桂酸是合成M的中间体,其一种合成路线如下:

已知: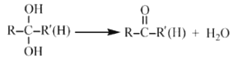
①烃A的名称为______。步骤I中B的产率往往偏低,其原因是__________。
②步骤III的反应类型是________。
③步骤Ⅳ反应的化学方程式为______________________________。
④肉桂酸的结构简式为__________________。
⑤C的同分异构体有多种,其中苯环上有一个甲基的酯类化合物有_____种。
【答案】 a、c 甲苯 反应中有一氯取代物和三氯取代物生成 加成反应 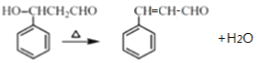
![]() 9。
9。
【解析】(1)a.M分子中有苯环,属于芳香族化合物,正确;b.M分子中没有酚羟基,遇FeCl3溶液不显紫色,b不正确;c.M分子中有碳碳双键,而且与苯环相连的碳原子上有氢原子,故其能使酸性高锰酸钾溶液褪色,正确;d.M分子中有3个酯基,故1molM完全水解生成3mol醇,d不正确。综上所述,关于M的说法正确的是a、c。
(2)由合成路线可知,A为甲苯,A在光照下发生甲基上的取代反应生成B,由B的分子式可知,B为二氯甲苯,由信息可知,B在碱性条件下水解产物可以发生消去反应得到苯甲醛。由C和D的分子式可知,C发生消去反应生成D,D为3-苯基丙烯醛,D与银氨溶液发生银镜反应后再酸化得到肉桂酸,则肉桂酸为3-苯基丙烯酸。
①烃A的名称为甲苯。步骤I中B的产率往往偏低,其原因是:该取代反应中,甲基上的H被取代的数目不好控制,反应中有一氯取代物和三氯取代物生成。
②步骤III的反应类型是加成反应。
③步骤Ⅳ反应的化学方程式为 。
。
④肉桂酸的结构简式为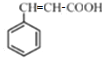 。
。
⑤C(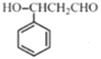 )的同分异构体有多种,其中苯环上有一个甲基的酯类化合物,其苯环上的另一个取代基有可能是-OOCCH3、-COOCH3或-CH2OOCH,苯环上的两个取代基有邻、间、对3种位置关系,所以共有9种。
)的同分异构体有多种,其中苯环上有一个甲基的酯类化合物,其苯环上的另一个取代基有可能是-OOCCH3、-COOCH3或-CH2OOCH,苯环上的两个取代基有邻、间、对3种位置关系,所以共有9种。


科目:高中化学 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。
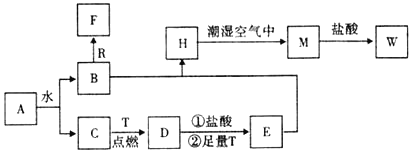
(1)物质A的化学式为_____,F化学式为____________;
(2)B和R在溶液中反应生成F的化学方程式为_____________________________;
(3)H在潮湿空气中变成M的化学方程式为_________________________________;
(4)A和水反应生成B和C的离子方程式为_________________________________;
(5)M投入盐酸中的离子方程式___________________________________________;
(6)“水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式____________________________;
(7)小苏打可作胃药,请写出其中和胃酸时的离子方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用98%的浓硫酸(密度为1.84 g·cm-3)配制1 mol·L-1的稀硫酸100 mL。配制过程中可能用到下列仪器:①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒。按使用先后顺序排列正确的是( )
A. ④③⑦⑤⑥ B. ②⑤⑦④⑥ C. ②⑥③⑦⑤⑥ D. ④③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室要用CuSO4·5H2O晶体配制500 mL 0.1 mol·L-1 CuSO4溶液,回答下列问题:

(1)应该用托盘天平称取CuSO4·5H2O________g。
(2)如图Ⅰ表示10 mL量筒中液面的位置,A与B,B与C刻度间相差1 mL,如果刻度A为8,量筒中液体的体积是________mL。
(3)若实验中如图Ⅱ所示的仪器有下列情况,对配制溶液的浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.定容前容量瓶底部有水珠__________________________;
B.定容时加水超过刻度线____________________________;
C.最终定容时俯视观察液面__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组,在学完分子晶体后,查阅了几种氯化物的熔、沸点,记录如下:
NaCl | MgCl2 | AlCl3 | SiCl4 | CaCl2 | |
熔点/℃ | 801 | 712 | 190 | -68 | 782 |
沸点/℃ | 1 465 | 1 418 | 230 | 57 | 1 600 |
根据这些数据分析,他们认为属于分子晶体的是( )
A.NaCl、MgCl2、CaCl2
B.AlCl3、SiCl4
C.NaCl、CaCl2
D.NaCl、MgCl2、AlCl3、SiCl4、CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是:
A. 氢氧化铝与稀硝酸反应:H+ + OH- = H2O
B. MgCl2溶液与氨水反应: Mg2+ + 2NH3·H2O = Mg(OH)2↓+2NH![]()
C. CuCl2溶液与铁粉反应: 3Cu2+ + 2Fe =3Cu + 2Fe3+
D. 锌与CH3COOH溶液反应:Zn + 2H+ = Zn2++ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
I.(1)海水中所得粗盐中通常含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,下列试剂加入的先后顺序正确的是________
A.BaCl2→Na2CO3→NaOH→HCl B.NaOH→BaCl2→Na2CO3→HCl
C.BaCl2→NaOH→Na2CO3→HCl D. Na2CO3→NaOH→BaCl2→HCl
(2)为了检验精盐中是否含有SO42-,正确的方法是____________________________。
II.海藻中提取碘的流程如图所示
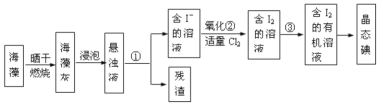
(1)灼烧过程中,需使用到的(除泥三角外)实验仪器有______
A.试管 B.瓷坩埚 C.坩埚钳 D.蒸发皿 E.酒精灯 F.三脚架
(2)指出提取碘的过程中有关实验操作名称:①________③__________④_________
(3)步骤②反应的离子方程式为___________________,该过程氧化剂也可以用H2O2,将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为__________
(4)下列关于海藻提取碘的说法,正确的是_________
A.含碘的有机溶剂呈现紫红色
B.操作③中先放出下层液体,然后再从下口放出上层液体
C.操作④时,温度计的水银球应伸入液面以下但不能触碰到蒸馏烧瓶的底部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量比为1:1的CO和H2组成的混合气体2.1 g在足量的氧气中点燃充分反应后,将产物立即通入足量的Na2O2固体中,固体质量增加为
A. 3.6 g B. 2.1g C. 7.2 g D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方式正确的是( )
A. H2气体中含有少量的CO2杂质可以通过灼热的炭粉除去
B. CO2气体中含有的少量HCl杂质可通过饱和Na2CO3溶液除去
C. K2CO3固体中含有少量的NaHCO3杂质可用加热的方式提纯
D. NaOH溶液中含有少量的Ba(OH)2可加入适量的Na2SO4过滤除去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com