
【题目】根据图填空。

(1)写出下列物质的化学式:A________________, C_________________。
(2)写出生成D的反应方程式_________________________________________。
(3)写出E→B的离子方程式__________________________________________。
【答案】 Fe KCl 4Fe(OH)2+2H2O+O2![]() 4Fe(OH)3 2Fe3++Fe
4Fe(OH)3 2Fe3++Fe![]() 3Fe2+
3Fe2+
【解析】由转化关系可知,C与AgNO3反应生成白色沉淀为AgCl,溶液进行焰色反应显紫色,说明含有K+,由此推知C为KCl;又白色沉淀在空气中变成灰绿色,最后变为红褐色,说明该沉淀为Fe(OH)2,则D为Fe(OH)3,E为FeCl3,所以B为FeCl2,某溶液为KOH,进而推知A为Fe单质。
(1)A的化学式为Fe,C的化学式为KCl;
(2)白色沉淀在空气中变成灰绿色,最后变为红褐色,反应的化学方程式为4Fe(OH)2+2H2O+O2![]() 4Fe(OH)3;
4Fe(OH)3;
(3)由FeCl3与铁反应生成FeCl2的离子方程式为2Fe3++Fe![]() 3Fe2+。
3Fe2+。


科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列判断正确的是
A. 0.1 mol Na2O2含有的离子总数为0.4NA
B. 常温常压下,18g H2O 所含的中子数为8NA
C. 5.6 g铁与足量盐酸反应转移的电子数为0.3NA
D. 将含0.l mol FeCl3的饱和溶液制成胶体后,生成的Fe(OH)3胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中要配制2mol/L的NaCl溶液980 ml,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
A. 980 mL,114.7g B. 500mL, 58.5g
C. 1000 mL, 117 g D. 1000mL,117.0g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的量的说法中正确的是( )
A.物质的量就是物质的质量B.摩尔是国际单位制中的基本单位
C.某容器中含有1mol氯D.阿伏加德罗常数是6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
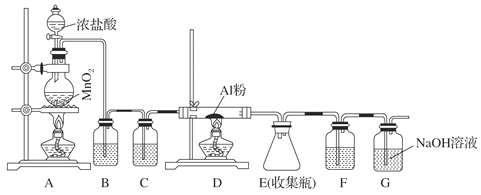
(1)其中装置A用来制备氯气,写出其离子反应方程式:_____________________________。
(2)装置B中盛放饱和NaCl溶液,该装置的主要作用是_____________________________。
(3)G为尾气处理装置,其中反应的化学方程式:___________________________________。
(4)制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:与足量AgNO3溶液反应,称量生成的AgCl质量。此方案__________(填“可行”,“不可行”)并说明理由__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1 mol·L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法不正确的是 ( )

A. a曲线表示的离子方程式为:AlO2-+H++H2O ==Al(OH)3↓
B. b和c曲线表示的离子反应是相同的
C. M点时,溶液中沉淀的质量为3.9 g
D. 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,则这个碳原子被称为“手性碳原子”.凡含有手性碳原子的物质一定具有光学活性.如有机物:有光学活性,发生下列反应后生成的有机物仍有光学活性的是( )
①与甲酸发生酯化反应
②与NaOH溶液反应
③与银氨溶液作用
④在催化剂存在下与H2作用.![]()
A.②④
B.①③
C.①④
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是
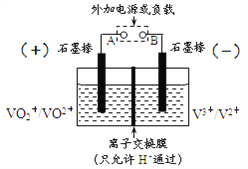
A. 放电时,右槽发生还原反应
B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C. 充电时,每转移1mol电子,n(H+)的变化量为1mol
D. 充电时,阴极电解液pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温常压下向2L的恒温密闭容器中投入2mol A和1mol B,发生可逆反应 3A(g)+2B(s)2C(g)+D(g)△H=﹣a kJ/mol.5min后达平衡,测得容器中n(C)=0.8mol.则下列说法正确的是( )
A.3v(A)=2v(C)=0.16 mol/(Lmin)
B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能)
C.升高温度,该平衡正向速率减小,故平衡逆向移动
D.使用催化剂或缩小容器体积,该平衡均不会移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com