
����Ŀ���о����������������ڴ����к������ӵ������ʱ���漰���·�Ӧ��
2NO2(g)��NaCl(s)![]() NaNO3(s)��ClNO(g)��K1����H1<0 (��)��
NaNO3(s)��ClNO(g)��K1����H1<0 (��)��
2NO(g)��Cl2(g)![]() 2ClNO(g)��K2����H2<0 (��)
2ClNO(g)��K2����H2<0 (��)
(1)4NO2(g)��2NaCl(s)![]() 2NaNO3(s)��2NO(g)��Cl2(g)��ƽ�ⳣ��K��________(��K1��K2��ʾ)��
2NaNO3(s)��2NO(g)��Cl2(g)��ƽ�ⳣ��K��________(��K1��K2��ʾ)��
(2)Ϊ�о���ͬ�����Է�Ӧ(��)��Ӱ�죬�ں����£���2 L�����ܱ������м���0.2 mol NO��0.1 mol Cl2��10 minʱ��Ӧ(��)��ƽ�⡣���10 min��v(ClNO)��7.5��10-3 mol��L-1��min-1����ƽ���n(Cl2)��_____________mol��NO��ת������1��______________��
(3)��ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2 ,�䷴ӦΪ��2CO��2NO![]() N2��2CO2 ��H<0
N2��2CO2 ��H<0
�����¶Ⱥ�������ֲ���������£��ܹ�˵���÷�Ӧ�ﵽƽ��״̬�ı�־����________��
A.��Ӧ������������ʵ���Ũ�����
B.NO��CO��CO2��N2������֮��Ϊ2:2:2:1
C.���������ܶȱ��ֲ���
D.��λʱ��������1molNO��ͬʱ������1molCO����
���ﵽƽ������������NOת���ʵ�����________��
A.ѡ�ø���Ч�Ĵ���B.�����������������뺤������ѹǿ
C.���ͷ�Ӧ��ϵ���¶�D.��С���������
���о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ����.Ϊ�˷ֱ���֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ�����,ijͬѧ���������ʵ�飬����ʵ�������Ѿ������±��С�
ʵ���� | T(��) | NO��ʼŨ��(mol/L) | CO��ʼŨ��(mol/L) | �����ıȱ����(m2/g) |
�� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
�� | a | b | c | 124 |
�� | 350 | d | e | 124 |
����a=_______________��e=__________________
���𰸡�![]() 2.5��10-2 75% D CD 280 5.80��10-3
2.5��10-2 75% D CD 280 5.80��10-3
��������
(1)��Ӧ���Ļ�ѧƽ�ⳣ��= ![]() ����Ӧ����ƽ�ⳣ��=
����Ӧ����ƽ�ⳣ��= 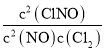 ����Ӧ��ƽ�ⳣ��=
����Ӧ��ƽ�ⳣ��= 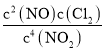 ��
��
(2)����ת������ع�ʽ��⣻
(3) ����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬���Դ��жϣ�
�����NOת����Ҳ����ʹƽ�������ƶ������ڷ�Ӧ��һ�����ϵ����С�Ŀ��淴Ӧ���ʼ�ѹ����С����������ԴﵽĿ�ģ�
������������ͬ������£������жϱ��������ʵ�Ӱ�죬Ҫ��֤�¶ȶ����ʵ�Ӱ�죬�����ıȱ��������Ӧ��ij�ʼŨ�ȵ�Ҫ��ͬ��ͬ������֤�����ıȱ���������ʵ�Ӱ�죬�¶ȡ���Ӧ��ij�ʼŨ��Ҫ��ͬ��
(1)��Ӧ���Ļ�ѧƽ�ⳣ��= ![]() ����Ӧ����ƽ�ⳣ��=
����Ӧ����ƽ�ⳣ��= 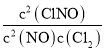 ����Ӧ��ƽ�ⳣ��=
����Ӧ��ƽ�ⳣ��= 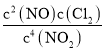 �����Լ���K=
�����Լ���K=![]() ��
��
(2)ת����n��Cl2��=![]() ��7.5��10-3molL-1min-1��2L��10min=7.5��10-2mol����ƽ���n��Cl2��=0.1mol��7.5��10-2mol=2.5��10-2mol��ת����n��NO��=7.5��10-3molL-1min-1��2L��10min=0.15mol����NO��ת������1=0.15mol��0.2mol��100%=75%��
��7.5��10-3molL-1min-1��2L��10min=7.5��10-2mol����ƽ���n��Cl2��=0.1mol��7.5��10-2mol=2.5��10-2mol��ת����n��NO��=7.5��10-3molL-1min-1��2L��10min=0.15mol����NO��ת������1=0.15mol��0.2mol��100%=75%��
(3) ����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��
A. ��Ӧ������������ʵ���Ũ����ȣ�����˵���������ʵ�Ũ�Ȼ������ٷ����仯������˵����Ӧ�ﵽƽ��״̬��
B. NO��CO��CO2��N2������֮��Ϊ2:2:2:1����˵���������ʵ�Ũ�Ȼ������ٷ����仯������˵����Ӧ�ﵽƽ��״̬��
C.��Ӧ��������ﶼ�����壬�ҷ�Ӧ����������������������ֲ��䣬����������ܶ�һֱ���ֲ��䣬����˵���ﵽƽ��״̬��
D. ��λʱ��������1molNO��ͬʱ������1molCO���ɣ�˵�����淴Ӧ������Ӧ���ʺ��淴Ӧ������ȣ��ﵽƽ��״̬��
��ѡD��
�����NOת����Ҳ����ʹƽ�������ƶ������ڷ�Ӧ��һ�����ϵ����С�Ŀ��淴Ӧ���ʼ�ѹ����С����������ԴﵽĿ�ģ��÷�ӦΪ���ȷ�Ӧ�������¶ȿ���ʹ��Ӧ�����ƶ������NOת���ʣ�ʹ�ô����ͱ����������������뺤������ѹǿ��ƽ�ⶼ���ƶ������ܴﵽĿ�ģ��ʴ�ΪCD��
��̽��ʵ��Ҫ���ֵ�һ�����������������ıȱ������ͬ�����¶�Ӧ����ȣ���a=280��CO��ʼŨ�����ر���������ʵ��Ҫ����һ�£���e=5.80��10-3��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֳ��õ�ζ�������ݹ���Ҫ������NaCl�ĺ�����Ӧ����15g/100 mL��Ī�����ǽϼ�һ�ֲ���Cl-�����ķ������ֲ��ø÷�����ij���۽����Ƿ����NaCl������Ҫ��ʵ��ԭ������(25��)��
Ag++Cl-=AgCl��(��ɫ)�� Ksp(AgCl)=1.8��10-23
2Ag++CrO42-=Ag2CrO4��(ש��) Ksp(Ag2CrO4)=1.2��10-22
ȷ��ȡ������Ʒ5.00 mLϡ����100 mL��������ȡ��10.00 mL ������ƿ�У��������м���������K2CrO4��Һ����0.100 0 mol/L������������Һ�ζ����ظ�ʵ�����Ρ�
(1)��Ʒϡ�����У���_____��ȡ������Ʒ��Ӧ��______�ж��ݣ������õ���������_______________��
(2)�ζ����۾�Ӧע��____________������_____________���ﵽ�ζ��յ㡣
(3)�ζ�����ʱ���ζ�����Һ������ͼ��ʾ�������Ϊ________��
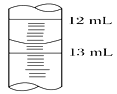
(4)��������������������Һ��ƽ�����Ϊ12.50 mL����ϡ�ͺ�Ľ�����NaCl��Ũ��Ϊ________mol/L�������۽����Ƿ����NaCl������ ________(����ϡ������ϡ�)��
(5)��25���£���Ũ�Ⱦ�Ϊ0.1 mol��L-1��MgCl2��CuCl2�����Һ����μ��백ˮ��������________�������ѧʽ���������ӳ�����ȫ������Ũ�ȡ�10-5��ʱ��Һ��pHΪ________________��֪25 ��ʱKsp[Mg(OH)2]=1.8��10-11��Ksp[Cu(OH)2]=1.0��10-21��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������˵������ȷ����( )
A.1mol H2��0.5mol O2��Ӧ�ų����Ⱦ���H2��ȼ����
B.1mol H2SO4��lmol Ba(OH)2��ȫ��Ӧʱ�ų����Ƚ����к���
C.��֪C(s) + ![]() O2(g) = CO(g) ��H=-110.5kJ/mol����̼��ȼ����Ϊ110.5kJ/mol
O2(g) = CO(g) ��H=-110.5kJ/mol����̼��ȼ����Ϊ110.5kJ/mol
D.ͬ��ͬѹ�£���֪�������ȷ�Ӧ��2A(g)+B(g)=2C(1) ��H1��2A(l)+B(l)=2C(g) ��H2������Hl����H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ�����������õ�������ѧ���ʣ����㷺Ӧ�������������С��Ӻ��ܷ���(��CoO��Co2O3������Al��Li��)����ȡ��CoCl2��6H2O������������ʾ��

��ش��������⣺
(1)����I�г���2Li + 2H2O=2 Li OH + H2����Ӧ�⣬��Ҫ�����Ļ�ѧ��Ӧ����ʽΪ____________________��
(2)��֪Co2O3����ǿ�����ԣ�������II�н�����Ϊ���ᣬ��ɵĺ����_______��
(3)�������Тٵ�Ŀ���dz�ȥAl3+��д���ò���Ӧ�����ӷ���ʽ______��
(4)����ʵ��������CoCO3������Ĺ��������������ƾ��ƺͲ������⣬����______��______(����������)��
(5)����������HCl��Χ�н��еģ��䲽����______��_____�����ˡ�ϴ�ӡ����ϴ�ӹ����п����ù�ҵ�ƾ�����ˮ�����ŵ���_____��
(6)ijͬѧ�ñ���������Һ�ζ�δ֪Ũ�ȵ�CoCl2��Һ�����п���Ϊָʾ������____(��ѡ������������ӵ���ɫ����)
A��KCl B��KSCN C��K2CrO4 D��K2S
��֪����������20��ʱ����ɫ��Kspֵ���±�
��ѧʽ | AgCl | AgSCN | Ag2S | Ag2CrO4 |
��ɫ | ��ɫ | dz��ɫ | ��ɫ | ��ɫ |
Ksp | 2.0��10-10 | 1.0��10-12 | 2.0��10-48 | 2.0��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС����ʵ������ȡƯ�ۣ���̽��������ʯ���鷴Ӧ�����Ͳ��
��֪���ٶ���������Ũ���ᷴӦ���Ʊ�������ͬʱ����MnCl2
�������ͼ�ķ�ӦΪ���ȷ�Ӧ���¶Ƚϸ�ʱ�������ͼ�ܷ������·�Ӧ��3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
����ȤС���������ͼʵ��װ�ã�����ʵ�顣

��ش��������⣺
��1���ټ�װ�������Ʊ��������䷢����Ӧ�����ӷ���ʽΪ______________��װ�õ������� _____________
��ʵ����������NaOH��Һ���մ�Ũ�����MnO2��Ӧ��ϵ�е��������塣�������¶Ȳ�ͬʱ�����ɵIJ��������NaClO��NaClO3��NaCl�е����ֻ����֡�����˵������ȷ����___________��������ĸ��
A��������ΪNaClO3��NaCl����μӷ�Ӧ���������ͻ�ԭ�������ʵ���֮��Ϊ1��5
B��������ΪNaClO��NaCl�������պ����Һ��c(ClO-)=c(Cl-)
C��������ΪNaClO��NaClO3��NaCl����NaOH��Cl2���Ӧ�����ʵ���֮��Ϊ2��1
��2��С���Ա���֣�������Ca(ClO)2����������С������ֵ���������ۺ���Ϊ�������ԭ���Dz�������δ��ʯ���鷴Ӧ���ݳ����Լ��¶����ߡ�Ϊ��̽����Ӧ�����Բ����Ӱ�죬������ȡһ������ʯ���飬�������ٵ�ͨ�������������ó���Ca(ClO)2��Ca(ClO3)2�������ʵ����ʵ�����n���뷴Ӧʱ�䣨t���Ĺ�ϵ���ߣ����Ա�ʾΪ��ͼ(������������ˮ�ķ�Ӧ)������ȡʯ�����к���Ca(OH)2�����ʵ���Ϊ______________mol��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���������ض��dz�����ˮ��������ij��ȤС������мΪԭ��ģ�ҵ���Ʊ��Ȼ�������һ�������Ʊ�������ص���������:

��ش���������:
(1)����������ͨ����������������������������е��ŵ���____________��
(2)���ϳ���������Na2FeO4�����ӷ���ʽΪ___________________________��
(3)Ϊ�˼���������������������FeCl3��Һ���Ƿ���Fe2+��ijͬѧȡ������Һ���Թ��У�ѡ�������Լ����ԴﵽĿ�ĵ���_______(����ĸ)��
a.KSCN��Һ b.NaOH��Һ c.K3[Fe(CN)6]��Һ d.������Һ
��ѡ������KMnO4��Һ���м��飬����������Ƿ��������˵������:____________��
(4)�����£���ʹ6.4mol/LFeCl3������Һ������Fe(OH)3���������Һ��pHС��____��{��֪��ʵ�������£�Ksp[(Fe(OH)3]=6.4��10-36}
(5)�ڲ�ͬ�¶ȺͲ�ͬpH�£�FeO42-���ȶ�����ͼ��ʾ:

����ͼ������Ϊ��������ϳ�����Na2FeO4�IJ��ʣ��ɲ�ȡ��ʵ��������ΧΪ______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܴ���Br����CO![]() ��SO
��SO![]() ��Al3����I����Mg2����Na����7�������е�ij���֡���ȡ����Һ����ʵ�飬�õ���������
��Al3����I����Mg2����Na����7�������е�ij���֡���ȡ����Һ����ʵ�飬�õ���������
������Һ�еμ�������ˮ����Һ���ɫ��������ɫ����ð����
�������ó�ɫ��Һ�м�������BaCl2��Һ���������ɣ�
����������Һ�м����μӵ�����Һ����Һ������ɫ��
��֪��5Cl2��I2��6H2O===10HCl��2HIO3
�ݴ˿����жϣ�����Һ�϶������ڵ���������
A. Al3����Mg2����SO![]() B. Mg2����CO
B. Mg2����CO![]() ��I��
��I��
C. Al3����SO![]() ��I�� D. Al3����Br����SO
��I�� D. Al3����Br����SO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ����20.00 mL 0.10 mol��L��1CH3COOH��Һ�е���0.10 mol��L��1 NaOH��Һ����ҺpH��NaOH��Һ�����ϵ��ͼ��ʾ������˵����ȷ����

A. T��ʱ��CH3COOH����ƽ�ⳣ��Ka=1.0��10-3
B. M���Ӧ��NaOH��Һ���Ϊ20.0 mL
C. N����Q����ʾ��Һ��ˮ�ĵ���̶ȣ�N��Q
D. N����ʾ��Һ��c(Na+)��c(OH��)��c(CH3COO��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС��ѧ��������ͼ��ʾװ����ȡ��ϩ��������������£�
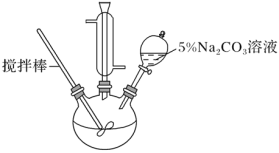
��.ȡ10.0 g��ϩ�ᣨCH2=CHCOOH����6.0 g�״���������Ũ���������������ƿ�У����Ӻ������ܣ��ý�������裬ˮԡ���ȡ�
��ַ�Ӧ����ȴ������Һ�м���5% Na2CO3��Һϴ�������ԡ�
��Һ��ȡ�ϲ���״Һ�壬������ˮNa2SO4���壬���˺������ռ�70��90 ����֡�
(1) �����ܵ�������______
(2) ��ʵ���п��������л�������Ľṹ��ʽΪ____����һ�ּ��ɣ���
(3) ������л��Һ��5% Na2CO3��Һϴ�ӵ�Ŀ����_______��
(4) ������м�����ˮNa2SO4�����������______��
(5) ��֪�״��ӷ����ж��ԣ���д��1���ڱ�ʵ������Ҫ��ȡ�İ�ȫ������ʩ_____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com