
ЁОЬтФПЁП(1)дкЯТСаЗДгІжаЃЌЫЎзїбѕЛЏМСЕФЪЧ________ЁЃ
A.Cl2+H2O![]() HCl+HClO B.NaH+H2O=NaOH+H2Ёќ
HCl+HClO B.NaH+H2O=NaOH+H2Ёќ
C.3Fe+4H2O(g)![]() Fe3O4 + 4H2 D. H2+CuO
Fe3O4 + 4H2 D. H2+CuO![]() H2O+Cu
H2O+Cu
E. 2NaCl+2H2O![]() 2NaOH+H2Ёќ+Cl2Ёќ
2NaOH+H2Ёќ+Cl2Ёќ
(2)гУЫЋЧХБэЪО3Cl2+6KOH=5KCl+KClO3+3H2OЕчзгзЊвЦЕФЗНКЭЪ§ФПЃК__________________ЁЃ
(3)дквЛЖЈЬѕМўЯТЃЌРћгУжУЛЛЗДгІX+Y=W+ZЃЌПЩЪЕЯжЮяжЪжЎМфЕФзЊЛЏ
ЂйШєXЮЊMgЃЌWЮЊCЃЌдђZЮЊ__________________ЁЃ
ЂкШєXЮЊSiO2ЃЌWЮЊCOЃЌИУЗДгІдкЙЄвЕЕФгУЭОЪЧ___________________ЁЃ
(4) ФГЮДжЊШмвКжаПЩФмКЌгаFe2+ЃЌШЗЖЈКЌИУРызгЕФЪЕбщЗНАИЮЊЃКШЁЩйСПИУШмвКгкЪдЙмжаЃЌЯШ__________________ЃЌдй__________________ЃЌдђЫЕУїШмвКжаКЌгаFe2+ЁЃ
ЁОД№АИЁПBCE 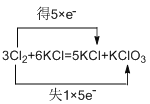 MgO жЦБИДжЙш ЕЮМгМИЕЮKSCNШмвКЃЌЮоУїЯдЯжЯѓ МгШыТШЫЎЃЈЛђH2O2ЛђЯЁЯѕЫсЕШЃЌКЯРэОљПЩЃЉЃЌШмвКБфГЩбЊКьЩЋ
MgO жЦБИДжЙш ЕЮМгМИЕЮKSCNШмвКЃЌЮоУїЯдЯжЯѓ МгШыТШЫЎЃЈЛђH2O2ЛђЯЁЯѕЫсЕШЃЌКЯРэОљПЩЃЉЃЌШмвКБфГЩбЊКьЩЋ
ЁОНтЮіЁП
ЃЈ1ЃЉбѕЛЏМСдкбѕЛЏЛЙдЗДгІжаБЛЛЙдЃЌЯрЙидЊЫиЛЏКЯМлНЕЕЭЃЌA.ЗДгІЧАКѓH2OжадЊЫиЛЏКЯМлВЛБфЃЛB.NaHжаHЕФЛЏКЯМлЮЊ-1МлЃЌЗДгІНсЪјКѓЛЏКЯМлЩ§ИпЮЊ0МлЃЌЖјH2OЗДгІНсЪјКѓHгЩ+1МлНЕЕЭЮЊ0МлЃЌH2OБЛЛЙдЃЌзїбѕЛЏМСЃЛC.FeгЩ0МлЩЯЩ§жС+2ЁЂ+3МлЃЌH2OжаHгЩ+1МлНЕЕЭЮЊ0МлЃЌH2OБЛЛЙдЃЌзїбѕЛЏМСЃЛD.H2OзїбѕЛЏВњЮяЃЛE.H2OжаHгЩ+1МлНЕЕЭЮЊ0МлЃЌH2OБЛЛЙдЃЌзїбѕЛЏМСЃЛЙЪД№АИЮЊЃКBCEЃЛ
ЃЈ2ЃЉгЩЗНГЬЪНПЩжЊЃЌClЛЏКЯМлгЩ0МлЩ§ИпЮЊ+5МлЃЌЭЌЪБгЩ0МлНЕЕЭЮЊ-1МлЃЌИљОнЗНГЬЪНПЩжЊЃЌЪЇШЅЕФЕчзгЪ§ЮЊЃК1ЁС5e-ЃЌЕУЕНЕФЕчзгЪ§ЮЊЃК5ЁСe-ЃЌЙЪгУЫЋЧХБэЪО3Cl2+6KOH=5KCl+KClO3+3H2OЕчзгзЊвЦЕФЗНКЭЪ§ФПЮЊЃК ЃЛ
ЃЛ
ЃЈ3ЃЉЂйгЩЬтПЩжЊЃЌИУЗДгІЪЧжУЛЛЗДгІЃЌШєXЮЊMgЃЌWЮЊCЃЌдђЗЂЩњЕФЗДгІЮЊЃКMgЃЋCO2![]() MgOЃЋCЃЌгЩДЫПЩжЊЃЌZЮЊMgOЃЛ
MgOЃЋCЃЌгЩДЫПЩжЊЃЌZЮЊMgOЃЛ
ЂкШєXЮЊSiO2ЃЌWЮЊCOЃЌдђЗЂЩњЕФЗДгІЪЧЃК2CЃЋSiO2![]() SiЃЈДжЙшЃЉЃЋ2CO
SiЃЈДжЙшЃЉЃЋ2CO![]() ЃЌИУЗДгІдкЙЄвЕЩЯЕФгУЭОЪЧжЦБИДжЙшЃЛ
ЃЌИУЗДгІдкЙЄвЕЩЯЕФгУЭОЪЧжЦБИДжЙшЃЛ
ЃЈ4ЃЉЮДжЊШмвКжаПЩФмКЌгаFe2+ЃЌПЩНЋЦфбѕЛЏЮЊFe3ЃЋЃЌдйНјааМьбщЃЌЭЌЪБвЊХХГ§ШмвКжаFe3ЃЋЕФИЩШХЃЌгЩДЫЪЕбщВйзїЮЊЃКШЁЩйСПИУШмвКгкЪдЙмжаЃЌЯШЕЮМгМИЕЮKSCNШмвКЃЌЮоУїЯдЯжЯѓЃЌМгШыТШЫЎЃЈЛђH2O2ЛђЯЁЯѕЫсЕШЃЌКЯРэОљПЩЃЉЃЌШмвКБфГЩбЊКьЩЋЃЌдђЫЕУїШмвКжаКЌгаFe2ЃЋЁЃ


 ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ
ЬьЬьЯђЩЯвЛБОКУОэЯЕСаД№АИ аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
аЁбЇЩњ10ЗжжггІгУЬтЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвдТСЭСПѓЃЈжївЊГЩЗжЮЊAl2O3ЃЌКЌSiO2КЭFe2O3ЕШдгжЪЃЉЮЊдСЯЩњВњТСКЭЕЊЛЏТСЕФвЛжжЙЄвеСїГЬШчЯТ[вбжЊЃКSiO2дкЁАМюШмЁБЪБзЊЛЏЮЊТСЙшЫсФЦЃЈNaAlSiO4ЁЄnH2OЃЉГСЕэ]ЁЃ

ЃЈ1ЃЉВйзїIЁЂЂђЕФУћГЦЮЊ____________ЁЃ
ЃЈ2ЃЉгУбѕЛЏЮяЕФаЮЪНБэЪОТСЙшЫсФЦЕФЛЏбЇЪН_____________ЁЃ
ЃЈ3ЃЉдгжЪFe2O3зюКѓДцдкгк___________жаЁЃ
ЃЈ4ЃЉЙЄвЕжЦБИAlЕФЛЏбЇЗНГЬЪНЮЊ__________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГаЃЛЏбЇаЁзщбЇЩњРћгУЯТЭМЫљСазАжУНјаа ЁАЬњгыЫЎЗДгІЁБЕФЪЕбщЃЌВЂРћгУВњЮяНјвЛВНжЦШЁFeCl3ЁЄ6H2OОЇЬхЁЃ(ЭМжаМаГжМАЮВЦјДІРэзАжУОљвбТдШЅ)
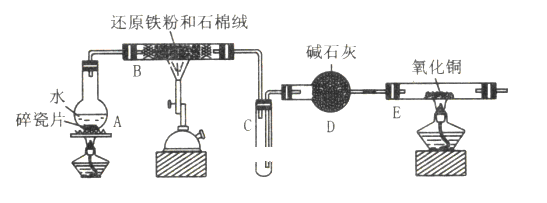
(1)зАжУBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ_________________________________________
(2)зАжУEжаЕФЯжЯѓЪЧЃК_____________________________________________________
(3)ЭЃжЙЗДгІЃЌД§BЙмРфШДКѓЃЌШЁЦфжаЕФЙЬЬхЃЌМгШыЙ§СПЯЁбЮЫсГфЗжЗДгІЃЌЙ§ТЫЁЃМђЪіМьбщТЫвКжа Fe3+ЕФВйзїЗНЗЈЃК____________________________________________________________________
(4)ИУаЁзщбЇЩњРћгУЩЯЪіТЫвКжЦШЁFeCl3ЁЄ6H2OОЇЬхЃЌЩшМЦСїГЬШчЯТЃК
![]()
ВНжшIжаЭЈШыCl2ЕФзїгУЪЧ____________________________
ИУСїГЬжаашБЃГжбЮЫсЙ§СПЃЌжївЊдвђЪЧ(НсКЯРызгЗНГЬЪНМђвЊЫЕУї)
________________________________________________________________
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПбЇЯАЛЏбЇжЊЪЖЪБПДЪщЪЧКмживЊЕФЃЌЯТУцМИОфЛАИФБфздПЮБОЃЌЦфжаЫЕЗЈе§ШЗЕФЪЧ
A. дзгЮќЪеЙтЦзвЧвЛАугУгкВтЖЈЮяжЪжаЕФЗЧН№ЪєдЊЫи
B. зібцЩЋЗДгІЪЕбщЪБЃЌВЛФмгУЯИЬњЫПДњЬцВЌЫП
C. МјБ№бђУЋКЭУоЛЈПЩгУзЦЩеКѓЮХЦјЮЖЕФЗНЗЈ
D. аЁЫеДђЪЧживЊЕФЛЏЙЄдСЯЃЌдкдьжНЁЂЗФжЏЁЂЪЏгЭЁЂЪГЦЗЕШЙЄвЕгаЙуЗЖЕФгУЭО
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПXЁЂYЁЂZЪЧЖЬжмЦкдЊЫиЃЌдзгАыОЖЕФДѓаЁЃКr(Y)>r(X)>r(Z)ЃЌШ§жждЊЫиЕФдзгађЪ§жЎКЭЮЊ15ЃЛXЁЂYЁЂZШ§жждЊЫиЕФГЃМћЕЅжЪдкЪЪЕБЬѕМўЯТПЩЗЂЩњШчЯТЭМЫљЪОзЊЛЏЙиЯЕЃЌЦфжаRЮЊ10ЕчзгЗжзгЃЌЪЧвЛжжГЃМћЕФЮоЛњШмМСЁЃЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ

A. XдЊЫиЮЛгкжмЦкБэжаЕФЕк16Са
B. XЕФЧтЛЏЮяЗаЕувЛЖЈИпгкYЕФЧтЛЏЮяЕФЗаЕу
C. XЁЂYЁЂZдЊЫиПЩвдзщГЩвЛжжЗжзгЪНЮЊZ2Y2X4ЕФЛЏКЯЮяЃЌЦфЫЎШмвКжаЫЎЕФЕчРыЪмЕНСЫвжжЦ
D. XЁЂYЁЂZдЊЫиСНСНжЎМфОљФмаЮГЩдзгИіЪ§БШЮЊ1 : 1ЕФЛЏКЯЮя
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПгаЙиОЇЬхЕФНсЙЙШчЭМЫљЪО,ЯТСаЫЕЗЈжаВЛе§ШЗЕФЪЧ
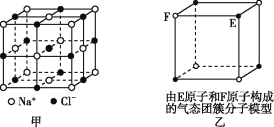
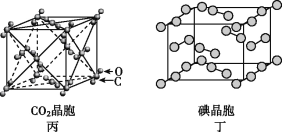
A. дкNaClОЇЬх(ЭММз)жа,ОрNa+зюНќЕФCl-аЮГЩе§АЫУцЬх
B. ИУЦјЬЌЭХДиЗжзг(ЭМвв)ЕФЗжзгЪНЮЊEFЛђFE
C. дкCO2ОЇЬх(ЭМБћ)жа,вЛИіCO2ЗжзгжмЮЇга12ИіCO2ЗжзгНєСк
D. дкЕтОЇЬх(ЭМЖЁ)жа,ДцдкЗЧМЋадЙВМлМќКЭЗЖЕТЛЊСІ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЙигкТШЫЎЕФа№Ъіе§ШЗЕФЪЧ
A. аТжЦТШЫЎПЩЪЙРЖЩЋЪЏШяЪджНЯШБфКьКѓЭЪЩЋ B. ЙтееТШЫЎгаЦјХнЗХГіЃЌИУЦјЬхЪЧCl2
C. аТжЦТШЫЎжажЛКЌCl2КЭH2OЗжзг D. ТШЫЎЗХжУЪ§ЬьКѓЫсадНЋБфШѕ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПдкФГЮоЩЋШмвКжаЛКТ§ЕиЕЮШыNaOHШмвКжБжСЙ§СПЃЌВњЩњГСЕэЕФжЪСПгыМгШыЕФNaOHШмвКЬхЛ§ЕФЙиЯЕШчЭМЫљЪОЃЌгЩДЫШЗЖЈЃЌдШмвКжаКЌгаЕФбєРызгЪЧЃЈ ЃЉ
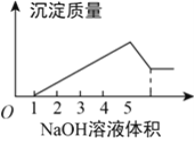
A. Mg2+ЁЂAl3+ЁЂBa2+ B. H+ЁЂMg2+ЁЂAl3+
C. H+ЁЂCu2+ЁЂAl3+ D. жЛгаMg2+ЁЂAl3+
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПAЁЂDЁЂFОљЪЧгЩЖЬжмЦкдЊЫизщГЩЕФЕЅжЪЃЌГЃЮТЯТCЪЧвКЬх, DЁЂFЮЊЦјЬхЃЌAЁЂBЁЂEЮЊЙЬЬхЃЌЦфжаBЮЊЕЛЦЩЋЙЬЬхЁЃ
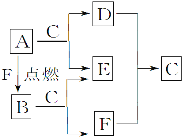
ЧыЛиД№ЯТСаЮЪЬтЃК
(1)BКЭEЕФЛЏбЇЪНЃКB________ЃЌE________ЁЃ
(2)AгыCЗДгІЕФРызгЗНГЬЪНЮЊ____________________________________________________________ЁЃ
(3)ЯТСаЙигкAЕФа№Ъіе§ШЗЕФЪЧ________(ЬюађКХ)ЁЃ
ЂйAгаКмЧПЕФЛЙдадЁЁ ЂкAЕФбцЩЋЗДгІГЪзЯЩЋЁЁ
ЂлЩйСПAПЩвдБЃДцдкРфЫЎРяЁЁ ЂмAзХЛ№ЪБгІбЁгУХнФУ№Л№Цї
(4)НЋAЁЂУОЁЂТСИї0.3 molЗжБ№ЗХШы100 mL 1 molЁЄLЃ1ЕФбЮЫсжаЃЌЭЌЮТЭЌбЙЯТВњЩњЕФЦјЬхЬхЛ§жЎБШЪЧ________(ЬюађКХ)ЁЃ
Ђй1ЁУ2ЁУ3ЁЁ Ђк6ЁУ3ЁУ2ЁЁ Ђл3ЁУ1ЁУ1ЁЁ Ђм1ЁУ1ЁУ1
ВщПДД№АИКЭНтЮі>>
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com