
����Ŀ��![]() ��
��![]() ��
��![]() ��
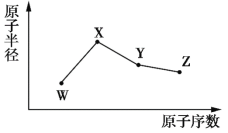
��![]() �����ֳ����Ķ���������Ԫ�أ���ԭ�Ӱ뾶��ԭ�������ı仯��ͼ��ʾ����֪
�����ֳ����Ķ���������Ԫ�أ���ԭ�Ӱ뾶��ԭ�������ı仯��ͼ��ʾ����֪![]() ��һ�ֺ��ص�������Ϊ18��������Ϊ10��
��һ�ֺ��ص�������Ϊ18��������Ϊ10��![]() �Ƕ�����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�������ϡ������Ԫ�ص�ԭ�Ӱ뾶����
�Ƕ�����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�������ϡ������Ԫ�ص�ԭ�Ӱ뾶����![]() �ĵ��ʳʻ�ɫ�������ڻ�ɽ�ڸ���������˵����ȷ����
�ĵ��ʳʻ�ɫ�������ڻ�ɽ�ڸ���������˵����ȷ����
A.![]() ������������Ӧˮ���������ǿ��
������������Ӧˮ���������ǿ��![]()
B.�����Ӱ뾶��![]()
C.![]() �ļ��⻯��ķе����ͬ������Ԫ�صļ��⻯��
�ļ��⻯��ķе����ͬ������Ԫ�صļ��⻯��
D.����״���µ������![]() �ĵ�����
�ĵ�����![]() �ĵͼ�������ͬʱͨ��Ʒ����Һ�У�Ʒ����ҺѸ����ɫ
�ĵͼ�������ͬʱͨ��Ʒ����Һ�У�Ʒ����ҺѸ����ɫ
���𰸡�C
��������
![]() ��
��![]() ��
��![]() ��
��![]() �����ֳ����Ķ�����Ԫ�أ�
�����ֳ����Ķ�����Ԫ�أ�![]() ��һ�ֺ��ص�������Ϊ18��������Ϊ10����֪
��һ�ֺ��ص�������Ϊ18��������Ϊ10����֪![]() ��������Ϊ8����
��������Ϊ8����![]() ��
��![]() ��
��![]() �Ƕ�����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�������ϡ������Ԫ��ԭ�ӵİ뾶������
�Ƕ�����Ԫ����ԭ�Ӱ뾶����Ԫ�أ�������ϡ������Ԫ��ԭ�ӵİ뾶������![]() Ϊ
Ϊ![]() ��
��![]() �ĵ��ʳʻ�ɫ�������ڻ�ɽ�ڸ�������
�ĵ��ʳʻ�ɫ�������ڻ�ɽ�ڸ�������![]() Ϊ
Ϊ![]() ��
��![]() Ϊ
Ϊ![]() ����������ѡ��ɡ�
����������ѡ��ɡ�
A.![]() �ķǽ����Ա�
�ķǽ����Ա�![]() ǿ��������������Ӧˮ��������ԣ�
ǿ��������������Ӧˮ��������ԣ�![]() ��A�����
��A�����
B.![]() �ĵ��Ӳ���࣬���Ӱ뾶���
�ĵ��Ӳ���࣬���Ӱ뾶���![]() ��
��![]() �ĵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��
�ĵ��Ӳ�ṹ��ͬ���˵����Խ�����Ӱ뾶ԽС�������Ӱ뾶��![]() ��B�����
��B�����
C.![]() ���Ӽ�����������
���Ӽ�����������![]() �ļ��⻯��ķе����ͬ������Ԫ�صļ��⻯�C����ȷ��
�ļ��⻯��ķе����ͬ������Ԫ�صļ��⻯�C����ȷ��
D.�����ʵ�����![]() ��
��![]() һ��ͨ��Ʒ����Һ��ǡ����ȫ��Ӧ������������ᣬ����ʹƷ����Һ��ɫ��D�����
һ��ͨ��Ʒ����Һ��ǡ����ȫ��Ӧ������������ᣬ����ʹƷ����Һ��ɫ��D�����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӏ�������ֵ������˵����ȷ����
A.��⾫��ͭʱת����NA�����ӣ������ܽ���32gͭ
B.�����£�pH=3��NH4Cl��Һ�У���ˮ�����OH��Ũ��Ϊ10-11mol/L
C.12.0g���ڵ�NaHSO4�к��е���������Ϊ0.1NA
D.�����£�1mol/LFe2(SO4)3��Һ�У�Fe3+��SO42-������������NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ԭ����������4������Ԫ��Xm+��Yn�������Ӻ�����Ӳ�ṹ��ͬ�������X��Y��Ԫ�ص�������ȷ����
A. X��ԭ������С��Y��ԭ������ B. X��Y�ĺ˵����֮���ǣ�m��n��
C. X��Y����ͬһ���� D. YԪ����XԪ�ص�������֮����8��(m+n)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ��ԭ������������������ֶ�����Ԫ�أ���
��ԭ������������������ֶ�����Ԫ�أ���![]() ��Ԫ�����ڱ���ԭ�Ӱ뾶��СԪ�أ�
��Ԫ�����ڱ���ԭ�Ӱ뾶��СԪ�أ�![]() ��
��![]() ���ڣ�
���ڣ�![]() Ԫ�ؿ�����
Ԫ�ؿ�����![]() ��
��![]() ��
��![]() Ԫ�طֱ��γɼס��ҡ����������ʣ��Ҽס��Ҿ�Ϊ10���ӻ������Ϊ18����˫ԭ�ӻ����
Ԫ�طֱ��γɼס��ҡ����������ʣ��Ҽס��Ҿ�Ϊ10���ӻ������Ϊ18����˫ԭ�ӻ����![]() Ԫ��ԭ�ӵ������������������Ӳ�����ȡ���֪���ף�������������˵����ȷ����
Ԫ��ԭ�ӵ������������������Ӳ�����ȡ���֪���ף�������������˵����ȷ����
A.�����Ӱ뾶��![]()
B.![]() ��
��![]() ����Ԫ�ع�ͬ�γɵ�10��������3��
����Ԫ�ع�ͬ�γɵ�10��������3��
C.![]() Ԫ����Ԫ�����ڱ��е�λ���ǵڶ����ڵڢ�A��
Ԫ����Ԫ�����ڱ��е�λ���ǵڶ����ڵڢ�A��
D.�������ɷǽ���Ԫ����ɣ�ֻ�����ۼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����飨NaHSO2��HCHO��2H2O��������ˮ���ʰ�ɫ��״�����ᾧ�Է�״��������ӡȾ��ҵ�Ļ�ԭ�����ϳɼ����ǹ�ҵ�е�Ư������SO2�����Zn����ȩΪԭ��������鼰����п�Ĺ����������£�
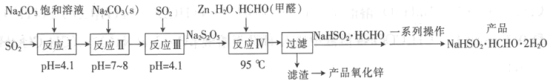
�ش��������⣺
��1��NaHSO2��HCHO��2H2O��SԪ�صĻ��ϼ�Ϊ__________��
��2������ӦI���еõ��IJ�����__________���ѧʽ����
��3���������ӦII��������ӦIII���м���ͨ��SO2��Ŀ����_________��
��4������Ӧ�����Ļ�ѧ����ʽΪ______________��
��5����������������������__________���ѧʽ����
��6����һϵ�в�������������Ũ��________��________��________���
��7��һ�ֲⶨ�����������������ķ������£���ȡa g��Ʒ��������ˮ�У������Թ����ĵ�ˮ����Ӧ����NaHSO4��HCOOH������ַ�Ӧ���������BaCl2��Һ�����ˣ������������Ƶ�����Ϊb g��
�ٵ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ___________��
�ڲ�Ʒ�������������Ϊ___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ɱ���ܱ������з������淴Ӧ��2NO2(g)![]() 2NO(g)��O2(g)������Ϊ��Ӧ�ﵽƽ��״̬�ı�־��
2NO(g)��O2(g)������Ϊ��Ӧ�ﵽƽ��״̬�ı�־��
A.��λʱ��������n mol O2��ͬʱ����n mol NO2
B.NO2��NO��O2���ߵ����ʵ���Ũ��֮��Ϊ2��2��1
C.���������ܶȲ��ٸı�
D.����������ѹǿ���ٱ仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 L�ܱ������У�A��B��C������̬���ʹ����˿��淴Ӧ����ϵ������ijһ�¶�ʱ��A��B��C���ʵ�����ʱ��Ĺ�ϵ��ͼ�ף�C�İٷֺ������¶ȵĹ�ϵ��ͼ�ҡ�
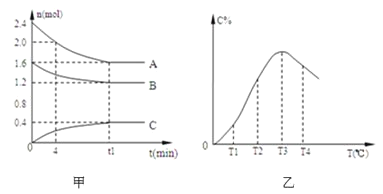
���з�������ȷ����(�� ��)
A.0��4 minʱ��A��ƽ����Ӧ����Ϊ0.02 mol��L��1��min��1
B.�÷�Ӧ�Ļ�ѧ����ʽΪ2A(g)+B(g)C(g)
C.��T1��T2�仯ʱ������Ӧ���ʴ����淴Ӧ����
D.�÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����20mLNaOH��Һ����μ���![]() ������Һ���ζ�������ͼ��ʾ�������ж���ȷ����
������Һ���ζ�������ͼ��ʾ�������ж���ȷ����
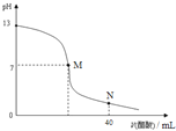
A.��M�㣬����ǡ�÷�Ӧ��ȫ
B.�ζ�ǰ������![]() ���ڼ���
���ڼ���![]()
C.NaOH��Һ�����ʵ���Ũ��Ϊ![]()
![]()
D.��N�㣬c(CH3COO-)> c(Na+)>c(H+)> c(CH3COOH)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������¿�ͼ����������˵����ȷ����
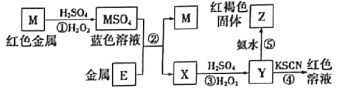
A.E2���������Ա�M2����������ǿ
B.�ڷ�Ӧ����������ϡ������ܿ������ɫ����
C.��Ӧ�ݵ����ӷ���ʽ�ɱ�ʾΪE2����3OH����E(OH)3��
D.�ڷ�Ӧ����ֻ����Ũ���ᣬ�ȱ������ԣ��ֱ�����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com