
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.2 | 5.2 | 12.4 |
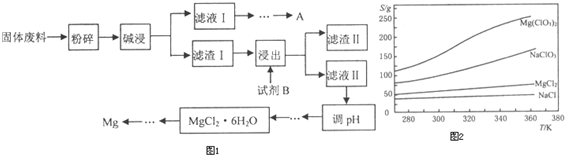
| ||
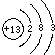 ,故答案为:
,故答案为: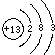 ;
;
| ||
| ||


科目:高中化学 来源: 题型:
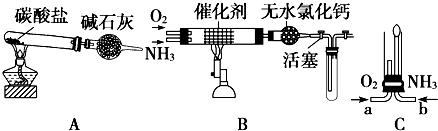
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、4.48g |
| B、3.36g |
| C、3.25g |
| D、2.80g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H6 |
| B、C4H6 |
| C、C3H4 |
| D、C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 阴离子 | MnO4-、SiO32-?、CO32?、I-、ClO-、Cl-、SO42-? |
| 阳离子 | Fe2+、Fe3+、NH4+、Ag+、Al3+ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NaW+Z2═2NaZ+W2 |
| B、2NaX+Z2═2NaZ+X2 |
| C、2NaW+Y2═2NaY+W2 |
| D、2NaZ+X2═2NaX+Z2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水稀释100倍,9<pH<11 |
| B、加入少量NH4Cl固体,溶液的pH升高 |
| C、加水稀释后c(OH-)/c(NH3?H2O)值将减小 |
| D、完全中和等浓度等体积的盐酸,耗氨水的体积比pH=11的NaOH溶液大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com