
【题目】下列哪一组结构或物质的元素组成很可能是不相同的
A. 细菌体内的DNA与细胞膜
B. 蓝藻细胞内的拟核与玉米的细胞壁
C. 骨骼肌细胞内的线粒体与染色体
D. 植物细胞的细胞壁与动物细胞中的糖原
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的三种钠盐NaX、NaY、NaZ的溶液,其pH依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是
A. HX、HZ、HY B. HZ、HY、HX
C. HX、HY、HZ D. HY、HZ、HX
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质性质与应用对应关系正确的是( )
A. KAl(SO4)2 12H2O能水解生成Al(OH)3胶体,可用作净水剂
B. SO2有漂白、杀菌性能,可在食品加工中大量使用
C. MnO2有较强的氧化性,可作H2O2分解的氧化剂
D. Si是半导体材料,可用于制光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50 mL 0.1 mol·L-1的NaCl溶液和50 mL 0.5 mol·L-1的CaCl2溶液混合后,若溶液的体积为二者体积之和,则混合溶液中c(Cl-)为
A.2 mol·L-1 B.1 mol·L-1
C.0.67 mol·L-1 D.0.55 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减少环境污染,某工厂生产玻璃与处理窑炉气的工艺流程如下:
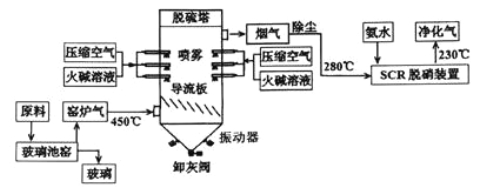
(1)生产普通玻璃、普通硅酸盐水泥和高炉炼铁都要用到的原料是________(填化学式),该物质在制玻璃过程中参与的化学方程式是_______________。
(2)生产玻璃中产生的窑炉气除SO2和氮氧化物外主要还有_________。
(3)窑炉气中的SO2一部分来源于原料中添加剂Na2SO4的热分解,该反应方程式为___________;
(4)在“脱硫塔”中喷洒火碱而不用石灰水的原因是___________;在进入“SCR脱硝装置”的烟气要先除尘的原因是_________________。
(5)烟气脱硝可采用氨水(NH3·H2O)脱除烟气的NO,其原理如图:

该脱硝原理中,NO最终转化为____________(填化学式)。当消耗1molNH3和0.25molO2时,除去的NO在标准状况下的体积为_____________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。

(1)甲同学用上图所示装置测定CO2的质量。实验时稀硫酸是与样品中的_________(填“Na2CO3”或
"NaCl”)发生反应。仪器b的名称是_____________。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是____________。
(2)乙同学用下图所示方法和步骤实验:

①操作I涉及的实验名称有__________、洗涤;操作Ⅱ涉及的实验名称有干燥、___________。
②乙测得的样品中Na2CO3质量分数的计算式为___________________。
(3)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计)____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨、烧碱在工农业生产和工业废水处理中具有广泛用途。回答下列问题:
(1)工业上制取硝酸的第一步是以氨和空气为原料,用铂一铑合金网为催化剂,在氧化炉中(温度为800℃)进行氨催化氧化反应。该反应的氧化产物为____________(填名称)。
(2)某工业废水中含有2Mg2+、Cu2+等离子。取一定量的该工业废水,向其中滴加烧碱溶液,当Mg(OH)2开始沉淀时,溶液中![]() 为____________。已知Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20
为____________。已知Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20
(3)已知反应N2(g)+3H2(g)![]() 2NH3(g)的△H=-92.2kJ/mol,1molN2(g),1molH2(g)分子中化学键断裂时分别需要吸收944.6KJ、436KJ的能量,则1molNH3(g)分子中化学键断裂时需吸收的能量为__________KJ。
2NH3(g)的△H=-92.2kJ/mol,1molN2(g),1molH2(g)分子中化学键断裂时分别需要吸收944.6KJ、436KJ的能量,则1molNH3(g)分子中化学键断裂时需吸收的能量为__________KJ。
(4)Fritz Haber 研究了下列反应:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
在500℃、20MPa时,将N2和H2通入到体积为2L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:

①在0~10min内,平均反应速率v(NH3)= ___________。
②在10~20min内,各物质浓度变化的原因可能是_________(填“加了催化剂”或“降低温度”),其判断理由是________________。
③温度和密闭容器的容积一定时,当容器内的总压强不再随时间而变化,反应是否达到了化学平衡状态?___________(填“是”或“否”)其判断理由是_________________。
④500℃时,该反应的平衡常数K的计算式为_________(不需要算出结果,) NH3的体积分数是_________(保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过电解MnSO4和ZnSO4制取Zn和MnO2,原料为软锰矿和闪锌矿,软锰矿中含MnO2约a%,SiO2约20%,Al2O3约4%,其余为水分,闪锌矿中含ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分。
I.(1)为了测量软锰矿中MnO2含量的测定,现将14. 5g软锰矿溶于足量的稀硫酸中,加入足量的碘化钾晶体,充分反应后,过滤,将滤液加水稀释至1L,取25.00ml该溶液于锥形瓶中,滴入几滴淀粉溶液作指示剂,用0. l000mol.L-1的标准Na2S2O3溶液滴定,消耗标准液50. 00mL,则软锰矿中MnO2含量_________。(己知:2KI+2 H2SO4+ MnO2=I2+2H2O+MnSO4+K2SO4;I2+2 S2O32-=2I-+ S4O62-)
II.研宄人员开发了综合利用这两种资源的同槽酸浸工艺,工艺流程如图l所示.

请回答下列问题:
(2)反应I的滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2 (SO4)3等,试完成反应I中生成CuSO4和MnSO4的化学方程MnO2+CuS+___________=________+_________+CuSO4+MnSO4.
(3)反应II加入适量锌的作用是___________;如果锌过量,还会进一步发生反应的离子方程式为_____________。
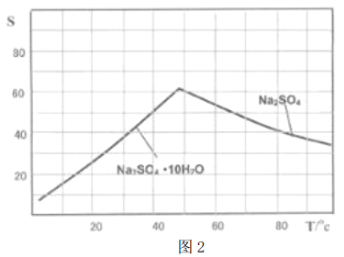
(4)图2是Na2SO4和Na2SO4·10H2O的溶解度曲线(g/l00g水),则Ⅳ中得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶→___________→用乙醇洗涤→干燥,用乙醇洗涤而不用水洗的原因是__________________________。
(5)用惰性电极电解MnSO4和ZnSO4制得Zn和MnO2的总反应是_______________________。
(6)本工艺可以循环利用的物质除MnO2、MnCO3、ZnCO3以外,还有___________(写化学式).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH值相同的醋酸和盐酸,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH值仍相同,则m和n的关系是( )
A. m>n B. m=n C. m<n D. 不能确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com