
【题目】在一隔热系统中,向20. 00 mL 0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000mol·L-1的NaOH溶液,测得混合溶液的温度变化如图。下列相关说法正确的是( )

A. 若a点溶液呈酸性,此时:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-)
B. 从a到b:![]() 逐渐增大
逐渐增大
C. 水的电离程度:b点<c点
D. 溶液的PH值:a点<c点<b点
【答案】A
【解析】a点时醋酸反应一半,溶液中存在的CH3COONa与CH3COOH的浓度比为1:1;b点时酸碱恰好完全反应,溶质为CH3COONa;c点时,加入的NaOH反应了一半,溶液中存在CH3COONa和NaOH,且浓度比为1:1。A选项,a点混合溶液以CH3COOH电离为主,溶液呈酸性,根据电荷守恒c(CH3COO-)+c(OH-)=c(Na+)+c(H+),溶液中醋酸根总量是Na+两倍,而醋酸根以CH3COO-和CH3COOH两种形式存在,所以2c(Na+)=c(CH3COOH)+c(CH3COO-),换算消除c(Na+),则c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-),A正确。B、从a点到b点,随着NaOH加入,溶液中CH3COOH分子不断消耗,CH3COO-不断增加,所以c(CH3COOH)/c(CH3COO-)逐渐减小,B错误。C、b点溶质为CH3COONa,CH3COO-的水解促进了H2O的电离,c点溶质为CH3COONa和NaOH,NaOH电离生成的OH-抑制了水的电离,所以水的电离程度b点>c点,C错误。D、a点溶质为1:1的CH3COOH和CH3COONa,溶液呈酸性;b点溶质为CH3COONa,溶液呈碱性;c点溶质为1:1的CH3COONa和NaOH,溶液呈碱性,由于存在较多的NaOH,因此溶液碱性比b强,则三点溶液的pH值大小关系为a点<b点<c点,D错误。正确答案A。


 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液,分别加水稀释至体积V,pH随lgV的变化情况如图所示,下列叙述中正确的是

A.XOH是弱碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述中正确的是
A.任何能使熵值增大的过程都自发进行
B.已知热化学方程式2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
C.人类利用的能源都是通过化学反应获得的
D.1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体打火机使用的燃料要求在室温下为气态,稍一加压,就变成液体,一减压(打开阀门)就汽化并易燃烧。下表中的有机物能较好地满足这些要求的是( )
选项 | A | B | C | D |
分子式 | C2H6 | C3H8 | C4H10 | C5H12 |
熔点/℃ | -183.3 | -181.7 | -138.4 | -127.9 |
沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学综合应用
(Ⅰ) 选择合适的图象:
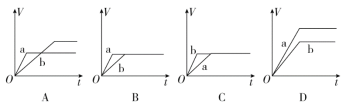
(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是_____________。
(2)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是 。
(Ⅱ)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极反应式是_________________________。
(2)乙装置中铁极的电极反应式为_______________________。
(3)检验石墨(C)极反应产物的方法是____________ _________。
(4)若在标准状况下,有2.24 L氧气参加反应,丙装置中阴极析出铜的质量为________g。

(Ⅲ)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的高效水处理剂,其电解制法如图所示。电解过程中,两极均有气体产生,Y极区域溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍澄清。查阅资料得知,高铁酸根离子(FeO![]() )在溶液中呈紫红色。
)在溶液中呈紫红色。
(1)电解过程中,X极区溶液的pH___________(填“增大”“减小”或“不变”)。
(2)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-===FeO![]() +4H2O和_____ _____。
+4H2O和_____ _____。
(3)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少__________g。
(4)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果: _______与盐酸反应最快。
Ⅱ.利用下图装置可以验证非金属性的变化规律。

(2)仪器A的名称为________,干燥管D的作用是____________________________。
(3)若要证明非金属性:S>C>Si,则A中加 ____________、B中加NaHCO3溶液、C中加___________,观察到C中溶液的现象为________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——有机化学基础】
香豆素(结构如下图中I所示)是用途广泛的香料,由香豆素经下列图示的步骤可转变为水杨酸。

![]()
请回答下列问题:
(1)香豆素分子中的官能团的名称为__________,步骤II→III的反应类型为___________。
(2)有机物III的结构简式为_________,在上述转化过程中,设计反应步骤II→III的目的是_____。
(3)下列关于有机物I、II、III、IV的叙述中正确的是________(选填序号)。
A. 可用FeCl3溶液来鉴别II和III
B. IV中核磁共振氢谱共有4种峰
C. I、II、III均可使溴的四氯化碳溶液褪色
D. 1molI最多能和5molH2发生加成反应
(4)写出水杨酸与过量NaHCO3溶液反应的化学方程式_____________。
(5)化合物IV有多种同分异构体,符合下列两个条件的芳香族同分异构体共有_____种。
①遇氯化铁溶液发生显色反应 ②能发生水解反应和银镜反应
其中,核磁共振氢谱共有5种吸收峰,且吸收峰面积比为1:2:2:2:1同分异构体的结构简式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com