
(10分)“铜都”安徽铜陵有许多黄铜矿(主要成分为CuFeS2,含少量Al2O3、SiO2),黄铜矿是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。
(1)火法炼铜首先要焙烧黄铜矿,其反应原理为2CuFeS2+O2 Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是 (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为 L。
Cu2S+2FeS+SO2。CuFeS2中Cu和Fe元素的化合价均为+2价,被还原的元素是 (填元素符号),若反应中转移0.3mol电子时,则标准状况下产生SO2的体积为 L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,HNO3的还原产物为NO,试写出Cu2S与稀硝酸反应的离子方程式 ,该反应中稀硝酸体现 (填“氧化性”、“还原性”或“酸性”)。
(3)焙烧黄铜矿还可得到Cu2O。将21.6g Cu2O加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,在所得溶液中加入1.0molL-1的NaOH溶液1.0L,此时溶液呈中性。原硝酸的物质的量浓度为 。
(1) Cu、O(2分) 1.12(2分) (2) 3Cu2S+16H++4NO3-==6Cu2++3S↓+4NO↑+8H2O
氧化性、酸性(每空2分) (3) 2.2molL-1(每空2分)
【解析】
试题分析:(1)CuFeS2中Cu和Fe元素的化合价均为+2价,则S元素的化合价是—2价。根据方程式2CuFeS2+O2 Cu2S+2FeS+SO2可知,在反应中铜元素的化合价从+2价降低到+1价,得到1个电子,氧元素的化合价从0价降低到—2价,得到2个电子,则被还原的元素是Cu、O。S元素的化合价部分从—2价升高到+4价,失去6个电子,因此若反应中转移0.3mol电子时,则标准状况下产生SO2的物质的量为0.3mol÷6=0.05mol,体积为0.05mol×22.4L/mol=1.12L。
Cu2S+2FeS+SO2可知,在反应中铜元素的化合价从+2价降低到+1价,得到1个电子,氧元素的化合价从0价降低到—2价,得到2个电子,则被还原的元素是Cu、O。S元素的化合价部分从—2价升高到+4价,失去6个电子,因此若反应中转移0.3mol电子时,则标准状况下产生SO2的物质的量为0.3mol÷6=0.05mol,体积为0.05mol×22.4L/mol=1.12L。
(2)焙烧黄铜矿产生的Cu2S可被稀硝酸氧化为Cu2+ 和硫单质,则1mol硫化亚铁失去4mol电子。HNO3的还原产物为NO,氮元素得到3个电子,因此根据电子得失守恒可知Cu2S与稀硝酸反应的离子方程式为3Cu2S+16H++4NO3-==6Cu2++3S↓+4NO↑+8H2O;该反应中有NO和硝酸铜产生,因此稀硝酸体现氧化性和酸性。
(3)21.6g Cu2O的物质的量是21.6g÷144g/mol=0.15mol,加入到500mL某浓度的稀硝酸中,固体物质完全反应,生成Cu(NO3)2和NO,因此反应中转移0.3mol电子,则根据电子得失守恒可知NO是0.3mol÷3=0.1mol,即被还原的硝酸是0.1mol。在所得溶液中加入1.0molL-1的NaOH溶液1.0L,此时溶液呈中性,这说明溶液中的铜离子转化为氢氧化铜沉淀,溶质是硝酸钠,根据钠离子守恒可知硝酸钠的物质的量是1mol,则未被还原的硝酸是1mol。原硝酸的物质的量浓度为(1mol+0.1mol)÷0.5L=2.2mol/L。
考点:考查氧化还原反应的应该判断与计算


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:填空题
(12分)如图为电解装置,X、Y为电极材料,a为电解质溶液。

(1)若a为含有酚酞的KCl溶液,X为Fe,Y为石墨,电解一段时间后:
X电极附近可观察到的实验现象是 ;
写出Y电极的电极反应式 。
(2)若要实现Cu +H2SO4=CuSO4+H2↑,
则Y电极材料是 ;
写出X电极的电极反应式 。
(3)若要利用该装置在铁制品表面镀上一层银,则a为 ,反应前两电极的质量相等,反应后电极质量相差2.16g,则该过程理论上通过电流表的电子数为 。
(4)若X、Y均为惰性电极,a为NaOH溶液,电解一段时间后,溶液的pH (填“增大”“不变”“减小”),若要使溶液恢复原来的状态,可往溶液中加入 。
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列过程属于物理变化的是:
A.煤的气化 B.石油分馏 C.石油裂解 D.煤的直接液化
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
铝与过量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是
A.加入适量的铝粉 B.加入适量的水
C.加入少量的硫酸铜溶液 D.加入浓度较大的盐酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省濉溪县高三第二次月考化学试卷(解析版) 题型:选择题
常温下,下列各组微粒在指定溶液中一定能大量共存的是
A.0.1 mol·L-1 Fe(NO3)3溶液中:Mg2+、H+、SO42-、Cl-
B.0.1 mol·L-1 KClO溶液中:Na+、H+、Cl-、NO3-
C.0.1 mol·L-1氨水中:Ba2+、Ag+、NH4+、NO3-
D.c(OH-)=10-13 mol·L-1的溶液中:MnO4-、Na+、Br-、CH3CHO
查看答案和解析>>
科目:高中化学 来源:2014-2015学年辽宁省高三下学期初考理综化学试卷(解析版) 题型:填空题
铜在工农业生产中有着广泛的用途。
(1)配制CuSO4溶液时需加入少量稀H2SO4,其原因是 (只写离子方程式)。
(2)某同学利用制得的CuSO4溶液,进行以下实验探究。
①图甲是根据反应Fe+CuSO4=Cu+FeSO4设计的原电池,请在图甲中的横线上完成标注。
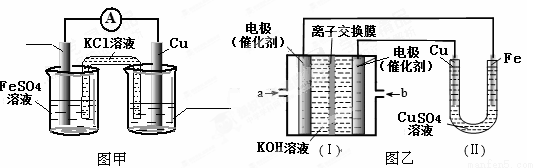
②图乙中,I是甲烷燃料电池的示意图,该同学想在II中实现铁上镀铜,则应在a处通入 (填“CH4”或“O2”),b处电极上发生的电极反应式为 ;若把II中电极均换为惰性电极,电解液换为含有0.1molNaCl溶液400mL,当阳极产生的气体为448mL(标准状况下)时,溶液的pH= (假设溶液体积变化忽略不计)。
(3)电池生产工业废水中常含有毒的Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去[室温下Ksp(FeS)=6.3×10-18mol2·L-2,K sp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后, 直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
sp(CuS)=1.3×10-36mol2·L-2]。请结合离子方程式说明上述除杂的原理:当把FeS加入工业废水中后, 直至FeS全部转化为CuS沉淀,从而除去溶液中Cu2+。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
下列对事实的解释或由事实所得结论中,正确的是
事实 | 解释或结论 | |
A | 常温下铁、铝均不溶于浓硫酸 | 常温下铁、铝与浓硫酸均不反应 |
B | 测定同浓度的Na2CO3溶液的pH小于Na2SiO3溶液的pH | 非金属性比较:C < Si |
C | 向某溶液中加入2滴KSCN浓液、溶液不显红色;再向溶液中加入几滴新制氯水,容液变为红色 | 该溶液中可能含有Fe2+ |
D | 用浓、稀HNO3分别完全溶解等质量的铜粉,参加反应的硝酸的物质的量比较:稀硝酸中的<浓硝酸中的 | 稀硝酸氧化性比浓HNO3强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com