
根据下表提供的数据,判断下列离子方程式或化学方程式正确的是
| 化学式 | 电离常数 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4×10-7 |
| K2=6×10-11 |
C
解析试题分析:依据电离常数分析可知酸性为H2CO3>HClO>HCO3-,酸性强的可以反应得到酸性弱的,据此分析判断;A、向Na2CO3溶液中滴加少量氯水,溶液中碳酸钠过量,盐酸和碳酸钠反应生成碳酸氢钠,次氯酸和碳酸钠反应生成碳酸氢钠和次氯酸钠,反应的离子方程式应为:2CO32-+2Cl2+H2O=2Cl-+ClO-+2HCO3-,故A错误;B、向NaHCO3溶液中滴加少量氯水,氯水中的盐酸和碳酸氢钠反应生成氯化钠、二氧化碳和水,次氯酸不能和碳酸氢钠反应,产物为次氯酸,反应的离子方程式为:HCO3-+Cl2=Cl-+HClO+CO2↑,故B错误;C、向NaClO溶液中通入少量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故C正确;D、向NaClO溶液中通入足量CO2反应生成碳酸氢钠和次氯酸,反应的化学方程式为:CO2+NaClO+H2O=NaHCO3+HClO,故D错误。
考点:考查弱电解质电离平衡常数的分析判断,主要是与碳酸钠反应的产物分析判断是解题关键。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:单选题
甲酸为一元弱酸,在15mL0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线。下面有关微粒浓度的大小关系正确的是
A.在A、B间的任意一点上都存在: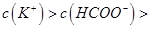

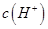
B.在B点:
 ,且a=7.5
,且a=7.5
C.在C点:
D.在D点:
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某学生用0.100 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
| A.移取20 mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞; |
| B.用标准溶液润洗滴定管2~3次; |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管使尖嘴处充满溶液; |
| D.取标准KOH溶液注入碱式滴定管至刻度“0”以上2~3 cm处; |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下,向0.1 mol·L-1 CH3COOH溶液中加少量水,下列有关说法错误的是( )
| A.溶液中所有离子的浓度都减小 | B.CH3COOH的电离程度变大 |
| C.水的电离程度变大 | D.溶液的pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
根据右下表数据,下列判断正确的是
| 物质 | HF | H3PO4 |
| 电离平 衡常数 | K= 3.6×10—4 | K1=" " 7.5×10—3 K2=" " 6.2×10—8 K3=" " 2.2×10—13 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列混合溶液在常温下的呈酸性 ( )
| A.相同浓度的CH3COOH和NaOH溶液等体积混合 |
| B.pH=2的HCl和pH=12的NaOH溶液等体积混合 |
| C.pH=3的HCl和pH=12的NaOH溶液等体积混合 |
| D.pH=2的CH3COOH和pH=12的NaOH溶液等体积混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关电解质溶液的叙述正确的是
| A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 |
| C.含1 mol KOH的溶液与1 mol CO2完全反应后,溶液中c(K+)=c(HCO) |
| D.在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
现有常温时pH=1的某强酸溶液10mL,下列操作能使溶液的pH变成2的是
| A.加入10mL 0.01mol·L-1的NaOH溶液 |
| B.加入10mL 的水进行稀释 |
| C.加水稀释成100mL |
| D.加入10mL 0.01mol·L-1的盐酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法中,正确的是
| A.25℃时,1L pH=3的盐酸和醋酸能消耗等质量的镁粉 |
| B.在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)将增大 |
| C.V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 |
| D.在0.1mol·L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32―离子浓度均增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com