
【题目】(1)用系统命名法命名下列有机物
①CH3CH(C2H5)CH(CH3)2 ________________________________________
②![]() ______________________________________________________
______________________________________________________
(2)写出下列物质的结构简式
①对二甲苯________________________________________
②2-甲基-1,3-丁二烯________________________________________
【答案】2,3-二甲基戊烷 2,4-二甲基-1-戊烯 ![]() CH2=C(CH3)CH=CH2
CH2=C(CH3)CH=CH2
【解析】
(1)①选取碳原子数最多的碳链为主链,主链为5个碳,即为戊烷,2、3位有甲基取代,因此命名为2,3-二甲基,合起来就是2,3-二甲基戊烷,故答案为:2,3-二甲基戊烷。
②选取含有碳碳双键的碳原子数最多的碳链为主链,主链为5个碳,即为戊烯,编号从双键最近一端开始,命名为2,4-二甲基-1-戊烯,故答案为:2,4-二甲基-1-戊烯。
(2)①对二甲苯的结构简式为:![]() ,故答案为:
,故答案为:![]() 。
。
②2-甲基-1,3-丁二烯,主链为1,3-丁二烯,在2号C含有1个甲基,该有机物的结构简式为:CH2=C(CH3)CH=CH2,故答案为:CH2=C(CH3)CH=CH2。


科目:高中化学 来源: 题型:
【题目】一种驱动潜艇的液氨-液氧燃料电池原理示意如图,下列有关该电池说法正确的是( )
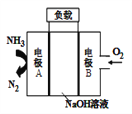
A. 电流由电极A经外电路流向电极B
B. 电池工作时,OH-向电极B移动
C. 该电池工作时,每消耗22.4L NH3转移3mol电子
D. 电极A上发生的电极反应为:2NH3-6e-+ 6OH-=N2 + 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) ![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
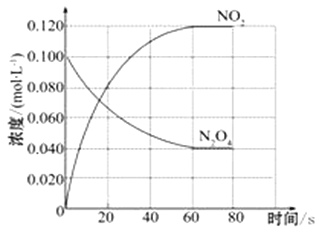
回答下列问题:
(1)反应的△H___________0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为_____________molL-1s-1,反应的平衡常数K1为______________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10 s又达到平衡。
① T __________100℃(填“大于”“小于”),判断理由是______________________________________;
② 温度T时反应的平衡常数K2 为 ___________________。
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向______________(填“正反应”或“逆反应”)方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列除杂方案正确的是( )
A.氢氧化钠溶液中混有氢氧化钡(硫酸铜溶液)
B.二氧化碳气体中混有氯化氢(氢氧化钠溶液)
C.硝酸铜溶液中混有硝酸银(铜粉)
D.氧化钙中混有碳酸钠(稀盐酸)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )。
A. 该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.乙烯和聚乙烯都能使溴的四氯化碳溶液褪色
D.液化石油气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,0.05 mol/L的硫酸溶液的pH=___,水电离出的c(H+)=___mol/L。
(2)在常温下,水电离出的c(H+)=1×10-13 mol·L-1的NaOH溶液中,pH=__________,c(NaOH)=_______mol·L-1。
(3)某温度下,纯水的c(H+)=2×10-7 mol·L-1,则此时纯水的c(OH-)为________。若温度不变,滴入稀盐酸使c(H+)=5×10-4 mol·L-1,则溶液中c(OH-)为________,此时温度________(填“高于”、“低于”或“等于”)25℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中正确的是
A. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
B. 小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O
C. NaHSO4溶液与Ba(OH)2溶液混合后呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D. 二氧化锰和浓盐酸共热:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分挟持装置已略去)进行实验:
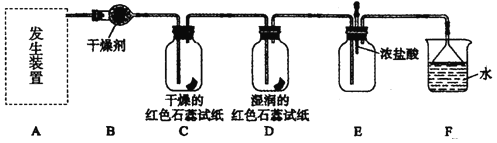
(1)写出实验室用固体制取氨气的化学方程式___________________________。
(2)利用上述原理,实验室制取氨气应选用下图中________发生装置进行实验。
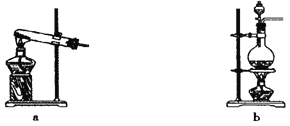
(3)B装置中的干燥剂可选用________(填“碱石灰”或“浓硫酸”)。
(4)气体通过C、D装置时,试纸颜色会发生变化的是________(填“C”或“D”),试纸颜色变为___________。
(5)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,发生的化学反应是____________可观察到的现象是____________。
(6)F装置的作用是____________,装置中倒扣的漏斗是为了_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com