
【题目】下列叙述正确的是( )
A. 分子晶体中都存在共价键
B. F2、C12、Br2、I2的熔沸点逐渐升高与分子间作用力有关
C. 氯元素含氧酸酸性 HClO > HClO2
D. 只要是离子化合物,其熔点一定比共价化合物的熔点高
科目:高中化学 来源: 题型:
【题目】(l)基态As原子的核外电子排布式为[Ar]______,有________个未成对电子。
(2) As与N是同主族元素,从原子结构角度分析:为什么As的最高价含氧酸H3AsO4是三元酸(含三个轻基),而N的最高价含氧酸HNO3是一元酸(只含一个烃基)______。
(3)比较下列氢化物的熔点和沸点,分析其变化规律及原因__________。
(4) Na3AsO3中Na、As、O电负性由大至小的顺序是______。AsO33-的空间构型为___, AsO33-中As的杂化轨道类型为_______杂化。
(5)砷化稼(GaAs)为黑灰色固体,熔点为1238℃。该晶体属于___晶体,微粒之间存在的作用力是_________。
NH3 | PH3 | AsH3 | SbH3 | |
熔点/K | 195.3 | 140.5 | 156.1 | 185 |
沸点/K | 239.6 | 185.6 | 210.5 | 254.6 |
(6)图为GaAs的晶胞,原子半径相对大小是符合事实的,则白球代表____原子。
己知GaAs的密度为5.307g·cm3, Ga和As的相对原子质量分别为69.72、74.92,求晶胞参数a=______pm (列出计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于钠元素的单质及其化合物的叙述错误的是( )
A.钠是银白色金属,氧化钠是白色粉末,过氧化钠是淡黄色粉末
B.大量的钠着火时可以用沙扑灭,不能用水或泡沫灭火剂灭火
C.金属钠在空气中长期放置,最终变为碳酸钠。
D.Na2O和Na2O2都能由金属钠和氧气化合生成,Na2O和Na2O2氧的价态也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分。表中所列的字母分别代表某一种化学元素。

下列说法正确的是( )
A. 沸点A2D<A2X
B. CA3分子是非极性分子
C. C形成的单质中σ键与π键个数之比为1∶2
D. B、C、D形成的气态氢化物互为等电子体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下的定容密闭容器中,当物质的下列物理量不再变化时,不能说明反应A(s) + 2B(g)![]() C(g) + D(g) 已达平衡状态的是
C(g) + D(g) 已达平衡状态的是
A. 混合气体的压强 B. 混合气体的密度
C. B的物质的量浓度 D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表中短周期的一部分,四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是 ( )

A. 原子半径:W>Z>Y>X
B. 气态氢化物的稳定性:Z>W>X>Y
C. W的最高正化合价与负化合价的绝对值可能相等
D. 若X位于第VA族,则沸点:XH3<WH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1 的醋酸溶液中存在电离平衡: CH3COOH![]() CH3COO-+H+,要使溶液中 c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
CH3COO-+H+,要使溶液中 c(H+)/c(CH3COOH)值增大,可以采取的措施是( )
A.加少量烧碱溶液 B.降低温度 C.加少量冰醋酸 D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能达到目的的是( )
A. 氯化铁溶液中滴加稀氨水制备氢氧化铁胶体
B. 将NH4Cl溶液蒸干制备NH4Cl固体
C. 用萃取分液的方法除去酒精中的水
D. 用可见光束照射以区别溶液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水。某小组在实验室中探究ClO2与Na2S的反应。回答下列问题:
(l)ClO2的制备:(已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4)

①装置A中反应的化学方程式为_______________。
②欲收集干燥的ClO2,选择上图中的装置,其连接顺序为 a→_________(按气流方向,用小写字母表示)
③装置D的作用是_________。
(2)ClO2与 Na2S 的反应
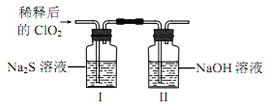
将上述收集到的ClO2用 N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
操作步骤 | 实验现象 | 结论 |
取少量Ⅰ中溶液于试管甲中, 加入Ba(OH)2溶液,振荡 | ①_________ | 有硫酸根离子生成 |
另取少量Ⅰ中溶液于试管乙中, 滴加品红溶液和盐酸 | 品红溶液不翅色 | ② 无_____生成 |
若在试管甲中继续加Ba(OH)2溶液至 过量,静置,取上层清液于试管丙③______ | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为__________。用于处理含硫废水时,ClO2相对于Cl2的优点是____________(任写2条)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com