
【题目】下列规律与化学反应的能量变化关系最大的是
A.阿伏加德罗定律 B.盖斯定律 C.勒夏特列原理 D.欧姆定律
科目:高中化学 来源: 题型:
【题目】最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:

下列说法中正确的是
A.CO和O生成CO2是吸热反应
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.增大反应物浓度可增大活化分子百分数,所以反应速率增大
B.放热反应的反应速率一定大于吸热反应的反应速率
C.反应NH3(g) + HCl(g)![]() NH4Cl(s)在室温下可自发进行,则该反应的△H<0
NH4Cl(s)在室温下可自发进行,则该反应的△H<0
D.对于反应X(s)+aY(g)![]() bZ(g)+W(g) △H>0,升高温度,正反应速率增大,逆反应速率减小
bZ(g)+W(g) △H>0,升高温度,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化中发生取代反应的是( )
A.苯与溴水混合,水层褪色
B.乙烯使溴的四氯化碳溶液褪色
C.甲苯制三硝基甲苯
D.苯和氯气在一定条件下生成六氯环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4 ℃,熔点9.79 ℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水)。
填写下列空白:
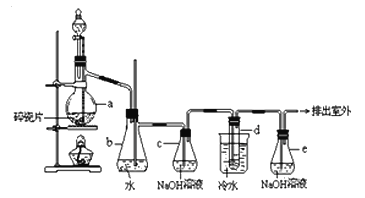
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式: 。
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是: 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氧化碳是一种用途相当广泛的化工基础原料。
⑴.利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍。
Ni(s)+4CO(g)![]() Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
Ni(CO)4(g)该反应的ΔH_______0(选填“>”或“=”或“<”)。
⑵.在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g);ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)=2CO(g);ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)=SO2(g);ΔH3=-296.0 kJ·mol-1
则2CO(g)+SO2(g)=S(s)+2CO2(g) ΔH4=________。
⑶.工业上一般采用CO与H2反应合成可再生能源甲醇,反应如下:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应达到平衡后,测
得c(CO)=0.2mol·L-1,则CO的转化率为___________。
合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,通过反应进行甲醇合成,T1℃下此反应的平衡常数为160。此温度下,在密闭容器中加入一定量CO和H2,反应到某时刻测得各组分的浓度如下:
物质 | H2 | CO | CH3OH |
浓度/(mol·L-1) | 0.2 | 0.1 | 0.4 |
比较此时正、逆反应速率的大小:v正_______v逆 (填“>”、“<”或“=”);若其他条件不变,在T2℃反应10min后达到平衡,c(H2)=0.4 mol·L-1,则该时间内反应速率:v(CH3OH)=__________;
(4)金属氧化物被一氧化碳还原生成金属单质和二氧化碳。下图是四种金属氧化物被一氧化碳还原时lg[c(CO)/c(CO2)]与温度(t)的关系曲线图。800℃时,其中最易被还原的金属氧化物是____(填化学式),该反应的平衡常数数值(K)等于____________。
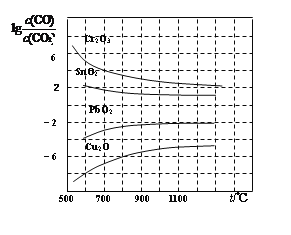
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物说法正确的是
A. 乙醇、乙烷和乙酸都可以与钠反应生成氢气
B. 75%(体积分数)的乙醇溶液常用于医疗消毒
C. 苯和乙烯都可使溴的四氯化碳溶液褪色
D. 石油分馏可获得乙酸、苯及其衍生物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2—叔丁基对苯二酚是一种重要的食品抗氧剂,现以对苯二酚、叔丁醇为原料,一定条件下经Freidel-Crafts 烷基化反应合成。原理如下:
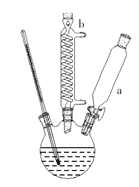
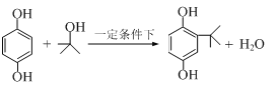
步骤Ⅰ:连接如右图所示装置。
步骤Ⅱ:向三颈烧瓶中加入4.0g 对苯二酚,15mL 浓磷酸,15mL甲苯,启动搅拌器,油浴加热混合液至90℃。从仪器a缓慢滴加 3.5mL叔丁醇,使反应温度维持在 90℃~95℃,并继续搅拌 15min 至固体完全溶解。
步骤Ⅲ:停止搅拌,撤去热浴,趁热转移反应液至分液漏斗中,将分液后的有机层转移到三颈烧瓶中,加入 45mL 水进行水蒸气蒸馏,至无油状物蒸出为止。
步骤Ⅳ:把残留的混合物趁热抽滤,滤液静置后有白色晶体析出,
最后用冷水浴充分冷却,抽滤,晶体用少量冷水洗涤两次,压紧、抽干。
⑴图中仪器a的名称为_____________;仪器b的作用是_____________。
⑵步骤Ⅱ中所加入物质中,有一种物质是催化剂,其化学式为_____________。
⑶已知:叔丁醇熔点是 25℃~26℃,常温下是固体。实验时加入叔丁醇的方法是
_____________。
⑷制备过程应严格控制反应温度90℃~95℃,其原因是_____________。
⑸2—叔丁基对苯二酚粗产品久置会变红,其原因是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知三种一元弱酸的酸性强弱 :HX>HY>HZ,则相同pH的NaX、NaY、NaZ溶液,其物质的量浓度由大到小的顺序正确的是
A.NaX、NaY、NaZ B.NaZ、NaY、NaX
C.NaY、NaZ、NaX D.NaX、NaZ、NaY
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com