
| A、用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中溶液全部加热蒸干 |
| B、蒸馏操作时,应将温度计水银球置于蒸馏烧瓶的支管口附近 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、使用容量瓶和分液漏斗前,要先检查是否漏水后使用 |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、硫原子的原子结构示意图: | ||
B、NH3分子的电子式: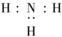 | ||
C、原子核内有8个中子的氧原子:
| ||
| D、氮气的结构式:N≡N |
查看答案和解析>>
科目:高中化学 来源: 题型:
 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应.反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的是( )| A、反应开始到第一次平衡时,N2的平均反应速率为 0.005mol/(L?min) |
| B、从曲线变化可以看出,反应进行到10min至20min时可能是使用了催化剂 |
| C、从曲线变化可以看出,反应进行至25min时,分离出0.1mol的氨气 |
| D、在25min时平衡正向移动,但达到新平衡后NH3的体积分数比原平衡小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16g O3与16g O2含有相同的氧原子数 |
| B、2.3g Na+中含有的电子数为0.1NA |
| C、1mol O2所含的原子数为NA |
| D、2.4g镁变为Mg2+时失去的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将0.2 mol?L-1的NH4Al(SO4)2溶液与0.3 mol?L-1的Ba(OH)2溶液等体积混合:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ |
| B、NH4HCO3溶液与足量Ba(OH)2溶液混合:HCO3-+Ba2++OH-═BaCO3↓+H2O |
| C、硫酸亚铁溶液与稀硫酸、双氧水混合:Fe2++H2O2+2H+=Fe3++2H2O |
| D、将大理石投入到足量盐酸中:CO32-+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、浓盐酸挥发,浓度不足 |
| B、配制溶液时,未洗涤烧杯 |
| C、配制溶液时,俯视容量瓶刻度线 |
| D、加水时超过刻度线,用胶头滴管吸出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com