
【题目】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe2+的核外电子排布式为_________________。
(2)NH3是一种很好的配体,NH3的沸点______(填“高于”“等于”或“低于”)AsH3。
(3)科学家通过X射线测得胆矾结构示意图可简单表示如下,图中虚线表示的作用力为________________。

(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈正四面体构型。Ni(CO)4易溶于________(填标号)。
A.水 B.四氯化碳 C.苯 D.硫酸镍溶液
(5)As的卤化物的熔点如下:
AsCl3 | AsBr3 | AsI3 | |
熔点/K | 256.8 | 304 | 413 |
表中卤化物熔点差异的原因是________________。
(6)向FeCl3溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表Fe3+,则Fe3+与氮原子之间形成的化学键是_________,Fe3+的配位数为_________。

【答案】 [Ar]3d6 高于 氢键、配位键 BC 对于组成和结构相似物质,相对分子质量逐渐增大,分子间作用力逐渐增强,熔点逐渐升高 配位键 6
【解析】(1). Fe是26号元素,失去2个电子生成Fe2+,Fe2+的核外电子排布式为:[Ar]3d6,故答案为:[Ar]3d6;
(2). NH3分子之间存在氢键,AsH3分子之间存在范德华力,氢键的作用强于范德华力,所以NH3的沸点高于AsH3,故答案为:高于;
(3). 据图可知,图中虚线表示的作用力有铜离子和O原子之间的配位键、氢原子和另一分子中的氧原子之间的氢键,故答案为:氢键、配位键;
(4). 金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,Ni(CO)4是液态挥发性物质,所以其熔点较低,为分子晶体,Ni(CO)4呈正四面体构型,是对称结构,所以是非极性物质,根据相似相溶原理可知,Ni(CO)4易溶于非极性溶剂,苯、四氯化碳是非极性物质,所以Ni(CO)4易溶于苯、四氯化碳,故答案为:BC;
(5). As的三种卤化物为组成和结构相似的分子晶体,对于组成和结构相似的分子晶体,相对分子质量越大,分子间作用力越强,熔点越高,故答案为:对于组成和结构相似物质,相对分子质量逐渐增大,分子间作用力逐渐增强,熔点逐渐升高;
(6). 据图可知,Fe3+提供空轨道,N原子提供孤电子对,Fe3+与氮原子之间形成的化学键是配位键,Fe3+的配位数为6,故答案为:配位键;6。


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
【题目】在一个密闭容器中,中间有一个可自由滑动的隔板,将容器分成两部分。当左边充入1molN2,右边充入8gCO和CO2的混合气体时,隔板处于如下图所示位置,V甲:V乙=4:1(两侧温度、压强均相同)。则混合气体中CO和CO2的物质的量比为( )

A. 1:1 B. 1:3 C. 3:1 D. 2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青海是我国最大的钾盐产地,某厂制得的钾盐(主要成分为KCl)混有MgCl2、CaCl2、K2SO4以及泥沙等杂质,以下是粗钾盐提纯的实验方案,各步操作流程如图,可以选用的试剂为:NaOH溶液、KOH溶液、Ba(OH)2溶液、HCl溶液、H2SO4溶液、HNO3溶液、Na2CO3溶液、K2CO3溶液

(1)过量Ca(OH)2的作用是除去溶液中的Mg2+,写出该反应的化学方程式___________。
(2)操作①和操作②都需用到玻璃棒,分别写出玻璃棒在操作①和操作②中的作用___________,_______________。
(3)试剂①、试剂②、试剂③分别为__________,____________,______________。若在操作②之前加入试剂③有什么后果___________________________________。
(4)若发现滤液浑浊,应如何操作___________________________________________。
(5)沉淀的成分有:泥沙、Mg(OH)2、BaSO4、CaCO3和_______________。
(6)除杂试剂需过量,但过量的试剂最后仍然要除去。过量的试剂③是如何除去的________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.1mol/LNH4HSO4溶液中滴加0.1mol/L的NaOH溶液,所得溶液pH与NaOH溶液体积的关系曲线如图所示,下列说法正确的是

A. a、b、c、d四个点中,水的电离程度最大的是d
B. 常温下,NH3·H2O的电离平衡常数Kb=5×10-6
C. b点溶液中:c(Na+)+c(NH4+)=c(SO42—)
D. c点溶液中:3c(Na+)= 4[c(SO42—) +c(NH4+)+ c(NH3·H2O)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
AlN 氮化铝是重要的半导体材料,Ga(镓)、P、As(砷)都是形成化合物半导体材料的重要元素。回答下列问题:
(1)As基态原子的电子占据了______个能层,最高能级的电子排布式为______。和As位于同一周期,且未成对电子数也相同的元素还有______种。
(2)元素周期表中,与P紧邻的4种元素中电负性最大的是______ (填元案符号)。Si、P、S三种元素的 第一电离能由大到小的顺序是______。
(3)NH3、PH3、AsH3三者的沸点由高到低的顺序是______。原因是______。
(4)白磷是由P4分子形成的分子晶体,P4分子呈正四面体结构,P原子位于正四面体的四个顶点,则P原子的杂化形式为_____,白磷易溶于CS2,难溶于水,原因是__________________。
(5)采用GaxIn1-xAs(镓铟砷)等材料,可提高太阳能电池的效率。GaxIn1-xAs立方体形晶胞中每个顶点和面心都有一个原子,晶胞内部有4 个原子,则该晶胞中含有_________个砷原子。
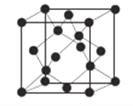
(6)AlN晶体的晶胞结构与金刚石相似(见下图),设晶胞的边长为ɑ pm,NA表示阿伏加德罗常数,则该晶体的密度为__________g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水得到的粗食盐水中常含Ca2+、Mg2+、SO42-,需要分离提纯。现有含少量CaCl2、MgSO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂:①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的Ca2+、Mg2+、SO42-。提纯时的操作步骤和加入试剂的情况如图。

图中a、b、c、d分别表示上述4种试剂中的一种,请回答:
(1)沉淀A的名称是________。
(2)试剂d是________;判断试剂d已经足量的方法是__________________________。
(3)加入b、c后溶液中发生的化学反应的化学方程式有______________________(任写两个)。
(4)现有下列仪器,过滤出沉淀A、B、C时必须用到的是____(填序号),仪器③的名称是_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程,属于放热反应的是( )
①水蒸气变成液态水 ②酸碱中和反应 ③浓硫酸稀释 ④碳与二氧化碳化合 ⑤H2在Cl2中燃烧 ⑥氯化钠电离
A.②③④⑤B.②③④C.②⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们的衣、食、住、行均与化学有密切密切的联系。
(1)服装面料种类繁多。下列面料中不属于天然纤维的是__________(填序号)。
a、棉和麻 b、丝和毛 c、涤纶和锦纶
(2)营养均衡有利于身体健康。
①为人体提供能量的主要营养物质是糖类、____________和蛋白质。
②蛋白质是构成人体细胞的基础物质。下列食品中富含蛋白质的是_________(填序号)。
a、香蕉 b、牛奶 c、花生油 d、马铃薯
③维生素是人体需要的营养物质。下图为某品牌维生素C泡腾片说明书的部分内容。该泡腾片中添加的着色剂是___________,甜味剂是___________。

(3)居室环境污染严重危害我们的健康。装修材料挥发出的___________(写名称)和苯是常见的环境污染物。存在于石料中的氡因为具有___________性,也是居室环境污染物之一。
(4)汽车和飞机是重要的交通工具,制造其轮胎的主要材料是__________(填序号)。
a、塑料 b、橡胶 c、玻璃钢 d、钛合金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com