
【题目】图1表示的是某同学通过实验得出的H2O2浓度与酶促反应速率关系图,图2是实验过程中的一个装置图.请分析回答下列问题:
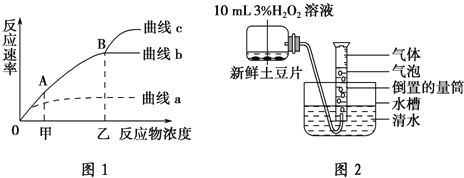
(1)图1中AB段说明反应速率大小主要与 有关,对应图2中的实验装置如何设计 .
(2)如果图2装置中放入的是经高温处理过的土豆片,实验现象是 ,原因是 .
(3)实验过程中温度、pH等保持不变,形成曲线a与曲线b差异的可能原因是 ;将图2装置中含有新鲜土豆片的烧瓶分别放置在不同温度的水浴锅中,定时记录不同温度条件下产生的气体量,绘制出的温度对H2O2酶酶促反应速率影响的曲线图不够科学,其原因是 .
(4)曲线b在B点后反应速率不再增加的原因是 ,曲线C形成的可能原因是 .
【答案】(1)H2O2浓度 改变图2装置中10mLH2O2的浓度,其它不变
(2)产生的气泡很少 高温处理后,H2O2酶失活
(3)土豆片的数量 温度会影响H2O2自身分解的速率
(4)受H2O2酶浓度的限制 增加土豆片的数量
【解析】
试题分析:本题主要考查酶的知识.
1、酶是由活细胞产生的具有催化活性的有机物,其中大部分是蛋白质、少量是RNA.
2、酶的特性.①高效性:酶的催化效率大约是无机催化剂的107~1013倍.
②专一性:每一种酶只能催化一种或者一类化学反应.
③酶的作用条件较温和:在最适宜的温度和pH条件下,酶的活性最高;温度和pH偏高或偏低,酶的活性都会明显降低.
解:(1)根据图1的曲线图可知,图1中AB段说明反应速率大小主要与H2O2浓度有关,对应图2中的实验装置应改变其中10mLH2O2的浓度,其它不变.
(2)如果图2装置中放入的是经高温处理过的土豆片,由于高温处理后,H2O2酶失活,故产生的气泡很少.
(3)实验过程中温度、pH等保持不变,形成曲线a与曲线b差异的可能原因是H2O2酶的数量,即土豆片的数量.因为温度会影响H2O2自身分解的速率,所以绘制出的温度对H2O2酶酶促反应速率影响的曲线图不够科学.
(4)曲线b在B点后受H2O2酶浓度的限制,反应速率不再增加.在B点增加H2O2酶的数量,即增加土豆片的数量,反应速率加快,形成曲线C.
故答案为:(1)H2O2浓度 改变图2装置中10mLH2O2的浓度,其它不变
(2)产生的气泡很少 高温处理后,H2O2酶失活
(3)土豆片的数量 温度会影响H2O2自身分解的速率
(4)受H2O2酶浓度的限制 增加土豆片的数量


科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列判断正确的是
A. 高温下,5.6 g Fe与足量水蒸气反应,转移的电子数为0.3NA
B. 标准状况下,22.4 L NO和11.2 L O2充分反应,产物的分子数为NA
C. 60g乙酸与足量乙醇发生酯化反应,充分反应后断裂的C-O键数目为NA
D. 向含有0.2 mol NH4Al(SO4)2的溶液中滴加NaOH 溶液至沉淀恰好完全溶解,所消耗OH-的数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述正确的是( )
A.乙烷中若混有乙烯,可通过酸性高锰酸钾溶液除去
B.乙醇中是否混有水,可用加入金属钠是否产生气体进行检验
C.蚕丝和棉花的组成元素相同,分子结构不同,因而性质不同
D.乙酸乙酯是否混有乙酸,可用加石蕊试液是否变红进行检测
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氯气和液氯是两种不同的物质
B. NH3是电解质,所以氨水能导电
C. 氨不能用浓硫酸干燥,但可以用无水CaCl2干燥
D. 新制的氯水呈酸性,向其中滴加几滴紫色石蕊试液并振荡,溶液先变红后褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法错误的是
A. Fe2O3 可用于制红色油漆 B. 碳酸钠可用于中和过多胃酸
C. 碳化硅硬度大,可用作砂纸、砂轮的磨料 D. Na2O2 可用于呼吸面具的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠是生活必需品,也是重要的化工原料.提纯含少量泥沙的粗盐,一般经过以下操作流程: 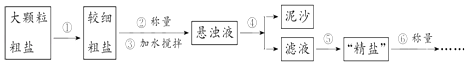
(1)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是 .
(2)实验结束后称量获得的“精盐”,并计算“精盐”的制得率,发现制得率较低,其可能原因是(填序号).
A.粗盐没有全部溶解即过滤
B.蒸发时液滴飞溅剧烈
C.蒸发后所得“精盐”很潮湿
D.蒸发皿上粘有的“精盐”没有全部转移到称量纸上
(3)小明查阅相关资料得知:粗盐中除含泥沙等不溶性杂质外,还含有少量的MgCl2、CaCl2等可溶性杂质.为了得到较纯净的氯化钠,小明将上述流程图中操作⑤得到的“精盐”又作了如下处理(假定杂质只有MgCl2、CaCl2两种). 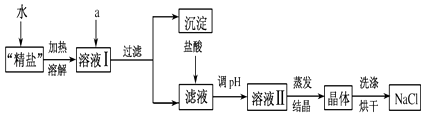
①提供的试剂:Na2CO3溶液、K2CO3溶液、NaOH溶液、KOH溶液、饱和NaCl溶液.
从提供的试剂中选出a所代表的试剂是、 , 写出发生反应的离子方程式 , .
②在滤液中加盐酸的作用是、(用化学方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案正确的是
A. 用酒精萃取碘水中的碘
B. 将 NO2 和 NO 混合气体通入足量水中,可除去混合气体中的 NO2
C. 用蒸馏操作分离四氯化碳和水
D. 为除去 FeCl2 溶液的 FeCl3 杂质,可向溶液中加入足量铜粉,过滤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com