
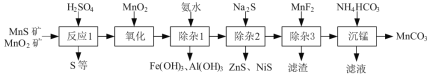
【题目】(一种由天然MnO2矿与MnS矿(还含Fe、Al、Mg、Zn、Ni、Si等元素的氧化物)制备高纯碳酸锰工艺如下:
已知:相关金属离子形成氢氧化物沉淀的pH范围如下:
金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
⑴“反应1”中MnO2与MnS反应的化学方程式为______。
⑵“反应1”后所得沉淀物中除S外,一定还含有的氧化物是______(填化学式)。
⑶“除杂2”后溶液中c(Zn2+)=1×105 mol·L1,则溶液中c(Ni2+)=______mol·L1。[已知:Ksp(ZnS)=2×1022,Ksp(NiS)=1×1024]
⑷“滤渣”的成分为______(填化学式);“滤液”中所含溶质的主要成分为___(填化学式)。
⑸将部分MnCO3溶于稀硫酸,所得溶液电解可制得MnO2循环使用。写出电解时所发生反应的离子方程式:______。
【答案】MnO2+MnS+2H2SO4=2MnSO4+S+2H2O SiO2 5×10-8 MgF2 Na2SO4、(NH4)2SO4 Mn2++2H2O ![]() MnO2↓+ 2H++H2↑
MnO2↓+ 2H++H2↑
【解析】
根据流程:二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)在硫酸中酸浸,主要的反应为:MnO2+MnS+2H2SO4=2MnSO4+S+2H2O,SiO2不溶于硫酸,过滤,得到的固体含有S和SiO2,滤液含有Mn2+、Fe2+、Fe3+、Al3+、Mg2+、Zn2+、Ni2+,加入MnO2将Fe2+氧化为Fe3+,加入氨水调节pH4.7~6之间,除去Fe3+、Al3+,除杂1为Fe(OH)3、Al(OH)3,滤液中加入Na2S除去Zn2+和Ni2+,除杂2的主要成分是NiS和ZnS,加入MnF2生成MgF2沉淀除去Mg2+,除杂3的滤渣为MgF2,加入碳酸氢铵发生反应:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O,沉锰后滤液主要含有Na2SO4、(NH4)2SO4。
(1) “反应1”中二氧化锰与硫化锰反应为:MnO2+MnS+2H2SO4=2MnSO4+S+2H2O,
答案为:MnO2+MnS+2H2SO4=2MnSO4+S+2H2O;
⑵Si元素以SiO2的形式存在,SiO2不溶于硫酸, “反应1”后所得沉淀物中除S外,一定还含有的氧化物是SiO2,
答案为:SiO2;
⑶“除杂2”后溶液中c(Zn2+)=1×105 mol·L1,则c(S2-)=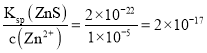 ,
,
c(Ni2+)=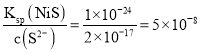 ,
,
答案为:5×10-8;
⑷根据分析,加入MnF2生成MgF2沉淀除去Mg2+,除杂3的滤渣为MgF2,加入碳酸氢铵发生反应:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O,沉锰后滤液主要含有Na2SO4、(NH4)2SO4,
答案为:MgF2;Na2SO4、(NH4)2SO4;
⑸将部分MnCO3溶于稀硫酸,得硫酸锰溶液,电解可制得MnO2,电解时所发生反应的离子方程式:Mn2++2H2O ![]() MnO2↓+ 2H++H2↑。
MnO2↓+ 2H++H2↑。
答案为:Mn2++2H2O ![]() MnO2↓+ 2H++H2↑。
MnO2↓+ 2H++H2↑。


科目:高中化学 来源: 题型:
【题目】重要的精细化学品M和N,常用作交联剂、涂料、杀虫剂等,合成路线如图1所示:
图1:
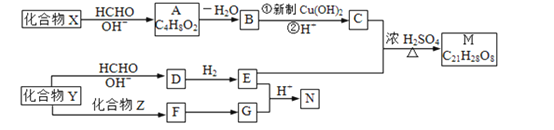
已知:i、-CHO+![]()
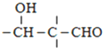
ii、RCHO+![]()
![]()
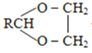 +H2O
+H2O
iii、N的结构简式是
请回答下列问题:
(1)A中含氧官能团名称是______________,由A生成B的反应类型是___________。
(2)写出下列物质的结构简式:X:_________Z:______________E:______
(3)C和甲醇反应的产物可以聚合形成有机玻璃,该聚合反应的化学方程式是:____。
(4)G中碳原子________(填“一定”、“不一定”或“一定不”)在同一平面内;1mol G一定条件下,最多能与________mol H2发生反应;与G含有相同官能团的同分异构体(不包含G)有___________种。
(5)由Y生成D的化学方程式是________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向10mL0.1 mol/L CuCl2溶液中滴加0.1 mol/L Na2S溶液滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法错误的是( )

A. 该温度下Ksp(CuS)=10-35.4
B. 曲线上各点的溶液均满足关系式c(S2-)·c(Cu2+)=Ksp(CuS)
C. Na2S溶液中C(S2-)+C(HS-)+C(H2S)=2C(Na+)
D. c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是

选项 | x | y |
A | 温度 | 容器内混合气体的密度 |
B | CO的物质的量 | CO2与CO的物质的量之比 |
C | SO2的浓度 | 平衡常数K |
D | MgSO4的质量(忽略体积) | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是

A. 正极反应式:Ca + 2Cl--2e- = CaCl2
B. 放电过程中,Li+向负极移动
C. 没转移0.1mol电子,理论上生成20.7 g Pb
D. 常温时,在正负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体粉末 X 中可能含有 Fe2O3、CuO、MnO2、CaO、NaCl 和 K2CO3 中的若干种。为确定该固体粉末的成分,进行了以下实验(所加试剂均过量):
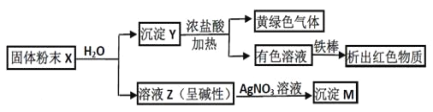
下列结论正确的是:
A. 固体粉末中一定含 K2CO3B. X 中可能存在 Fe2O3
C. 沉淀 M 一定含 AgClD. 沉淀 Y 中不一定存在 MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是

A.图1表示镁条与盐酸反应的能量变化
B.图2表示H2SO4溶液中滴入BaCl2溶液后,溶液的导电性随BaCl2物质的量的变化
C.图3表示电解精炼铜时,溶液中Cu2+的物质的量浓度随转移电子物质的量的变化
D.图4表示其他条件一定,反应2SO2+O2![]() 2SO3在有、无催化剂情况下SO2的体积分数随时间的变化
2SO3在有、无催化剂情况下SO2的体积分数随时间的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某食用香料乙酸橙花酯的结构简式如图所示,则关于该有机物叙述中正确的个数是( )

①分子式为C12H20O2 ②它的同分异构体中有芳香族化合物 ③能使酸性KMnO4溶液褪色 ④1mol该有机物在一定条件下能和3mol H2反应 ⑤密度比水小 ⑥1mol该有机物水解时能消耗1molNaOH⑦能在一定条件下生成高分子化合物
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素符号、结构示意图、电子式、结构式等通常叫做化学用语,下列化学用语错误的是( )
A.CO2分子的电子式为:![]()
B.NaOH的电子式为:![]()
C.Cl-的结构示意图为: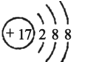
D.HClO的结构式为:H-Cl-O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com