

分析 (1)依据容量瓶构造解答;
(2)依据配制一定物质的量浓度溶液配制步骤选择需要仪器并判断操作正误;
(3)试剂瓶标签上应注明浓度和药品名称;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
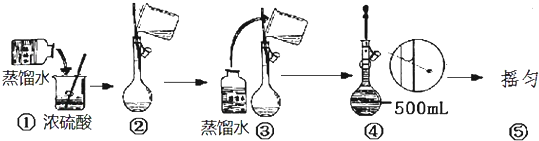
解答 解:(1)容量瓶为配制一定物质的量浓度专用仪器,容量瓶上标有:温度、容积、刻度线,
故选:BCE;
(2)配制一定物质的量浓度溶液配制步骤:计算、量取、稀释、移液、洗涤、定容、摇匀等,需要仪器:量筒、胶头滴管、烧杯、玻璃棒和500mL容量瓶,所以还缺少的仪器:500mL容量瓶;
浓硫酸稀释应将浓硫酸沿着烧杯壁缓缓注入水中,故①错误;
定容时,应平时刻度线,故④错误;
所以错误的操作为:①④;
故答案为:500mL容量瓶;①④;
(3)试剂瓶标签上应注明溶液的物质的量浓度和物质名称,所以盛放500mL0.4mol?L-1Na2CO3溶液的试剂瓶标签应注明0.4mol?L-1 Na2CO3溶液,
故答案为: ;
;
(4)A.定容时,俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故A不选;
B.NaOH 溶解后趁热移入容量瓶中,冷却后溶液体积偏小,溶液浓度偏高,故B不选;
C.容量瓶用蒸馏水洗净后,未待干燥便用来配制,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度不变,故C不选;
D.摇匀后发现液面未到刻度线,继续加水至刻度线,导致溶液体积偏大,溶液浓度偏低,故D选;
故选:D.
点评 本题考查配制一定物质的量浓度的溶液及误差分析,明确配制原理及操作步骤是解题关键,注意容量瓶构造及使用方法和注意事项,注意误差分析的方法和技巧,题目难度不大.


科目:高中化学 来源: 题型:选择题
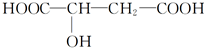 .苹果酸可能发生的反应是( )
.苹果酸可能发生的反应是( )| A. | 只有①②③ | B. | 只有②③④ | C. | 只有①②⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2Br-CH2Br 二溴乙烷 | B. | CH3OOCCH3乙酸甲酯 | ||
| C. |  硬脂酸甘油脂 硬脂酸甘油脂 | D. | 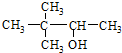 2,2-二甲基-3-丁醇 2,2-二甲基-3-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+
,所含化学键的类型离子键和极性共价键;D、E的最高价氧化物对应水化物发生反应的离子方程式Al(OH)3+OH-=AlO2-+2H2O用电子式表示BA3的形成过程3H•+ →
→ ,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图
,A、C形成的化合物中,C的质量分数最高的化合物的结构式H-O-O-H,C2-的离子结构示意图 ,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T
,A有多种同位素,其中一种同位素原子核内有两个中子,这种同位素原子的表示方法31H或T查看答案和解析>>
科目:高中化学 来源: 题型:解答题
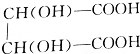 +2NaOH=
+2NaOH=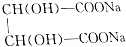 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
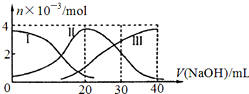
| A. | H2 A在水中的电离方程式是:H2A=H ++HA -;HA -═H++A2- | |
| B. | 当V(NaOH)=20mL时,则有:c(Na + )>c(HA- )>c(H + )>c(A 2- )>c(OH- ) | |
| C. | 当V(NaOH)=30mL时,则有:2c(H + )+c(HA- )+2c(H2A)=c(A 2- )+2 c(OH- ) | |
| D. | 当V(NaOH)=40mL时,其溶液中水的电离受到抑制 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com