
����Ŀ������Cu2O�������Ĵ����Ͱ뵼����ϣ���ҵ�ϳ������з����Ʊ�Cu2O��
��1���Ȼ�ԭ��
���������£���Һ̬�£�N2H4����ԭ���Ƶ�Cu(OH��2�Ʊ�Cu2O��ͬʱ�ų�N2���÷�Ӧ�Ļ�ѧ����ʽΪ________________��
��2����ⷨ ������ȼ�ϵ��Ϊ��Դ���õ�ⷨ�Ʊ�Cu2O��װ����ͼ��
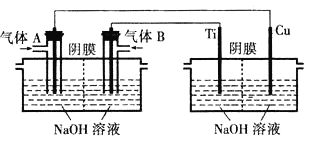
��A�Ļ�ѧʽΪ________________��
��ȼ�ϵ���У�OH-���ƶ�����Ϊ________________���������������������������������������У������ĵ缫��ӦʽΪ________________��
�����һ��ʱ�����ʹ��������Һ�ָ�ԭ����ɣ�Ӧ�����в���һ����________________(�ѧʽ����
���Ʊ������У���ѭ�����õ�����Ϊ________________���ѧʽ����
��3���ɷ���ԭ��
���÷�ӦCu +CuO![]() Cu2O�Ʊ�Cu2O������Ӧ��ľ��ȹ�������������ֳɷ֣��ȷ�Ϊ���ݣ�һ��������H2��ַ�Ӧ������������6.4g����һ��ǡ������500mLϡ���ᣬ���ɱ�״����4.48LNO����ϡ��������ʵ���Ũ��Ϊ________��
Cu2O�Ʊ�Cu2O������Ӧ��ľ��ȹ�������������ֳɷ֣��ȷ�Ϊ���ݣ�һ��������H2��ַ�Ӧ������������6.4g����һ��ǡ������500mLϡ���ᣬ���ɱ�״����4.48LNO����ϡ��������ʵ���Ũ��Ϊ________��
���𰸡�4Cu (OH��2+N2H4![]() N2+2Cu2O+6H2O O2 �������� 2Cu+2OH--2e-=Cu2O+H2O H2O H2 3.2mol/L
N2+2Cu2O+6H2O O2 �������� 2Cu+2OH--2e-=Cu2O+H2O H2O H2 3.2mol/L
��������
��1���ڼ��������£���Һ̬�£�N2H4����ԭ���Ƶ�Cu(OH��2�Ʊ�Cu2O��ͬʱ�ų�N2������ԭ���غ㡢�����غ�ɵø÷�Ӧ�Ļ�ѧ����ʽΪ4Cu(OH��2+N2H4![]() N2+2Cu2O+6H2O����2����������ȼ�ϵ��Ϊ��Դ���õ�ⷨ�Ʊ�Cu2O����Cu�缫���Դ���������ӣ���ȼ�ϵ��ͨ�����ļ�Ϊ������ͨ�������ĵ缫Ϊ���������Կ�֪����AΪ������A�Ļ�ѧʽΪO2 ��
N2+2Cu2O+6H2O����2����������ȼ�ϵ��Ϊ��Դ���õ�ⷨ�Ʊ�Cu2O����Cu�缫���Դ���������ӣ���ȼ�ϵ��ͨ�����ļ�Ϊ������ͨ�������ĵ缫Ϊ���������Կ�֪����AΪ������A�Ļ�ѧʽΪO2 ��
������ͬ�ֵ����ų⣬���ֵ���������ԭ����ԭ��������������ƶ�����ȼ�ϵ����OH-���ƶ�����Ϊ���������ƶ����ڵ�����������ͭ����������Cu+��Ȼ������Һ�е�OH-����γ�Cu2O���缫��ӦʽΪ2Cu+ 2OH-- 2e-=Cu2O+H2O��
�������ڷ������ܷ�ӦʽΪ2Cu+H2O![]() Cu2O+H2������֪����Һ�м�����ˮ����ɣ�����Ҫ�����������ˮ����ѧʽ��H2O��
Cu2O+H2������֪����Һ�м�����ˮ����ɣ�����Ҫ�����������ˮ����ѧʽ��H2O��
�����������õ��������ɲ���ȼ�ϵ���У���Ϊȼ�����ĵ��������ɼ���ѭ��������ΪH2�� ��3�� ��Cu2O���ΪCu��CuO��ԭ������Cu��CuO�Ļ����,��һ�ݻ������������������ԭ���õ�Cu��ˮ����Ӧ�������������6.40gΪ�������OԪ�ص�������Oԭ�ӵ����ʵ���Ϊn(O)=6.4g��16g/mol=0.4mol������CuԪ���غ��֪n(CuO��= n(O)=0.4mol����һ���м���500mLϡ���ᣬ����ǡ����ȫ�ܽ⣬��Һ������ΪCu(NO3)2����ͬʱ�ռ�����״����NO����4.48L��NO�����ʵ���Ϊn(NO��=4.48L��22.4L/mol=0.2mol�����ݵ���ת���غ��֪�ڲ�ֺ�Cu��CuO�Ļ������,2n(Cu��=3n(NO��=3��0.2mol��n (Cu��=0.3mol����ͭԪ���غ��֪n[Cu(NO3)2]=n��CuO��+n��Cu��=0.4mol+0.3mol=0.7mol�����ݵ�Ԫ���غ��֪n(HNO3)= n(NO)+2 n[Cu(NO3)2] =0.2mol+2��0.7mol=1.6mol�������Ũ��Ϊ1.6mol��0.5L=3.2 mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���M���л��ϳɵ���Ҫ�м��壬�Ʊ�M��һ�ֺϳ�·������(���ַ�Ӧ�������Լ���ȥ)��

��֪����A���ܶ�����ͬ������H2�ܶȵ�38��������ӵĺ˴Ź�����������3��壻
�� (-NH2���ױ�����)��
(-NH2���ױ�����)��
�� R-CH2COOH
R-CH2COOH
��ش��������⣺
(1)B�Ļ�ѧ����Ϊ______��A�й����ŵĵ���ʽΪ______��
(2)C![]() D�ķ�Ӧ������______��I�Ľṹ��ʽΪ______��
D�ķ�Ӧ������______��I�Ľṹ��ʽΪ______��
(3)F![]() G�Ļ�ѧ����ʽΪ______��
G�Ļ�ѧ����ʽΪ______��
(4)M�����ܷ����ķ�ӦΪ______(��ѡ����ĸ)��
a.�ӳɷ�Ӧ b.������Ӧ c.ȡ����Ӧ d.��ȥ��Ӧ
(5)��д������������������������E��ͬ���칹����______��
������FeCl3��Һ������ɫ��Ӧ ������NaHCO3��Ӧ �ۺ���-NH2
(6)���������ϳ�·�ߣ���![]() Ϊԭ��(���Լ���ѡ)������Ʊ�
Ϊԭ��(���Լ���ѡ)������Ʊ�![]() �ĺϳ�·�ߣ�______��
�ĺϳ�·�ߣ�______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.1 mol��L��1 CH3COOH��Һ�д������µ���ƽ�⣺ CH3COOH ![]() CH3COO����H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
CH3COO����H+�����ڸ�ƽ�⣬����������ȷ���ǣ� ��
A. ����ˮʱ��ƽ�����淴Ӧ�����ƶ�
B. ��������NaOH���壬ƽ��������Ӧ�����ƶ�
C. ��������0.1 mol��L��1 HCl��Һ����Һ��c(H+)��С
D. ��������CH3COONa���壬ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(H2NNH2)��һ�ָ���ȼ�ϣ��йػ�ѧ��Ӧ�������仯����ͼ��ʾ����֪����1 mol��ѧ�����������(kJ)��N��NΪ942��O=OΪ500��N��NΪ154�������1 mol N��H�����������(kJ)�ǣ�

A. 194 B. 391 C. 516 D. 658
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����е�ͼʾ���Ӧ������������ǣ� ��
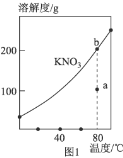
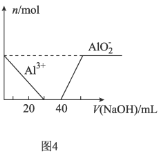
A.ͼ1��ʾ![]() ���ܽ�����ߣ�ͼ��a���ʾ����Һͨ�����¿��Եõ�b��
���ܽ�����ߣ�ͼ��a���ʾ����Һͨ�����¿��Եõ�b��
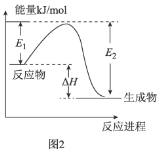
B.ͼ2��ʾijһ���ȷ�Ӧ����ʹ�ô���![]() ��
��![]() ��
��![]() ���ᷢ���ı�
���ᷢ���ı�
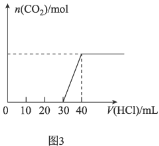
C.ͼ3��ʾ��![]() ��
��![]() �Ļ����Һ�еμ�ϡ����ʱ������
�Ļ����Һ�еμ�ϡ����ʱ������![]() �����
�����
D.ͼ4��ʾ��![]() ��
��![]() ��
��![]() ��
��![]() �����Һ�еμ�
�����Һ�еμ�![]() ��
��![]() ��Һʱ
��Һʱ![]() ��
��![]() �ı仯���
�ı仯���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ӵ���ֳ�Ϊ��ҡ�ڵ�������㷺ʹ���ڵ綯���г��ȣ����ŵ���̾�������ӵ�Ƕ�����Ƕ����(ϰ����������Ƕ�����Ƕ��ʾ�������ò�����Ѳ��ʾ)������ŵ���̾�������������������������˶����γɵ�������װ�ýṹ��ͼ��ͼ��ʾ(���ҺΪ����LiPF6��̼�������ܼ�����ĤΪ�����������ͨ���ĸ߷���Ĥ)������ԭ��ΪC6Li��Li(1��x)MO2![]() LiMO2��C6Li(1��x)(M��������Ԫ��)��������˵���������(����)
LiMO2��C6Li(1��x)(M��������Ԫ��)��������˵���������(����)
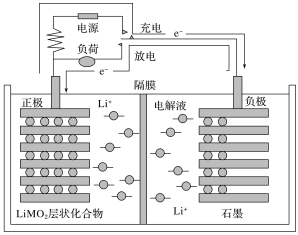
A.��طŵ�ʱ������Ϊʯī
B.����ӵ�ص��ŵ�������С�����������ظ����ʹ��
C.��س��ʱ�����ķ�ӦΪLiMO2��xe��=Li(1��x)MO2��xLi��
D.����ӵ�صĵ��Һ������ˮ��Һ����Ϊ��ǻ��ý���������ˮ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
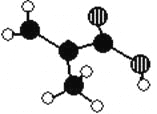
����Ŀ��ij������������ij��Ʒֻ��C��H��O����Ԫ�أ������ģ������ͼ��ʾ��ͼ��������֮������ߴ�����ѧ�����絥����˫���ȣ���
��1���ò�Ʒ�Ľṹ��ʽΪ__________________________��
��1H�˴Ź�������֤���û�����ĺ˴Ź�����������_______�����շ塣
��2�����������У���ò�Ʒ��Ϊͬ���칹�����_____________������ţ�����ò�Ʒ��Ϊͬϵ�����_____________������ţ���
��CH3CH=CHCOOH �� CH2=CHCOOCH3 ��CH3CH2CH=CHCOOH �� CH3CH(CH3)COOH
��3����һ�������£��ò�Ʒ���Ҷ�����Ӧ�ɵõ�����ʽΪC6H10O3�����ʣ������ʷ����Ӿ۷�Ӧ�ɵõ��������������۾��ĸ߷��Ӳ��ϣ���д�����ָ߾���Ľṹ��ʽ��
____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾװ�ó�ȥ��CN����Cl����ˮ�е�CN��ʱ��������ҺPHΪ9~10������������ClO����CN������Ϊ��������Ⱦ�����壬����˵������ȷ����

A. ��ʯī����������������
B. �����ĵ缫��ӦʽΪ��Cl�� + 2OH����2e��= ClO�� + H2O
C. �����ĵ缫��ӦʽΪ��2H2O + 2e�� = H2�� + 2OH��
D. ��ȥCN���ķ�Ӧ��2CN��+ 5ClO�� + 2H+ = N2�� + 2CO2�� + 5Cl��+ H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֦������������о�����ṹ��ʽ������ʾ�����й��ڷ�֦���������ȷ����

A�������к���2�ֹ�����
B�������Ҵ������ᷴӦ���ҷ�Ӧ������ͬ
C��1 mol��֦������к�2mol��OH���ǻ���
D����ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ����ԭ����ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com