
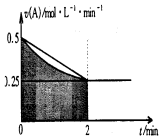
| A. | 0-2min,速率不断减少的主要原因是A的浓度减少 | |
| B. | 反应开始前2min,C的浓度增加量等于A的浓度减少量 | |
| C. | 至2min时,A的物质的量减小值可能是0.5mol | |
| D. | 至2min时,c(B)介于1mol•L-1 至1.5mol•L-1 之间 |
分析 根据图象可知,阴影部分的面积△c(A)的范围为:0.25 mol?L-1?min-1×2min=0.5mol?L-1<△c(A)<0.25 mol?L-1?min-1×2min+$\frac{1}{2}$×0.25 mol?L-1?min-1×2min=0.75mol?L-1;
A.浓度越小化学反应速率越小;
B.同一可逆反应中同一段时间内各物质的浓度变化量之比等于其计量数之比;
C.图中阴影部分的面积表示0~2min内A的物质的量浓度的减小值,不是物质的量的减小值;
D.根据A的浓度变化及反应方程式计算出B的浓度变化.
解答 解:根据图象可知,阴影部分的面积△c(A)的范围为:0.25 mol?L-1?min-1×2min=0.5mol?L-1<△c(A)<0.25 mol?L-1?min-1×2min+$\frac{1}{2}$×0.25 mol?L-1?min-1×2min=0.75mol?L-1;
A.浓度越小化学反应速率越小,随着反应的进行,A浓度逐渐减小,则化学反应速率逐渐减小,故A正确;
B.同一可逆反应中同一段时间内各物质的浓度变化量之比等于其计量数之比,A、C的计量数相等,则反应开始前2min,二者的浓度变化量之比等于其计量数之比为1:1,所以C的浓度增加量等于A的浓度减少量,故B正确;
C.图中阴影部分的面积表示0~2min内A的物质的量浓度的减小值,不是物质的量的减小值,故C错误;
D.物质的量变化与化学计量数成正比,则2min时,B的物质的量浓度c(B)介于:0.5mol/L×2=1mol/L~0.75mol/L×2=1.5mol/L之间,故D正确;
故选C.
点评 本题考查了化学反应速率的变化曲线及其应用,题目难度中等,正确理解图象中阴影部分的面积所表示的含义为解答本题的关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题
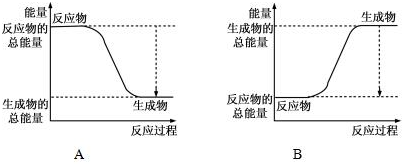
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
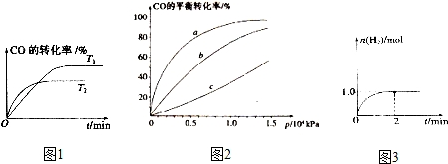
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
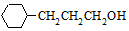 流程图如图
流程图如图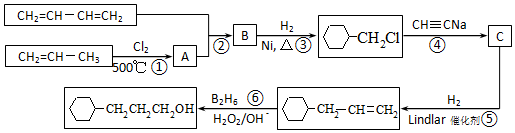
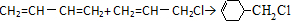 .
.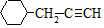 .
.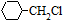 含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式
含有六元环且核磁共振氢谱有4组峰的同分异构体的结构简式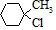 .
.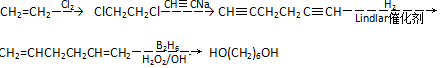 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,80g SO3含有的氧原子数为3NA | |
| B. | 物质的量浓度为0.5 mol•L-1 的MgCl2溶液,含有的Cl- 数目为0.5NA | |
| C. | 常温常压下,22.4L H2中所含原子数为2NA | |
| D. | 标准状况下,22.4L水中所含的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向品红溶液中通入气体X,品红溶液褪色,则气体X可能是Cl2 | |
| B. | CO2中含少量SO2,可将该混合气体通人足量饱和NaHCO3溶液中除去SO2: | |
| C. | 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色,说明该食盐试样中不含KIO3 | |
| D. | 相同体积、pH均为3的HA和HB两种酸的溶液分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
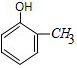 2-甲基苯酚、
2-甲基苯酚、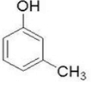 3-甲基苯酚、
3-甲基苯酚、 4-甲基苯酚.
4-甲基苯酚.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com