
【题目】现有HA、HB和H2C三种酸。室温下用0.1mol·L-1NaOH溶液分别滴定20.00 mL浓度均为0.1mol·L-1的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH 溶液体积的变化如图所示。
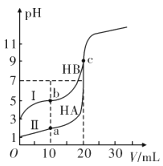
(1)a点时的溶液中由水电离出的c(H+)=________mol·L-1,Ka(HB)=________。
(2)与曲线I 上的c点对应的溶液中各离子浓度由大到小的顺序为________;b点对应的溶液中c(HB)____c(B-)(填“>”“<”或“=”)。
(3)已知常温下向0.1mol·L-1的NaHC 溶液中滴入几滴石蕊试液后溶液变成红色。
①若测得此溶液的pH=1,则NaHC的电离方程式为_______________。
②若在此溶液中能检测到H2C 分子,则此溶液中c(C2-)________c(H2C)(填“>”“<”或“=”)。
③若H2C的一级电离为H2C=H++ HC-,常温下0.1mol·L-1H2C溶液中的c(H+ )=0.11mol·L-1,则0.1mol·L-1NaHC溶液中的c(H+)________0.01mol·L-1(填“>”“<”或“=”)。
【答案】 3×10-13 1×10-5 c(Na+)>c(B-)>c(OH-)>c(H+) < NAHC=Na++H++C2- > >
【解析】(1)由图中曲线I可知,浓度0.1mol·L-1的HA酸溶液的pH=1,说明HA是强酸,完全电离,a点时加入10mL氢氧化钠溶液,则溶液中酸过量, ![]() ,酸抑制水的电离,溶液中由水电离出的c(H+)=
,酸抑制水的电离,溶液中由水电离出的c(H+)=![]() mol·L-1=3×10-13mol/L;由图中曲线Ⅱ可知,浓度0.1mol·L-1的HB酸溶液的pH=3,Ka(HB)=
mol·L-1=3×10-13mol/L;由图中曲线Ⅱ可知,浓度0.1mol·L-1的HB酸溶液的pH=3,Ka(HB)= 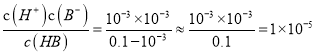 ;(2)曲线I上的c点对应的溶液是HB酸与氢氧化钠完全中和生成的NaB溶液,溶液呈碱性,各离子浓度由大到小的顺序为c(Na+)>c(B-)>c(OH-)>c(H+);b点对应的溶液为以HB和NaB按1:1为溶质的溶液,溶液呈酸性说明HB的电离大于NaB的水解,则c(HB) <c(B-);(3)①若0.1mol·L-1的NaHC溶液的pH=1,则NaHC为强酸的酸式盐,其电离方程式为NAHC=Na++H++C2-;②若在此溶液中能检测到H2C分子,则NAHC是弱酸的酸式盐,溶溶液呈酸性说明HC-电离大于水解,此溶液中c(C2-)>c(H2C);③若H2C的一级电离为H2C=H++HC-,常温下0.1mol·L-1H2C溶液中的c(H+)=0.11mol·L-1,其中一级电离产生的c(H+)=0.1mol·L-1,二级电离不完全电离在第一级电离产生的氢离子抑制下电离的c(H+)=0.01mol·L-1,则0.1mol·L-1NaHC溶液中在没有受抑制情况下电离程度增大,则c(H+)>0.01mol·L-1。
;(2)曲线I上的c点对应的溶液是HB酸与氢氧化钠完全中和生成的NaB溶液,溶液呈碱性,各离子浓度由大到小的顺序为c(Na+)>c(B-)>c(OH-)>c(H+);b点对应的溶液为以HB和NaB按1:1为溶质的溶液,溶液呈酸性说明HB的电离大于NaB的水解,则c(HB) <c(B-);(3)①若0.1mol·L-1的NaHC溶液的pH=1,则NaHC为强酸的酸式盐,其电离方程式为NAHC=Na++H++C2-;②若在此溶液中能检测到H2C分子,则NAHC是弱酸的酸式盐,溶溶液呈酸性说明HC-电离大于水解,此溶液中c(C2-)>c(H2C);③若H2C的一级电离为H2C=H++HC-,常温下0.1mol·L-1H2C溶液中的c(H+)=0.11mol·L-1,其中一级电离产生的c(H+)=0.1mol·L-1,二级电离不完全电离在第一级电离产生的氢离子抑制下电离的c(H+)=0.01mol·L-1,则0.1mol·L-1NaHC溶液中在没有受抑制情况下电离程度增大,则c(H+)>0.01mol·L-1。


科目:高中化学 来源: 题型:
【题目】已知:①2HI+Cl2=2HCl+I2,②2Fe+3Cl2=2FeCl3,③2FeBr2+3Cl2=2FeCl3+2Br2.在一定条件下HI、Fe、FeBr2分别与足量的Cl2反应,如果三个反应电子转移数目相等,则HI、Fe、FeBr2的物质的量之比为
A. 1:1:1 B. 1:3:3 C. 3:1:1 D. 6:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2 mol氢气完全燃烧生成水蒸气时放出能量484 kJ,且氢气中1 mol H—H键完全断裂时吸收能量436 kJ,水蒸气中1 mol H—O键形成时放出能量463 kJ,则氧气中1 mol O=O键断裂时吸收能量为( )
A. 920 kJ B. 557 kJ C. 496 kJ D. 188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有X、Y、Z、W、Q五种短周期元素,它们在周期表中的位置如下图所示。下列说法不正确的是
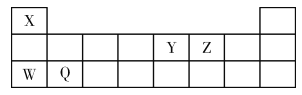
A. W的单质和某些化合物可用于道路照明、漂白剂、制玻璃等
B. 含W、Y、Z三种元素的化合物,其水溶液可能呈中性或碱性
C. X与Y、X与Z形成的简单化合物,分子间都能形成氢键,并且均具有氧化性和还原性
D. Y与Z形成的化合物只有五种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)俗称“工业盐”,其外观与食盐相似,有咸味,有毒,可用做食品防腐剂和肉类食品的发色剂。已知亚硝酸钠能与氢碘酸(HI,具有强酸性)发生如下反应:4HI+2NaNO2=2NaI+I2+2NO↑+2H2O。下列说法正确的是
A. 亚硝酸钠具有氧化性,不可能表现出还原性
B. 该反应中氧化剂与还原剂的物质的量之比为1:1
C. 向反应所得的混合溶液中加入稀硫酸和亚硝酸钠,I-不可能转化为I2
D. 人误食亚硝酸钠中毒时,可服用氢碘酸解毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
元素代号 | X | Y | Z | M | W | Q | R |
原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是________________________________;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______(填离子符号)。
W和R按原子个数比1﹕4构成的阳离子所含的化学键是____________________。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______(填化学
式),其电离方程式为_____________________________________。
(3)M与Z相比,非金属性较强的是_____________(填元素名称),请从原子结构的角度说明理由_________________________________________________________________。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
![]() KMnO4+
KMnO4+![]() H2O2+
H2O2+![]() H2SO4 →
H2SO4 → ![]() K2SO4+
K2SO4+![]() MnSO4+
MnSO4+![]() O2↑+
O2↑+![]() H2O
H2O
请配平,当有0.5 mol H2O2参加此反应,电子转移的个数为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物a和苯通过反应合成b 的过程如图(无机小分子产物略去)。下列说法正确的是
![]()
A. 该反应是加成反应
B. 若R为CH3时,b中所有原子可能共面
C. 若R为C4H9时,取代b苯环上的氢的一氯代物的可能的结构共有4种
D. 若R为C4H5O时,lmolb最多可以与5molH2加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在稀硫酸中,KMnO4和H2O2能发生氧化还原反应。
氧化反应:H2O2-2e-===2H++O2↑
还原反应:MnO4-+5e-+8H+===Mn2++4H2O
(1)写出该氧化还原反应的离子方程式:_______________________。
(2)反应中氧化剂是________;被氧化元素是__________;若有0.5 mol H2O2参加此反应,电子转移个数为____________。
(3)若KMnO4的量不足,在Mn2+的催化作用下,H2O2仍能分解,分解反应的化学方程式为________________________;这时若有0.5 mol H2O2发生分解,电子转移个数为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com