
【题目】氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________(填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

①分析“对金属制品有腐蚀作用”的原因:_______________。
②需“密闭保存”的原因:______________。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________。
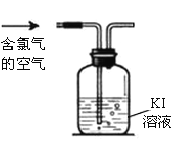
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______。
【答案】 Cl2+2NaOH=NaCl+NaClO+H2O b NaClO有强氧化性,而一般金属具有较强还原性 消毒液的有效成分NaClO能与空气中的CO2作用,使其变质 Cl-+ClO-+2H+=Cl2↑+H2O 通入空气的体积
【解析】本题考查氯及其化合物的性质,(1)氯气与碱反应,其反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O;氯气具有强氧化性,与还原性物质发生反应,A、氯气不与NaCl反应,故错误;B、Fe2+具有还原性,能与氯气反应,不产物有毒物质,故正确;C、KMnO4具有强氧化性,不与Cl2反应,故错误;(2)①因为NaClO具有强氧化性,而一般金属具有较强的还原性,两者发生氧化还原反应,对金属制品有腐蚀作用;②NaClO与空气中CO2发生:2NaClO+CO2+H2O=Na2CO3+2HClO,HClO见光受热分解,会使次氯酸钠失去漂白的性质,因此密封保存;③发生氧化还原反应,产生氯气,离子方程式为ClO-+Cl-+2H+=Cl2↑+H2O。


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】向1 L的密闭容器中加入1 mol X、0.3 mol Z和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是

A.Y的起始物质的量为0.5 mol
B.该反应的化学方程式为:2X(g)+Y(g) ![]() 3Z(g) H<0
3Z(g) H<0
C.若t0=0,t1=10 s,则t0~t1阶段的平均反应速率为v(Z)=0.03 mol/(L·s)
D.反应物X的转化率t6点比t3点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断中一定正确的是( )
A. NaCl及Na2O2固体中阴、阳离子数之比均为1:1
B. 等质量的O2与O3中,氧原子的个数比为3:2
C. 分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2
D. 10 mL 0.3 mol·L-1 NaCl溶液与30 mL 0.1 mol·L-1 AlCl3溶液中Cl -物质的量浓度比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行该反应:2SO2(g)+O2(g)![]() 2SO3(g),已知反应中某一时刻SO2、O2、SO3的浓度为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(g),已知反应中某一时刻SO2、O2、SO3的浓度为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
A. SO2为0.4mol/L、O2为0.2mol/L
B. SO2为0.25mol/L
C. SO2、SO3均为0.15mol/L
D. SO3为0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列晶体属于A1型最密堆积的是( )
A. 干冰、氯化钠、金属铜 B. 硫化锌、金属镁、氮化硼
C. 水晶、金刚石、晶体硅 D. 硫化锌、氯化钠、金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法。
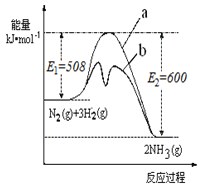
(1)根据如图提供的信息,写出该反应的热化学方程式 ,下图的曲线中 (填“a” 或“b”)表示加入铁触媒(催化剂)的能量变化曲线。
(2)在恒容容器中,下列描述中能说明上述反应已达
平衡的是 。
A.3υ(H2)正=2υ(NH3)逆
B.单位时间内生成n mol N2的同时生成2n molNH3
C.容器内气体的密度不随时间的变化而变化
D.容器内压强不随时间的变化而变化
(3)为了寻找合成NH3的适宜条件,某同学设计了三组实验(如下表),请在下表空格处填入相应的实验条件及数据。
实验编号 | T(℃) | n (N2)/n(H2) | P(MPa) |
ⅰ | 450 | 1/3 | 1 |
ⅱ | 1/3 | 10 | |
ⅲ | 480 | 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备氨基甲酸铵(NH2COONH4)的反应如下:2NH3(g)+CO2(g)![]() NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢氨。
NH2COONH4(s)该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则生成碳酸铵或碳酸氢氨。
(1)该反应在一定条件下能够白发进行,则反应的△H_____________0(填“>”、“<”或“一”)。
(2)写出生成碳酸氢氨的化学方程式:______________。
(3)实验步骤如下:
步骤1:按图所示组装仪器,检查装置的气密性。

步骤2:在相应仪器中装入药品,其中在三颈烧瓶中加入氢氧化钠固体,恒压滴液漏斗中装入浓氨水。
步骤3:滴加浓氨水并搅拌,调节反应速率,在反应器中得到产品。
干燥管中盛放的药品是___________。
对比碳酸盐和酸反应制CO2,该实验利用干冰升华产生CO2气体的优点是__________________。
③以恒压滴液漏斗代替分液漏斗的目的是______________________。
(4)该实验装置可能存在的安全问题是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两个完全相同的装置,某学生分别在它们的侧管中装入一定量的Na2CO3和NaHCO3,A、B中分别装有足量的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是
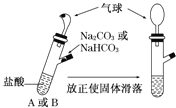
A. 侧管中装入Na2CO3的气球膨胀速率大
B. 若加入等质量的Na2CO3和NaHCO3 ,最终两气球体积不同
C. 最终两试管中Na+、Cl-的物质的量一定相同
D. 热稳定性:Na2CO3 < NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com