
| A.固体CH3COOK | B.固体CH3COONH4 | C.气体NH3 | D.固体NaHCO3 |


科目:高中化学 来源:不详 题型:单选题
| A.4 | B.6 | C.8 | D.10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,pH=5的NaHSO3溶液中:c(HSO3一)>c(SO32一)>c(H2SO3) |
| B.在0.1mol·L一1NaHCO3溶液中有: c(Na+) +c(H+)=c(HCO3一) + c(CO32-) + c(H2CO3) |
| C.在0.1mol·L一1Na2CO3溶液:c((HCO3-) + 2c(H2CO3) +c(H+)=c(OH-) |
| D.常温下,将10mL0.lmol.L一1的盐酸与20mL0.1mol.L一1的氨水混合,所得溶液中:. |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.用标准溶液润洗滴定管2~3次 |
| B.取标准KOH溶液注入碱式滴定管至刻度0以上2~3cm |
| C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.调节液面至0或0以下刻度,记下读数 |
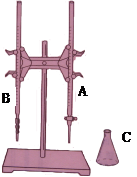
| 实验次数 | c(KOH)/mol·L-1 | B中起点刻度 | B中终点刻度 | V(HCl)/ml |
| 1 | 0.1000 | 0 | 24.95 | 25.00 |
| 2 | 0.1000 | 0 | 24.96 | 25.00 |
| 3 | 0.1000 | 0 | 24.50 | 25.00 |
| 4 | 0.1000 | 0 | 24.94 | 25.00 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H++ OH-,若要使水的电离程度增大,并使c(H+)增大,应加入的物质为
H++ OH-,若要使水的电离程度增大,并使c(H+)增大,应加入的物质为| A.NaHSO4 | B.KAl(SO4)2 | C.NaHCO3 | D.CH3COONa |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.7 | B.2.0 | C.12.0 | D.12.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液呈中性,可选用甲基橙或酚酞作指示剂 | B.溶液呈中性,只能选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 | D.溶液呈碱性,只能选用酚酞作指示剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.c(SO42-)>c(H+)>c(NH4+)>c(OH-) | B.c(H+)>c(SO42-)>c(NH4+)>c(OH-) |
| C.c(OH-)-c(NH4+)=c(H+)-2c(SO42-) | D.c(OH-)+c(NH3·H2O)=c(H+)-c(SO42-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com