
| A、石灰水 | B、氢氧化钠溶液 |
| C、硫酸 | D、氨水 |
科目:高中化学 来源: 题型:
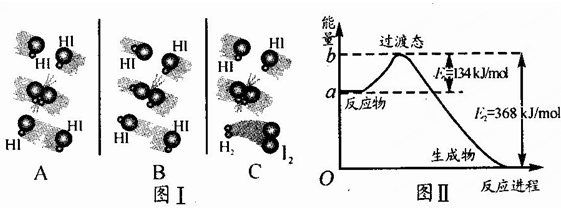
查看答案和解析>>
科目:高中化学 来源: 题型:
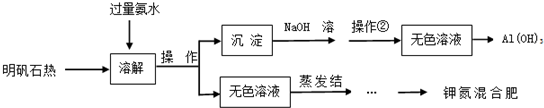
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
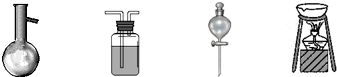
| A、蒸馏、蒸发、分液、升华 |
| B、蒸馏、洗气、分液、蒸发 |
| C、蒸馏、分液、过滤、升华 |
| D、蒸发、分液、过滤、蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
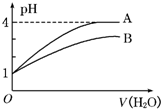 常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中正确的是( )| A、A酸比B酸的电离程度小 |
| B、pH=1时,B酸的物质的量浓度比A酸大 |
| C、B酸比A酸容易电离 |
| D、A是强碱,B是弱碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油的裂化和裂解可以得到烯烃 |
| B、石油的催化重整是获得芳香烃的主要途径 |
| C、石油分馏出的各馏分均是纯净物 |
| D、煤干馏产生的煤焦油经分馏可得到芳香烃 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com