
| 离子 | Na+ | Al3+ | Cl- | X |
| 个数 | 2a | a | a | b |
| A. | NO3-、2a | B. | SO42-、2a | C. | OH-、2a | D. | SO42-、4a |
科目:高中化学 来源: 题型:选择题
| A. | 不含其他杂质的天然油脂属于纯净物 | |
| B. | 油脂在酸性条件下水解称为皂化 | |
| C. | 油脂的烃基部分饱和程度越大,熔点越低 | |
| D. | 各种油脂水解后的产物中都有甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
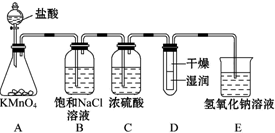
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:2 | C. | 8:7 | D. | 7:8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、CH3COO-、Na+、Cl- | B. | Na+、NO3-、NH4+、SO42- | ||
| C. | Fe2+、NO3-、Na+、SO42- | D. | Na+、HCO3-、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 实验Ⅰ:液体分层,下层呈无色 | |
| B. | 实验Ⅱ:烧杯中先出现白色沉淀,后溶解 | |
| C. | 实验Ⅲ:试管中溶液颜色先变为灰绿色后迅速变为红色 | |
| D. | 实验Ⅳ:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可以与酸性高锰酸钾溶液反应 因此可以用酸性高锰酸钾溶液除去乙烷中的乙稀 | |
| B. | 溴乙烷可以通过乙稀与溴化氢加成得到 也可以通过乙烷与溴发生取代反应制备 | |
| C. | 区分甲苯和苯可以用酸性高锰酸钾溶液也可以用溴水 | |
| D. | 鉴别己烯是否混有少量甲苯 正确的实验方法是可以加足量溴水 然后再加入酸性高锰酸钾溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12的烷烃,含有3个甲基结构的同分异构体有2种 | |
| B. | 乙烷、乙醇、乙酸、苯、纤维素、油脂、蛋白质均能发生取代反应 | |
| C. | 甲烷、苯都属于烃,都不存在同分异构体 | |
| D. | 相同质量的甲烷和乙烷完全燃烧,乙烷耗氧量多 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯元素的相对原子质量为$\frac{12}{b}$ | |
| B. | m g该氯原子的物质的量为$\frac{m}{a{N}_{A}}$ mol | |
| C. | 该氯原子的摩尔质量是aNAg | |
| D. | n g该氯原子所含的电子数是$\frac{17n}{a}$个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com