
【题目】回答下列关于NO、NO2的问题:
(1)汽车排气管上装有催化转化器可减少尾气对环境的污染,汽车尾气中的有害气体CO和NO反应可转化为无害气体排放,写出相关反应的化学方程式:___________________
(2)工业生产中利用氨水吸收SO2和NO2,原理如图所示:
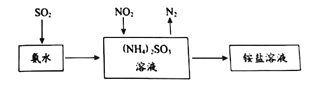
NO2被吸收后生成的铵盐是____________(填化学式);为证明溶液中NH4+的存在,可向少量铵盐溶液中加入___________溶液。
【答案】2CO+2NO![]() N2和2CO2 (NH4)2 SO4 NaOH
N2和2CO2 (NH4)2 SO4 NaOH
【解析】
二氧化硫通入氨水中生成亚硫酸铵,利用亚硫酸铵中SO32-的还原性吸收NO2,SO32-被氧化为SO42-,NO2被还原为N2,最后得到(NH4)2 SO4溶液。
(1)汽车尾气中的有害气体CO和NO反应可转化为无害气体N2和CO2,其化学反应的化学方程式:2CO+2NO![]() N2和2CO2,故答案为:2CO+2NO
N2和2CO2,故答案为:2CO+2NO![]() N2和2CO2;
N2和2CO2;
(2)由流程图知,二氧化硫通入氨水中生成亚硫酸铵,利用亚硫酸铵中SO32-的还原性吸收NO2,SO32-被氧化为SO42-,NO2被还原为N2,离子方程式为:
2NO2+4(NH4)2 SO3= N2+4(NH4)2 SO4,NO2被吸收后生成的铵盐为(NH4)2 SO4,检验溶液中的NH4+,向溶液中滴加氢氧化钠溶液加热,并用湿润的红色石蕊试纸检证产生的气体,试纸变蓝,就证明有NH4+,所以为证明溶液中NH4+的存在,可向少量铵盐溶液中加入氢氧化钠溶液,故答案为:(NH4)2 SO4;NaOH;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】甲酯除草醚是一种光合作用抑制剂,能被叶片较快地吸收,但在植物体内传导速度较慢,它是芽前除草剂,主要用于大豆除草等。工业上通常用烃A进行合成,其合成路线如下:
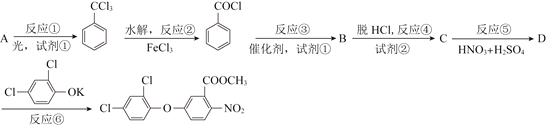
已知:![]()
![]() RCH=O+H2O(R代表烃基)
RCH=O+H2O(R代表烃基)
(1)试剂①为:_____________,试剂②为___________。
(2)写出A的结构简式_____________。
(3)写出下列反应的化学方程式:反应①____________。反应⑤____________。
(4)由于苯环和侧链基团的相互影响,新引进苯环的基团在苯环上取代的位置由原有基团决定,如:苯酚分子中“![]() ”使苯环上_________
”使苯环上_________![]() 选编号填空,下同
选编号填空,下同![]() 的H原子容易被取代;根据题目信息可知“
的H原子容易被取代;根据题目信息可知“![]() ”使苯环上________的H原子容易被取代。
”使苯环上________的H原子容易被取代。
![]() 邻位
邻位 ![]() 间位
间位 ![]() 对位
对位
(5)反应②须在饱和![]() 溶液中进行,若在NaOH溶液中进行,则会进一步水解,试写出
溶液中进行,若在NaOH溶液中进行,则会进一步水解,试写出![]() 在足量NaOH溶液中完全水解的化学反应方程式_________________
在足量NaOH溶液中完全水解的化学反应方程式_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家借助自主研制的新型钨钴铁合金催化剂攻克了单壁碳纳米管结构的可控制备难题。海底金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源,含有钨、铁、锰、锌、钴等。
(1)基态钴原子的核外未成对电子数为__________。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为__________。
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲醛分子属__________(填“极性”或“非极性”)分子,其中心原子的VSEPR构型为__________。
(3)六羰基钨[W(CO)6]的熔点为172℃,是一种重要的无机金属配合物,可溶于多数有机溶剂。三种组成元素的电负性由大到小的顺序为 __________(用元素符号表示)。配体CO中与W形成配位键的原子是C而不是O,原因是 ____________。
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是 ____________(填字母)。
A.苯 B.二氧化硫 C.四氯化碳 D.环己烷
(5) Fe2+、Fe3+能与CN-形成络离子,其晶胞结构如图1所示。该离子可形成铁蓝钾盐,该钾盐的化学式为___________。
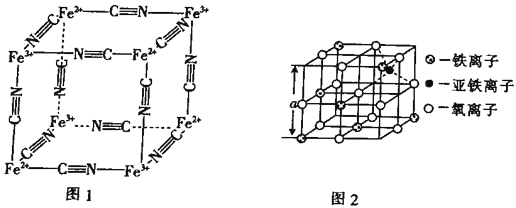
(6)图2是从铁氧体离子晶体Fe3O4中取出的能体现其晶体结构的一个立方体,该立方体是不是Fe3O4的晶胞__________(填“是”或“否”);立方体中铁离子处于氧离子围成的 _________(填空间结构)空隙;根据上图计算Fe3O4晶体的密度为 ________gcm-3。(图中a=0.42nm,计算结果保留两位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.2mol丁烷完全裂解生成乙烯的分子数一定为0.2NA
B.13gNaN3爆炸分解为Na和N2 , 转移电子数为0.2NA
C.1L0.1mol·L-1(NH4)2SO3溶液中,含NH4+数目为0.2NA
D.0.2molN2O4充入密闭容器中,产生气体分子总数为0.4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于平衡常数的说法正确的是:
A.K不变,平衡可能移动
B.同一个反应的化学计量数增大2倍,K值也增大两倍
C.K值越大,反应速率也越快
D.对于合成氨反应,压强增大,平衡右移,K增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒定温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A (g)+2B (g)4C (?)+2D (?),“?”代表状态不确定。反应一段时间后达到平衡,测得生成 1.6 mol C,且反应前后压强之比为5:4,则下列说法正确的是
A.增加C,B的平衡转化率不变
B.此时B的平衡转化率是35%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.该反应的化学平衡常数表达式是K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钙[Ca(NO2)2]是易溶于水的无色晶体,可用作水泥硬化促进剂和防冻阻锈剂等。实验室可通过反应Ca(NO3)2+CaFe2O4+NO→Ca(NO2)2+Fe2O3(未配平)制备高纯度的亚硝酸钙,装置如图所示:
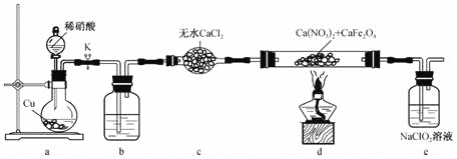
下列说法错误的是( )
A.装置b中盛放的试剂为浓硫酸 B.向烧瓶中加入稀硝酸前需打开K
C.装置e主要用于除去尾气中的NO D.d中每生成1 mol Ca(NO2)2,转移 ![]() mol电子
mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将a g二氧化锰粉末加入b mol/L的浓盐酸c L中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是
A.可以收集到氯气![]() L
L
B.NA可表示为:![]()
C.反应后溶液中的Cl―数目为:![]()
D.反应后溶液中的H+数目为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.1molN2O4气体通入体积为lL的恒容密闭容器中,立即出现红棕色。在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法正确的是( )
A.压缩容器,颜色变浅
B.在平衡时体系内含N2O40.04mol
C.以N2O4的浓度变化表示的平均反应速率为0.002mol/(L·s)
D.平衡时,如果再充入一定量N2O4,则可提高N2O4的转化率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com